Природная вода, содержащая большое количество растворенных солей кальция, магния и железа, называется жесткой. Различают общую, временную (карбонатную) и постоянную (некарбонатную) жесткость.
Общей жесткостью называется суммарная концентрация ионов Са2+, Mg2+ и Fe2+ в воде, выраженная в мольэкв/л. Общая жесткость воды равна сумме постоянной и временной жесткости.
Постоянной жесткостью называется часть общей жесткости, остающаяся после кипячения воды при атмосферном давлении в течение определенного времени. Постоянную жесткость воды называют также некарбонатной жесткостью, так как она обусловлена наличием сульфатов, хлоридов кальция, магния и железа.
Временной жесткостью называется часть общей жесткости, удаляющаяся кипячением воды при атмосферном давлении в течение определенного времени. Она равна разности между общей и постоянной жесткостью. Временную жесткость называют также карбонатной жесткостью, т.к. она обусловлена наличием гидрокарбонатов кальция и магния.
По величине жесткости воду делят на 6 классов.
| Классы | Жесткость воды (моль экв/л) |
| 1 – очень мягкая | 0 – 1,5 |
| 2 – мягкая | 1,5 – 3,0 |
| 3 – средней жесткости | 3,0 – 4,5 |
| 4 – довольно жесткая | 4,5 – 6,0 |
| 5 – жесткая | 6,0 – 10,0 |
| 6 – очень жесткая | свыше 10,0 |
Процесс, приводящий к снижению жесткости воды, называется ее умягчением.
Существующие способы умягчения можно разделить на 3 группы:
- термическое умягчение воды;
- реагентные методы умягчения воды;
- умягчение воды методом обмена ионов.
Для устранения временной жесткости воды применяют
- термическое умягчение (кипячение):
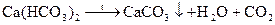
- реагентное умягчение гашеной известью:


Для устранения общей жесткости методом осаждения используют
- карбонат натрия (соду):


- фосфат натрия (тринатрийфосфат):

В последнее время для очистки воды стали широко применять иониты (ионообменные смолы):

Обменная емкость катионита (ε) определяется из соотношения:
 ,
,
где V – объем воды, пропущенной через катионит, л,
m – масса катионита, г.
Обменная емкость выражается в моль экв/г.
Общая жесткость воды может быть рассчитана по формуле:
 ,
,
где: m1, m2, m3 – массы содержащихся в воде катионов кальция, магния или соответствующих им солей, мг;
Мэкв1, Мэкв2, Мэкв3 – молярные массы эквивалентов металлов или соответствующих им солей, г/моль экв;
V – объем воды, л.
 2017-11-01
2017-11-01 236
236








