Благородные металлы (БМ) относятся к категории благородных. БM не взаимодействуют с O2, как на холоду, так и при повышенной температуре, не взаимодействуют с S2, поэтому в природе находятся не в виде сульфидов, оксидов, а в самородном виде.
С Cl взаимодействуют только при высоких температурах.
С Br взаимодействуют на холоду, с I – при нагревании.
В растворах щелочей, органических и неорганических кислот все металлы
(за исключением Ag и Pd) не растворяются. Но они растворяются во многих типах растворителей, например:
1. Царская водка (HNO3 + HCl);
2. CN-;
3. Жидко - фазное хлорирование [Cl2 + HCl (NaCl)];
4. Тиомочевина.
a) неправильный вариант:
 Au + Cl2 + HCl AuCl3 +…
Au + Cl2 + HCl AuCl3 +…
j0Au/Au 3+ = +1.5 B;
j0Cl2/Cl- = +1.36 B.
DG0 < 0; DG0= - nFE.
E= j0ок - j0восст > 0;
1.36 - 1.5 < 0.
б) правильный вариант:
 Au + 3/2Cl2 + HCl H[AuCl4]
Au + 3/2Cl2 + HCl H[AuCl4]
DG0= - nFE; E0 > 0.
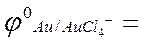 | 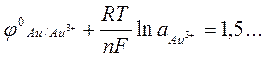 | ||
E0 = j0Cl/Cl- - j0 Au/AuCl4- = 1.36 -...
 H[AuCl4] H+ + [AuCl4]-;
H[AuCl4] H+ + [AuCl4]-;
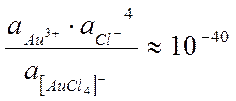 |
 [AuCl4]- Au3+ + 4Cl-.
[AuCl4]- Au3+ + 4Cl-.
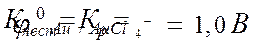 |
E0 > 0; DG0 < 0.
Благородные металлы могут быть переведены в раствор различными системами. Необходимыми условиями являются:
1. Hаличие в системе окислителя с высоким электродным потенциалом;
2. Наличие иона – комплексообразователя, который способен образовывать
с металлами прочные комплексные соединения, что приводит к снижению потенциала металла в растворе его соли.
Например:


 HNO3+HCl = Cl2+NO*Cl+H2O.
HNO3+HCl = Cl2+NO*Cl+H2O.

 NO + Cl
NO + Cl
NO2 O2

|
|
 Au + HNO 3 + HCl H[AuCl4] + NO2 + H2O;
Au + HNO 3 + HCl H[AuCl4] + NO2 + H2O;

 Au + NaCN + O 2 Na[Au+(CN)2] + NaOH;
Au + NaCN + O 2 Na[Au+(CN)2] + NaOH;
 Au + Thio + Fe2(SO4)3 + H2SO4 = [Au+(Thio)2]2SO4 + FeSO4 +…
Au + Thio + Fe2(SO4)3 + H2SO4 = [Au+(Thio)2]2SO4 + FeSO4 +…
CNS-; S2O3; Br2+Br -; I2 + I-.
 2014-01-25
2014-01-25 787
787








