1. Hейтрализация цианистых растворов с отгонкой образующихся HCN и последующим улавливанием ее щелочным раствором.
Исходная пульпа (рН=10 ¸ 11) подкисляется H2SO4 до рН=2,5 ¸ 2,8.
При этом под действием H2SO4 происходит разложение простых и некоторых комплексных соединений.
NaCN + H2SO4 = HCN + Na2SO4
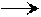 [Zn(CN)4]2- + H2SO4 HCN +ZnSO4
[Zn(CN)4]2- + H2SO4 HCN +ZnSO4
НСN удаляется в газовую фазу, улавливается NaOH, происходит регенерация NaCN (достоинство метода).
Недостатки: не регенерируется значительная часть комплексных соединений, поэтому очистки до ПДК не происходит.
2. Oбработка цианистой пульпы сульфатом Fe(II) (солью Мора).
Преследуется цель: связать простые растворимые токсичные соединения в
нетоксичные растворимые или нерастворимые соединения: Fe(CN)6]3-, [Fe(CN)6]4-, Fe(CN)2.
Недостатки:
- очистки до ПДК нет;
- не разрушаются CNS–;
- возможен переход нетоксичных соединений снова в токсичные.
3. Oкислительные методы;
Суть их основана на обработке цианистой пульпы окислителями, которые окисляют все группы цианистых соединений и роданидов, разрушают при этом CN–, переводя его в безвредные CO32- , NH4+ или N2.
Очистка этими методами ведется до ПДК.
Действующим методом в этой группе является:
a) Xлорный метод;
В качестве окислителя используют NaClO, Ca(ClO)2, CaOCl2 или Cl2.
CN- + ClO- = CNO- + Cl-;
хлорат- цианат-
ион ион
CNO- +2H2O = CO32- + NH4+;
CNS- +4ClO + 2OH- = CNO- + 4Cl- + SO42- + H2O;
[Cu(CN)3]2- + 7ClO- + 2OH- + H2O = 2Cu(OH)2 + 6CNO- + 7Cl-.
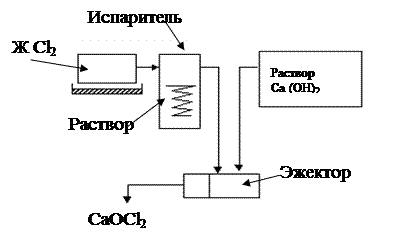
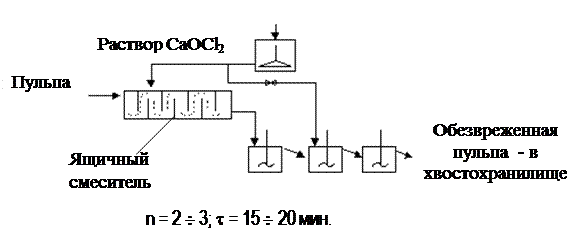
Обезвреживание с помощью жидкого хлора ведется по следующей схеме:
Достоинства: очистка до ПДК.
Недостатки:
- использование токсичного хлор-газа;
- дорогой метод;
- образование ионов хлора, что приводит к “засаливанию” воды.
 | |||
 |
б) Метод озонирования
Считается перспективным.
В качестве окислителя используется озон: О3=О2 + О
Он образуется при воздействии электрического разряда на воздух (или кислород):
CN- + O = CNO-
CNO- + H2O = CO32- + NH4+ и т.д.
Очистка ведется до ПДК, но не нужны ни какие дополнительные реагенты и не образуется побочных продуктов.
Недостаток: высокая стоимость электроэнергии необходимой для получения озона.
в) Анодное окисление
Заключается в пропускании раствора через электролизер с нерастворимыми анодами и катодами. Метод применяют для пульп с высокой концентрацией CN-.
На аноде:
 CN- + 2OH- = CNO-+ 2H2O +2e;
CN- + 2OH- = CNO-+ 2H2O +2e;
[Cu(CN)3]2- + 8OH- = Cu(OH)2 + 3CNO- + 3H2O - +7e;
CNS- + 10OH- = CNO- + SO42- + 5H2O +8e
2CNO- + 4OH- = 2CO2 + N2 + 2H2O +6e
Недостатки: высокий расход электроэнергии.
Известны и другие методы (сорбции на анионитах, экстракция), не вышедшие из стадии лабораторных исследований.
 2014-01-25
2014-01-25 791
791








