Устойчивости сопряженной кислоты, возникающей после присоединения протона к основанию.
Электроотрицательности атома, несущего неподеленную пару электронов.
Чем больше электроотрицательность, тем выше основные свойства.
Так как электроотрицательность О > S, то основные свойства
С2 Н5 О Н > С2 Н5 S Н
RNH2 + H + —> RN H3 +
ROH + H + —> R O+ –H
|
H
Ион аммония более устойчив, чем ион оксония, поскольку присоединение про-
тона Н + к электронной паре энергетического уровня 2s2 атома азота энергетически более выгодно, чем к паре электронов энергетического уровня 2 р2 атома кислорода (хотя атом кислорода обладает большей электроотрицательностью).
Заместители- доноры увеличивают электронную плотность в основном центре и этим увеличивают основные свойства.
СН3 NH 2 < C 2H 5 NH2 < (C 2H 5) 2 NH
Заместители акцепторы уменьшают электронную плотность в основном центре и
уменьшают основные свойства.
НО- СН 2 - СН 2 - NH2 < СН 3 - СН 2 - NH2
акцептор донор
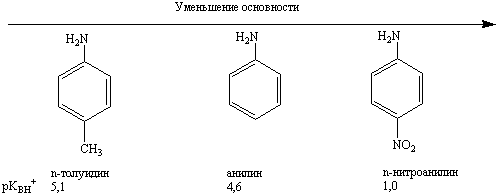
Основные свойства ароматических аминов ниже, чем алифатических, поскольку неподеленная пара электронов атома азота взаимодействует с электронной системой бензольного цикла, и электронная плотность на атоме азота снижается.
С6 Н 5 - NH2 < СН3 NH 2
анилин метиламин
Таким образом, спирты, амины обладают кислотными и основными свойствами.
У спиртов преобладают кислотные над основными, а у аминов- основные над
кислотными.
Следует помнить:
 2014-01-31
2014-01-31 969
969








