Ферменты ускоряют химические реакции, снижая энергию активации.
Чтобы сделать молекулы вещества реакционноспособными, нужно сообщить им дополнительное количество энергии – это энергия активации, т.е. количество энергии в калориях, которое необходимо для перевода при данной температуре всех молекул 1 моля вещества в активное состояние.
КАТАЛИЗ приводит к ускорению достижения равновесия за счет снижения энергии активации (Еа), часто ступенчато.
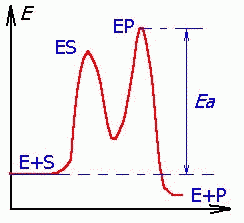
Катализаторы понижают энергию активации и таким образом ускоряют химические реакции. При этом катализатор (фермент) Е взаимодействуют с субстратом S с образованием комплекса фермент-субстрат ЕS. Этот комплекс обладает более низкой энергией активации. Затем комплекс распадается на продукт Р и свободный фермент Е.
 Е + S Е S Р + Е
Е + S Е S Р + Е
Фермент субстрат фермент продукт свободный
субстратный фермент
комплекс
Таким образом, в основе ферментативной реакции лежит образование фермент-субстратного комплекса. Он образуется в результате взаимодействия субстрата с активным центром фермента. Активный центр образуется обычно из 3-5 остатков аминокислот. Они могут находиться на большом расстоянии друг от друга в полипептидной цепи, но цепь приобретает такую конформацию, что эти аминокислотные остатки сближаются и образуется активный центр. Таким образом, активность фермента зависит от пространственной конформации.
Отличительное свойство ферментов состоит в том, что ферменты не расходуются в ходе реакции и не претерпевают необходимых изменений.
 2014-01-31
2014-01-31 756
756








