
Сначала получают термические кривые. Полученные точки переносят на диаграмму, соединив точки начала крист-ции сплавов и точки конца крист-ции, получают диаграмму состояния.
Анализ: 1. Количество компонентов: К = 2 (компоненты А и В). 2. Число фаз: Ф = 2 (жидкая фаза L, кристаллы твердого раствора  )3. Основные линии диаграммы:acb –ликвидус, выше этой линии сплавы находятся вЖ сос-ии;
)3. Основные линии диаграммы:acb –ликвидус, выше этой линии сплавы находятся вЖ сос-ии;
adb –солидус, ниже этой линии сплавы находятся в Т.4. Характерные сплавы системы:Чистые компоненты А и В крист-ся при t=const.
Пр-сс крист-ции сплава I: до точки 1 охл-ся сплав вЖ сос-нии. При t, соответствующей точке 1, начинают образ-ся центры крист-ации тв. р-ра  . На кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты крист-ции. На участке 1–2 идет пр-сс крист-ции, протекающий при понижающейся t, т.к согласно правилу фаз в двухкомпонентной сис-ме при наличии 2 фаз (Ж и тв.р-ор
. На кривой охлаждения отмечается перегиб (критическая точка), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты крист-ции. На участке 1–2 идет пр-сс крист-ции, протекающий при понижающейся t, т.к согласно правилу фаз в двухкомпонентной сис-ме при наличии 2 фаз (Ж и тв.р-ор  ) число степеней свободы будет =1
) число степеней свободы будет =1  . При t соотв-щей точке 2, сплав затвердевает, при дальнейшем понижении t охл-ся сплав в Т сос-ии, состоящий из однородных кристаллов тв.р-ора
. При t соотв-щей точке 2, сплав затвердевает, при дальнейшем понижении t охл-ся сплав в Т сос-ии, состоящий из однородных кристаллов тв.р-ора  .
.
Рис. 5.2. Схема микроструктуры сплава – однородного твердого раствора
5. Кол-ный структурно-фазовый анализ сплава.
Пользуясь диаграммой можно для любого сплава при любой t опр-ть не только число фаз, но и их состав и кол-нное соотношение. Для этого используется правило отрезков. Для проведения кол-нного структурно-фазового анализа через заданную точку проводят горизонталь (коноду) до пересечения с ближайшими линиями диаграммы (ликвидус, солидус или оси компонентов).
а). Опр-ние состава фаз в точке m: Для его опр-ния через точку m проводят горизонталь до пересечения с ближайшими линиями диаграммы: ликвидус и солидус.СоставЖ фазы опр-ся пр-цией точки пересечения горизонтали с линией ликвидус p на ось конц-ции.СоставТ фазы опр-ся пр-цией точки пересечения горизонтали с линией солидус q (или осью компонента) на ось конц-ции.
СоставЖ фазы изм-тся по линии ликвидуса, а состав Т фазы – по линии солидуса.С понижением t состав фаз изменяется в сторону уменьшения содержания комп-та В.
б). Опр-ие кол-нного соотношенияЖ и Т фаз при заданной t (в точке m):
Кол-нная масса фаз обратно пропорциональна отрезкам проведенной коноды.
 Кол-во всего сплава (Qсп) опр-ся отрезком pq.О трезок, прилегающий к линии ликвидус pm, определяет кол-воТ фазы.
Кол-во всего сплава (Qсп) опр-ся отрезком pq.О трезок, прилегающий к линии ликвидус pm, определяет кол-воТ фазы.
 Отрезок, прилегающий к линии солидус (или к оси компонента) mq, определяет количество жидкой фазы.
Отрезок, прилегающий к линии солидус (или к оси компонента) mq, определяет количество жидкой фазы.
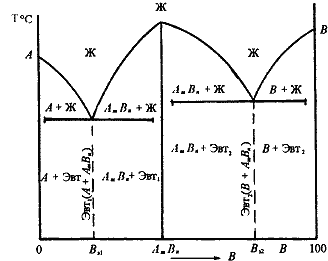
12.Диаграмма состояния сплавов с образованием химического соединения.
Диаграмма состояния сложная, состоит из нескольких простых диаграмм. Число компонентов и количество диаграмм зависит от того, сколько химических соединений образуют основные компоненты системы. Число фаз и вид простых диаграмм определяются характером взаимодействия между компонентами.
Эвт1 (кр. А + кр. AmBn);Эвт2 (кр. B + кр. AmBn).
Такая диаграмма получается (рис. 3.1д), когда сплавляемые компоненты образуют устойчивое химическое соединение АnВm, не диссоциирующее при нагреве вплоть до температуры плавления и образующее промежуточную фазу постоянного состава. Химическое соединение считается устойчивым, если оно плавится без разложения.При концентрации, соответствующей химическому соединению АnВm, отмечается характерный перелом на кривой свойств. Это объясняется тем, что некоторые свойства химических соединений обычно резко отличаются от свойств образующих их компонентов. Обычно такие диаграммы состояния характерны для систем, образованных металлами и элементами, которые обладают и металлическими, и неметаллическими свойствами.
В ряде диаграмм состояния сплавов, образующих химические соединения (рис. 3.2е), могут возникать промежуточные фазы переменного состава (δ -фаза), имеющие сравнительно широкие области существования. Эти фазы представляют собой твердые растворы замещения или внедрения в кристаллической решетке химического соединения. Для этих фаз обычно характерны свои кристаллические решетки, отличные от кристаллических решеток компонентов.Помимо устойчивых химических соединений, которые плавятся (кристаллизуются) при постоянной температуре, в диаграммах могут образовываться и неустойчивые химические соединения, распад которых происходит, не доходя до температуры плавления.
 2018-03-09
2018-03-09 190
190








