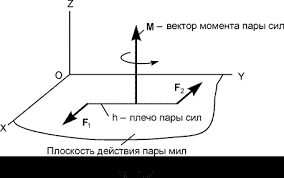
Скорость протекания реакций типа R23 — К24 весьма велика. Кроме того, на поверхности частиц могут резко ускоряться реакции молекулярного окисления, например реакция R20, а также осуществляться реакции окисления перекисью водорода:
R 25 (S02)адс + (H2 O2)адc " (SO42- )адс + 2 (Н+)адc.
Общий эффект гетерогенных реакций в окислении диоксида серы в существенной степени зависит от концентрации частиц, площади поверхности на единицу объема, физико-химических свойств поверхности и т. д. Немаловажным обстоятельством является и то, что при достаточно высокой относительной влажности поверхность частиц покрывается слоем молекул воды. При 25 0С и относительной влажности 60 — 70% частицы летучей золы покрыты слоем воды, который меньше мономолекулярного, а при относительной влажности 90 % — несколькими молекулярными слоями воды. В условиях высокой влажности скорость окисления диоксида серы может возрасти на 1— 2 порядка. Естественно, что на первом этапе существования дымового факела скорость окисления диоксида серы может быть высокой, но по мере очищения атмосферы от частиц, снижения их объемной концентрации и насыщения поверхности, вероятность протекания гетерогенных реакций будет уменьшаться. В меняющихся условиях факела обобщенный коэффициент скорости гетерогенных реакций может находиться в пределах 0,3 — 0,003 ч -1. Для условий реальной атмосферы над крупным промышленным районом эту скорость можно принять равной 0,01 ч -1, а соответствующее время жизни диоксида серы относительно гетерогенных реакций — 100 ч. -1
Третьим механизмом окисления диоксида серы служит окисление в жидко капельной фазе облаков и туманов. При этом могут протекать следующие реакции:
R26 (S02)раств + Н20 ® Н+ + HSO3
R27 НS0з + (02)раств ®. НS05-.;
R28 HSO5- + НS0з- ® 2НS04-;
R29 (SO2)pаств + Н2О + Оз ® Н+ + НS04- +О2
R30 (SО2)раств + Н2О + Н 2О2 ® Н+ + HSO4- + Н2О
Перечисленные реакции могут иметь каталитический характер, при этом их скорость возрастает на 1— 2 порядка. В качестве катализаторов могут выступать, например, ионы марганца и железа, концентрация которых в дождевых осадках над промышленными регионами составляет соответственно 3 10 -7 и 4 10 -6моль/л. Скорость окисления диоксида серы в собственно жидкой фазе весьма высока (обобщенная константа скорости превышает 1 ч -1). Однако скорость выведения диоксида серы из атмосферы этим механизмом определяется не только химическими реакциями, но и вероятностью попадания молекулы в жидко капельную фазу. Эта вероятность в свою очередь зависит от множества факторов: климатических условий региона, времени года, высоты выброса диоксида серы относительно земной поверхности, значения рН облачных и дождевых капель и т. д. Например, для европейского региона с характерным для него распределением «сухих» и «мокрых» периодов коэффициент скорости окисления диоксида серы в жидкофазных реакциях можно оценить в 0,007 ч -1 (соответствующее время жизни — 140 ч).
Скорость окисления диоксида серы не постоянна во времени и снижается по мере удаления воздушных масс от источника загрязнения. Функциональная зависимость скорости окисления диоксида серы от времени переноса загрязненных воздушных масс:
КS = 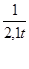 (1.7)
(1.7)
где КS — обобщенная константа скорости окисления диоксида серы, ч -1, t — время переноса загрязненных воздушных масс, ч. Эта эмпирическая формула справедлива для диапазона 3 ч<t <25 ч, что, по нашему определению, соответствует расстояниям переноса регионального масштаба. Необходимо заметить, что формула (1.7) получена для условий сухой погоды (относительная влажность менее 75 %), поэтому она не учитывает окисления в жидко капельной фазе и, возможно, недоучитывает гетерогенного окисления.
Получена зависимость скорости окисления от интенсивности солнечного света и концентраций озона в окружающем воздухе:
КS =(0,03 + 0,01) (RH[03]0), (1.8)
где R — поток солнечной радиации на уровне земной поверхности, кВт/м2,Н — высота слоя перемешивания факела, м; [Оз]о — концентрация озона в окружающем факел воздухе, млн -1.
Образовавшаяся в результате окисления диоксида серы серная кислота в дальнейшем частично или полностью нейтрализуется. Основным нейтрализующим щелочным агентом выступает аммиак, что подтверждается данными химического анализа сульфатов, которые на 60 — 90 % состоят из сульфата или бисульфата аммония. Реакция нейтрализации проходит, как правило, в жидкой фазе или на поверхности полужидких частиц. Следовательно, скорость нейтрализации будет определяться содержанием в атмосфере аммиака, и зависеть от наличия жидко капельной и аэрозольной фазы. Оценки показывают, что для европейского региона скорость нейтрализации серной кислоты при переносе в атмосфере составляет 0,02 ч -1, а соответствующее время жизни (среднее) — 50 ч.
 2020-01-14
2020-01-14 107
107