Введение
В настоящее время вода широко используется в различных областях промышленности в качестве теплоносителя и рабочего тела, чему способствует широкое распространение воды в природе и ее особые термодинамические свойства, связанные со строением молекул. Полярность молекул воды, характеризуемая дипольным моментом, определяет большую энергию взаимного притяжения молекул воды (ориентационное взаимодействие) при температуре 10…30 С и соответственно большую теплоту фазового перехода при парообразовании, высокую теплоемкость и теплопроводность. Значение диэлектрической постоянной воды, также зависящей от дипольного момента, определяет своеобразие свойств воды как растворителя.
При нагреве воды на поверхностях нагрева образуются твердые отложения накипеобразующих солей. При испарении воды в пар переходят коррозионно-активные газы, которые способствуют разрушению поверхности охлаждения и генерируют новые вещества, образующие отложения из продуктов коррозии.
Надежность работы энергетического оборудования на станции непосредственно связана с качеством подпиточной воды котлов. Правильно рассчитанный, смонтированный и эксплуатируемый комплекс водоподготовки, дополненный химической программой коррекции котловой воды, является необходимым условием долговечной и экономичной работы любого котлоагрегата.
В условиях эксплуатации энергетического оборудования на ТЭС или АЭС при организации водного режима необходимо создавать условия, при которых обеспечиваются минимальные значения скорости коррозии и снижение накипных отложений. Отложения могут образовываться из примесей, поступающих в воду теплоэнергетических установок от внешних и от внутренних источников.
Исходные данные
Исходной водой является вода Бассейны Ингула со следующим химическим составом:
-биогенные компоненты:
 =1,66 мг/л;;
=1,66 мг/л;;
NO2+=0,030 мг/л;
NO3+=0,11 мг/л;
Fe=0,11 мг/л;
P=0,060мг/л;
Si=5,9 мг/л;
-окисляемость:
БО=28,4 мгО2/л;
ПО=7,8мгО2/л;
-главные ионы:
HCO3-=294,7 мг/л;
SO42-=67,8 мг/л;
Cl-=55,7 мг/л;
Ca2+=92,3 мг/л;
Mg2+=15,9 мг/л;
Na++K+=38,5мг/л;
-Жо=5,9 мг-экв/л;
Блоки: 210МВт 6шт.
Таблица 1
|
| Общая концентрация | Электро провод ность, χ=Сλf мкСм/см | |||||||
| Молекуля рная масса "М" | Эквива лентная масса "Э" | Обозначения | Исх. концентрация | Скорректированная концентрация | |||||
| [H] мг/кг | [C]мг-экв/кг | [H] мг/кг | [C] мг-экв/кг | [N] моль/кг | % | ||||
| 40,08 | 20,04 | Ca2+ | 51,8 | 2,585 | 51,8 | 2,585 | 0,0013 | 0,005 | 110,67 |
| 24,03 | 12,01 | Mg2+ | 10,8 | 0,899 | 10,8 | 0,899 | 0,0004 | 0,001 | 40,8 |
| 23 | 23 | Na+ | 6,4 | 0,278 | 11,884 | 0,517 | 0,0005 | 0,001 | 23,84 |
| 1 | 1 | H+ | |||||||
| Сумма Kt | 3,762 | 4,001 | |||||||
| 17 | 17 | OH- | |||||||
| 61 | 61 | HCO3- | 199,7 | 3,274 | 199,7 | 3,274 | 0,0033 | 0,020 | 134,18 |
| 60 | 30 | CO32- | |||||||
| 96 | 48 | SO42- | 17,3 | 0,360 | 17,3 | 0,360 | 0,0002 | 0,002 | 20,75 |
| 35,46 | 35,46 | Cl- | 13,0 | 0,367 | 13,0 | 0,367 | 0,0004 | 0,001 | 25,78 |
| Сумма An | 4,001 | 4,001 | |||||||
| Обозначения | Значения | Обозначения и расчетные формулы | Значения | ||||||
| NH4-,мг/л | 0,60 | мольл | 0,006 | ||||||
| NO2-, мг/л | 0,02 | f’ | 0,921 | ||||||
| NO3-, мг/л | 0,11 | f“ | 0,720 | ||||||
| Fe, мг/л | 0,10 | CО2ф,моль/л | 0,00002 | ||||||
| P, мг/л | 0,04 | СО2р,моль/л | 0,00016 | ||||||
| Si, мг/л | 0,00 | рНф | 8,59 | ||||||
| БО, мгО2/л | 10,7 | рНр | 7,75 | ||||||
| ПО, мгО2/л | 4,00 | Ис | 0,84 | ||||||
| Жо, мг-экв/л | 3,7 | Жо-расчетное значение, мг-экв/л | 3,48 | ||||||
| СС,мг/л | СС, расчетное значение мг/л | 304,48 | |||||||
| Электропроводность,Сf,мкСмсм | 356,02 | ||||||||
Расчёт и корректировка исходного состава воды
Для начала найдём эквивалентные массы ионов:
Э = М/Z,
где М- молярная масса иона;
Z- заряд иона.
Э(Са2+) = 40,08/2 = 20,04 г-экв;
Эквиваленты остальных ионов считаются аналогично.
Расчет начинаем с анионного состава воды:
[С] = [Н]/Э,
где [Н]- концентрация иона, выраженная в мг/л,
Э- эквивалент иона.
С(HCO3-) =3,274мг-экв/кг;
С(SO42-) = 0,360мг-экв/кг;
C(Cl-) = 0,367 мг-экв/кг.
Σ An = 4,001мг-экв/кг.
Рассчитаем катионный состав воды:
С(Са2+) = 2,585мг-экв/кг;
С(Mg2+) = 0,899мг-экв/кг;
С(Na+) = 0,278мг-экв/кг;
Σ Kt = 3,762мг-экв/кг.
Правильность определения концентраций катионов и анионов, т.е. солей, образованных эквивалентным количеством ионов, проверяют на основании закона электронейтральности по уравнению:
Σ Kt=ΣAn.
При несоблюдении этого условия, следует скорректировать состав воды. Это достигается путём добавления натрия Na+.
Т.о. закон электронейтральности соблюдается.
Пересчитаем значения концентраций примесей в другие виды концентраций: [N]= [Н]/(М.1000), моль/л;
Пересчёт остальных концентраций осуществляется аналогично.
[С]= [Н]/104,%
Ионная сила раствора равна полусумме произведений молярных концентраций на квадраты их зарядов.
μ = 0,5 
Коэффициент активности – функция ионной силы раствора:
lg f' = -0.5Zi2 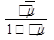 ,
,
f = 10  ,
,
Концентрация в природных водах недиссоциированных молекул Н2СО3 составляет обычно лишь доли процента от общего количества свободной углекислоты, под которым понимают сумму Н2СО3+ СО2.
Равновесное значение суммы Н2СО3+ СО2, моль/кг
Н2СО3+ СО2 =  ,
,
и рН – равновесное

Таблица 2
| Молекуляр- | Эквивалент- | Обозначения | Концентрации после коагуляции | Электропровод- | |||
| ная масса "М" | ная масса "Э" | [H] мг/кг | [C] мг-экв/кг | [N] моль/кг | % | ность, мкСм/см | |
| 40.08 | 20.04 | Ca2+ | 51.800 | 2.585 | 0.0013 | 0.005 | 109.97 |
| 24.03 | 12.01 | Mg2+ | 10.800 | 0.899 | 0.0004 | 0.001 | 40.54 |
| 23 | 23 | Na+ | 11.884 | 0.517 | 0.0005 | 0.001 | |
| 1 | 1 | H+ | |||||
| Сумма Kt | 4.001 | ||||||
| 17 | 17 | OH- | |||||
| 61 | 61 | HCO3- | 169.200 | 2.774 | 0.003 | 0.017 | 113.50 |
| 60 | 30 | CO32- | |||||
| 96 | 48 | SO42- | 41.300 | 0.860 | 0.000 | 0.000 | 49.23 |
| 35.46 | 35.46 | Cl- | 13.000 | 0.367 | 0.000 | 0.001 | 25.74 |
| Сумма An | 4.001 | ||||||
| Обозначения | Значения | Обозначения и расчетные формулы | Значения | ||||
| NH4+, мг/л | 0.300 | мольл | 0.006 | ||||
| NO2-, мг/л | 0.011 | f' | 0.920 | ||||
| NO3-, мг/л | 0.055 | f'' | 0.715 | ||||
| Fe, мг/л | 0.030 | СО2 моль/л | 0.0005 | ||||
| P, мг/л | 0.022 | pH | 7.153 | ||||
| Si, мг/л | 0.000 | Жо - расчетное значение, мг-экв/л | 3.484 | ||||
| БО, мгО2/л | 5.350 | CC, расчетное значение мг/л | 297.984 | ||||
| ПО, мгО2/л | 2.000 | Электропроводность, СfмкСмсм | 362.783 | ||||
| Dk,мг-экв/л | 0.500 | ||||||
Вывод: Величина pH имеет оптимальное значение, т.к. входит в интервал 5,5-7,5. Бикарбонатная щелочность увеличилась на дозу коагулянта, а содержание сульфатов увеличилось.
 2020-01-14
2020-01-14 419
419







