Содержание
| 1. Общие сведения о непредельных углеводородах |
| 2. Строение молекул непредельных углеводородов: |
| 2.1 Этилена |
| 2.2 Ацетилена |
| 3. Свойства непредельных углеводородов |
| 3.1 Этена |
| 3.2 Этина |
| 4. Номенклатура непредельных углеводородов |

Общие сведения о непредельных углеводородах.
Углеводороды, в молекулах которых не все свободные валентности атомов углерода насыщены атомами водорода, называют непредельными.
КЛАССИФИКАЦИЯ
Первая группа: Этиленовые имеют по международной номенклатуре два окончания – ИЛЕН, ЕН, поэтому их ещё называют алкенами.
Общая формула алк ен ов CnH2n
Гомологический ряд начинается с этилена (эт ен а) С2H4
Пропилена (проп ен) C3H6
Вторая группа: Ацетиленовые по международной номенклатуре имеют одно окончание – ИН, поэтому их называют – АЛК ИН АМИ.
Общая формула алк ин ов CnH2n-2
Гомологический ряд начинается с
АЦЕТИЛЕНА (эт ин а) C2H2
(проп ин) C3H4

2.1
СТРОЕНИЕ ЭТИЛЕНА
(C2H4)
В молекуле этилена наблюдается SP2 – гибридизация, т.е. смешиванию и выравниванию подвергается одно шарообразное S – облако и два гантелеобразных p – облака.
Таким образом, у каждого атома углерода образуется по три гибридных облака: по одному гибридному облаку они отдают на перекрывание между собой; по два гибридных облака они отдают на перекрывание s – облаками атомов водорода, В месте их перекрывания возникает СИГМА -связь.
У каждого атома углерода осталось по одному P – облаку, которые не подвергались гибридизации.
Такие облака перекрываются между собой, образуя π - связь, которая непрочна. Она перпендикулярна плоскости СИГМА – связь.

ВЫВОД:
В молекулах АЛКЕНОВ между атомами углерода имеется одна двойная связь, состоящая из прочной СИГМА – связи и непрочной π – связи.
2.2
Строение АЦЕТИЛЕНА – (C 2 H 2 )
В молекуле ацетилена наблюдается SP – гибридизация, следовательно у каждого атома углерода образовалась по два гибридных облака, по одному гибридному облаку они отдают на перекрывание друг с другом, а по второму гибридному облаку они отдают на перекрывание с S – облаками атома водорода. В месте их перекрывания возникает прочная сигма – связь.
У каждого атома углерода осталось по два P – облака, которые не подвергались гибридизации, перекрываясь между собой они образуют две непрочных π - связи, которые взаимно перпендикулярны.
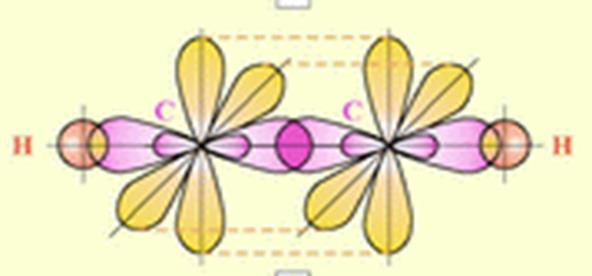
ВЫВОД:
В молекулах АЛКИНОВ между атомами углерода имеется одна тройная связь, состоящая из сигма– связи и из двух π - связей.
3.1
ХИМИЧЕСКИЕ СВОЙСТВА ЭТИЛЕНА
v ГОРЕНИЕ: (полное)
С2Н4+3O2→2CO2+2H2
доказывает принадлежность к органическим веществам
Ø ГИДРИРОВАНИЕ – это присоединение водорода к веществу
H2C=CH2+H2 à H3C-CH3
это уравнение доказывает непрочность π – связи
–––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––––
Ø Полимеризация – это присоединение одинаковых молекул в более крупные.
n H2C=CH2 à (-CH2-CH2-)n
РЕАКЦИЯ ИДЁТ С ОБРАЗОВАНИЕМ ПОЛИЭТИЛЕНА.

3.2
 2020-04-07
2020-04-07 205
205







