Электронная лекция
По дисциплине
« Химическая технология органических веществ. Часть 2 »
для студентов направления подготовки
18.03.01 – Химическая технология всех форм обучения
Подготовил: должность, степень
д.т.н., доц., проф. каф. ХПТ Сулимов А.В.
Дзержинск, 2019 год
ПРОЦЕССЫ АЛКИЛИРОВАНИЯ
Это введение алкильных групп в молекулы органических и некоторых неорганических соединений. Путем алкилирования получают большое число многотоннажных продуктов ОС: при алкилировании бензола получают этил-и изопропилбензол, которые в дальнейшем используются для получения стирола и a-метилстирола, производства фенола и ацетона методом ФАД, оксида пропилена и др.; при алкилировании трет-бутанабутенами получают изо-октан. Этим способом синтезируют также метил-трет-бутиловый эфир (добавка к моторному топливу), амины, меркаптаны, элементоорганические соединения и др.
Классификация реакций
Процессы алкилирования классифицируют по 2 принципам. По типу образующихся связей
1. Алкилирование по атому углерода. Основано на замещении атома водорода на алкильную группу (алкилирование парафинов и ароматических соединений (реакции Фриделя - Крафтса)).
2. Алкилирование по атому кислорода (метил-трет-бутиловый эфир, оксиэтилирование фенолов).
3. Алкилирование по атому азота. Это замещение атома водорода в аммиаке или аминах (синтез аминов, аммонолиз органических соединений).
4. Алкилирование по атому серы (получение меркаптанов).
5. Алкилирование по атомам других элементов (Al, Si, Pb) (получение металлорганических соединений типа А1(С2Н5)3, РЬ(С2Н5)4, диалкилдихлорсиланы и др.).
По строению алкильной группы, введенной в органическое соединение:
1. Циклоалкилирование.
2. Введение арильной группы.
3. Винилирование (с помощью ацетилена).
4. Алкилирование с помощью соединений, имеющих различные заместители (Cl) и функциональные группы (COONa, сульфогруппы и др.).
5. β-Оксиалкилирование - введение оксиалкильной группы с помощью оксида этилена или пропилена (получение этиленхлоргидрина, гликолей, оксиэтилированных спиртов, кислот, амидов и др.).
Алкилируюшие агенты и катализаторы
1. Алкены: этен, пропен и высшие. Имеют наибольшее значение из-за дешевизны. Используются для С-алкилирования парафинов и ароматических соединений. Не используются для N-алкилирования и мало для S- и О-алкилирования и получения металлорганических соединений. Механизм ионный с использованием протонных и апротонных кислот через промежуточное образование карбокатиона. Удлинение и разветвление УВ-цепи в алкене повышает его реакционную способность. В некоторых случаях механизм радикальный, инициирование - УФ излучением или термическое.
2. Хлорпроизводные с достаточно подвижным атомом хлора. Используются почти для всех видов алкилирования (С, S, О, N и Met-opг.). В основном используются тогда, когда затруднено или невозможно использование алкенов. Реакционная способность зависит от поляризации связи C-Cl и растет при удлинении алкильной группы. Реакции катализируются апротонными кислотами с промежуточным образованием карбокатиона. При алкилировании по атомам С, N, S процесс может идти без катализатора. При синтезе металлорганических соединений процесс идет по свободно-радикальному механизму (тетраэтилсвинец).
3. Спирты и простые эфиры. Спирты используются в том случае, когда они дешевле хлорпроизводных. Используется катализаторы кислотного типа.
Энергетическая характеристика процессов алкилирования
Все реакции алкилирования протекают с выделением тепла. Тепловой эффект зависит от природы алкилируюшего агента и типа разрывающейся связи в алкилируемом веществе. При использовании одного и того же агента тепловой эффект изменяется в ряду: Саром > Салиф > N > О. Если используются различные алкилирующие агенты, то:
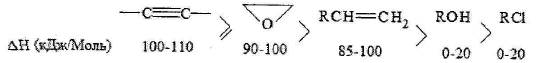
С-АЛКИЛИРОВАНИЕ
 2020-04-07
2020-04-07 259
259







