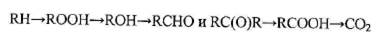
Все процессы окисления можно разделить на следующие группы:
1. Окисление без разрыва С-С связи
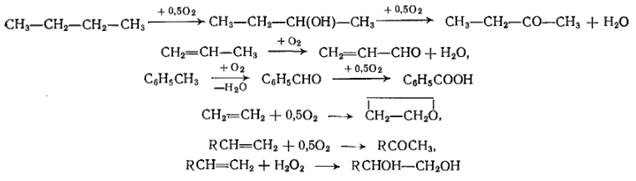
2. Окисление, протекающее с разрывом С-С связи (деструктивное окисление)
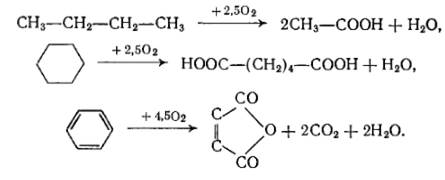
3. Процессы окислительного аммонолиза и окислительного сочетания
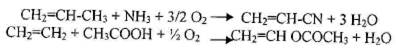
Окислительные агенты
1. Кислород и кислородсодержащие смеси: технический кислород, воздух, воздух обогащенный кислородом, искусственные смеси (кислород с азотом).
2. HNО3 - чаще всего 40-60 %, иногда меньше 20 % (для окисления алканов).
3. Гидропероксиды (С6Н5СН(СН3)ООН, С6Н5С(СН3)2ООН, (СН3)3СООН) пероксиды (Н2О2, (С6Н5СОО)2) и надкислоты (СН3СОООН, H2MoО5, H2WО5).
Энергетическая характеристика процессов окисления
Все процессы окисления являются необратимыми и экзотермичными. Тепловой эффект реакции зависит глубины окисления и вида окислительного агента.
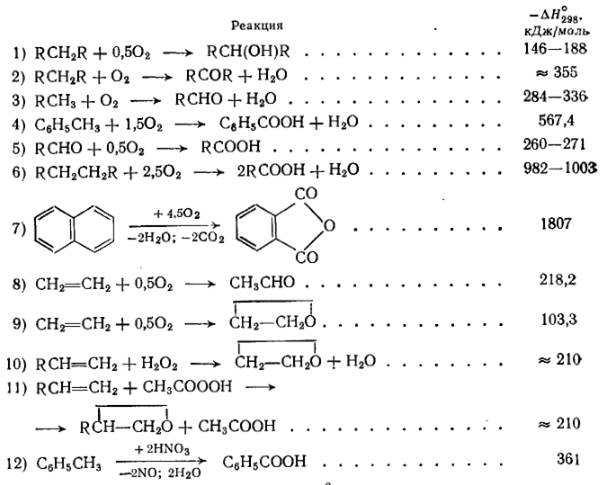
ПРОЦЕССЫ ГОМОГЕННОГО ОКИСЛЕНИЯ
ПО НАСЫЩЕННОМУ АТОМУ УГЛЕРОДА
С помощью этих процессов осуществляют окисление алканов, циклоалканов (нафтенов), боковых цепей ароматических соединений спиртов, альдегидов.
Чаще всего это гомогенно-каталитические реакции. Процесс может протекать в газовой фазе в присутствии HBr, HNО3, NO.
Жидкофазные реакции могут протекать без катализатора (автокаталитические реакции) и в присутствии катализаторов ими чаще всего являются соли металлов переменной валентности Со3+, Мn2+, Сu2+ и др.
Механизм гомогенного окисления
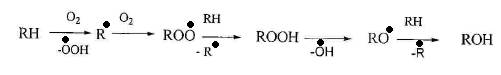
Гомогенное окисление в отсутствии катализатора протекает по радикально-цепному механизму. Процесс идет через стадию образования свободных радикалов и состоит из элементарных стадий инициирования, роста и обрыва цепи.
Спирты образуются через стадию получения гидропероксидов
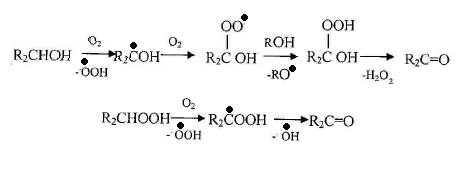
Кетоны получаются из вторичных спиртов и гидропероксидов
Альдегиды образуются
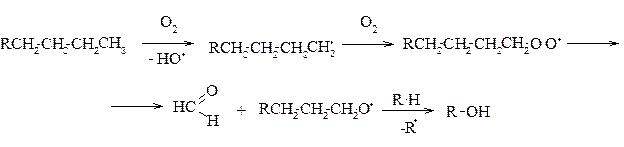
Карбоновые кислоты образуются окислением альдегидов или кетонов. происходящим с расщеплением цепи
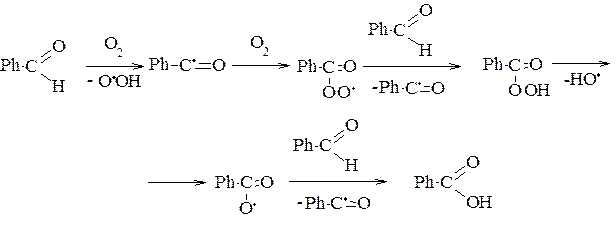
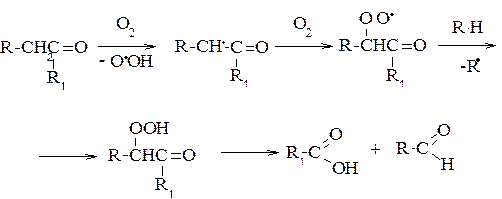
 2020-04-07
2020-04-07 197
197








