Равновесное состояние в сплавах соответствует минимальному значению свободной энергии. Это состояние достигается при достаточно длительном нагреве или при очень медленном охлаждении сплава.
В зависимости от температуры и содержания углерода, железоуглеродистые стали образуют следующие фазы и структурные составляющие:
1.Жидкая фаза – жидкий раствор углерода в железе.
2.Твердые фазы:
2.1. Феррит (Ф) - твёрдый раствор углерода в Fea. Имеет ОЦК решётку. При 20 0С нормальная растворимость 0,006%. Максимальная растворимость при 727°С составляет 0,02% С. Он обладает самой низкой прочностью из всех структурных составляющих, но очень пластичен и вязок.
sв=250МПа; НВ80; d=50%; y=80%.
2.2. Аустенит (А) – твердый раствор углерода в Feg. Имеет ГЦК – решётку. Предельная растворимость углерода в Feg при t=1147°С составляет 2,14%; он более твердый и прочный по сравнению с ферритом НВ160; d=40…50%, sв=?
2.3. Цементит (Ц) – химическое соединение Fe3C – карбид железа. В нём содержится 6,67% С. Цементит обладает высокой твёрдостью НВ³800, очень низкой пластичностью, хрупкостью.
В зависимости от условий существования различают цементит первичный, который образуется из жидкости при затвердевании расплава;
вторичный – образуется при распаде аустенита;
третичный – образуется при выделении углерода из феррита.
2.4. Перлит (П)- эвтектоидная механическая смесь феррита и цементита, содержащая 0,8%С; образуется при 727°С в результате распада аустенита в процессе его охлаждения. Он обладает высокой прочностью по сравнению с аустенитом и ферритом.
sв=800МПа; d=15%; НВ160…200.
2.5. Ледебурит (Л) – механическая смесь (эвтектика) аустенита и цементита, образуется из жидкого расплава при t=1147°С при содержании 4,3%С. Твёрдость НВ600…700, хрупок. Т.к. при t ниже 727°С аустенит превращается в перлит, то ледебурит при таких температурах (<727°С) состоит из перлита и цементита.
Сплавы с такой структурой обладают хорошими литейными свойствами.
Феррит, аустенит, цементит, перлит, ледебурит называются структурными составляющими железо – углеродистых сплавов.
Условные обозначения структур.

Диаграмма состояние железо –цементита
Fe – Fe3C
|
|
|
|
|







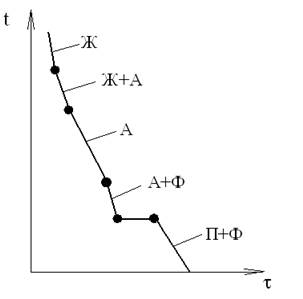
 Диаграмма состояния строится для характеристики структуры сплава в зависимости от состава и температуры. Она представляет собой графическое изображение состояния сплавов. Диаграмма состояния строится в координатах температура – состав. Построение проводят с помощью метода термического анализа. Сущность метода заключается в построении кривых охлаждения для сплавов с различной концентрацией углерода. Кривые охлаждения выражают критическую зависимость между изменением температуры (сплава) при охлаждении и временем, в течение которого эти изменения происходят. На кривой охлаждения будут точки перегибов, которые соответствуют изменениям состояния сплава при охлаждении.
Диаграмма состояния строится для характеристики структуры сплава в зависимости от состава и температуры. Она представляет собой графическое изображение состояния сплавов. Диаграмма состояния строится в координатах температура – состав. Построение проводят с помощью метода термического анализа. Сущность метода заключается в построении кривых охлаждения для сплавов с различной концентрацией углерода. Кривые охлаждения выражают критическую зависимость между изменением температуры (сплава) при охлаждении и временем, в течение которого эти изменения происходят. На кривой охлаждения будут точки перегибов, которые соответствуют изменениям состояния сплава при охлаждении.


|
|
Для получения диаграммы строится множество кривых охлаждения для сплавов с разной концентрацией углерода. Для этих сплавов получаем критические точки. Затем критические точки наносятся на общую диаграмму в координатах Т, 0С – состав. Критические точки соединяются, получаются линии диаграммы. Таким образом получили диаграмму железо-углерод. Чем больше сплавов с различной концентрацией углерода исследовано, тем точнее будет построена диаграмма состояния.

Характерные фазовые точки диаграммы.
т. А 1539°С – температура плавления чистого железа.
т. G 910°С – равновесная температура полиморфного превращения Fea®Feg
т. С 1147°С – эвтектическая или ледебуритная точка.
т. S 723°С – эвтектоидная или перлитная точка.
6,67% - точка содержания С в Fe3C (т.D)
4,3% - точка содержания С в ледебурите.
2,14% - точка максимальн. содержан. углерода в аустените при t=1147°С (т.E).
0,8% - точа максимального содержания углерода в перлите.
0,02% - макс. содержание углерода в феррите при t=723°С (т.P)
0,006% - макс. содержание углерода в феррите при t=20°С (т.Q)
Основные линии фазовых превращений.
1. Линия ACD – линия ликвидус. Выше неё сплав находится в жидком состоянии.
2. Линия ACF – линия солидус. Ниже нее сплав находится в твердом состоянии.
3. Линия ECF – ледебуритная эвтектическая линия.
4. линия PSK – перлитная эвтектоидная линия.
5. линия ES – линия переменной растворимости С в аустените.
6. линия Р 0,006 – линия переменной растворимости в феррите.
7. линия GS и линия GP – линии начала и конца превращения аустенита в феррит соответственно.
Основные фазовые области.
Различают однофазные и двухфазные области.
1. Однофазные области.
- жидкий раствор С в Fe
- аустенитная область (AESG)
-ферритная область (0,006 PG)
2. Двухфазные области.
- жидко – твёрдая (Ж+А; Ж+Ц)
- А+Ц (ECFKS) в этой области существуют равновесные структуры А+Ц; А+Л; Л; Л+Ц.
- Ф+Ц (PSK 6,67 0,006) в этой области существуют равновесные структуры Ф+Ц; Ф+П; П; П+Ц.
Механические свойства сплава определяются микроструктурой. Зная структуру сплава при комнатной температуре и свойства структурных составляющих, можно судить о свойствах сплава.
 2020-04-12
2020-04-12 494
494







