| Лекарственное вещество | Химическая структура | Описание |
| Glucose— глюкоза | 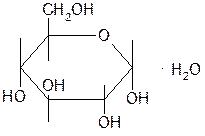 a-D-глюкопираноза a-D-глюкопираноза | Белый мелкокристаллический порошок без запаха, сладкого вкуса. Удельное вращение от +52 до +53° (10%-ный водный раствор) |
| Galactose D— D-галактоза (Левовист) | 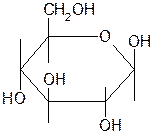 b-D-галактопираноза b-D-галактопираноза | Порошок или гранулы от белого до почти белого цвета. Т. пл. 167 °C. Удельное вращение +78 — +81° (водный раствор) |
| Saccharum lactis— сахар молочный (Лактоза) |  4-(b-D-галактопиранозидо)-D-глюкопираноза 4-(b-D-галактопиранозидо)-D-глюкопираноза | Белые кристаллы или белый кристаллический порошок без запаха, слабого сладкого вкуса. Удельное вращение от +52 до +53,5° (5%-ный водный раствор) |
| Saccharum— сахар (Сахароза) |  a-D-глюкопиранозидо-b-D-фруктофуранозид a-D-глюкопиранозидо-b-D-фруктофуранозид | Белые твердые куски мелкокристаллического строения без запаха, сладкого вкуса. Удельное вращение от +66,5 до +66,8° (10%-ный водный раствор) |
Лекарственные вещества углеводов сходны по физическим свойствам (табл. 29.1). Они представляют собой бесцветные или белые кристаллические вещества без запаха, сладкого вкуса. Легко растворимы в воде, очень мало или трудно растворимы в этаноле, практически нерастворимы в эфире и хлороформе.
Структура углеводов обусловливает особенности физических и химических свойств их растворов. От наличия нескольких асимметрических углеродных атомов в молекулах моносахаридов и дисахаридов зависят оптические свойства растворов. Эти свойства являются характерными константами для углеводов.
При окислении D-глюкозы образуется D-глюконовая кислота, а при восстановлении — сорбит.
Восстановительные свойства глюкозы, галактозы и лактозы связаны с наличием в молекуле полуацетального гидроксила. У сахарозы эти свойства проявляются в значительно меньшей степени, так как оба полуацетальных гидроксила находятся в связанном состоянии. При нагревании растворов дисахаридов в присутствии кислот происходит их гидролиз до моносахаридов. Сахароза гидролизуется с образованием глюкозы и фруктозы, а сахар молочный — до глюкозы и галактозы.
Для качественного и количественного анализа используют главным образом восстановительные свойства углеводов и физические свойства их растворов.
Подлинность глюкозы, галактозы и лактозы устанавливают, нагревая до кипения их растворы с реактивом Фелинга. При этом глюкоза образует кирпично-красный осадок оксида меди (I). Лактоза в тех же условиях дает желтый осадок, переходящий в буровато-красный. При действии на глюкозу, сахарозу и лактозу аммиачным раствором нитрата серебра выделяется черный осадок серебра. Сахароза, в отличие от глюкозы, галактозы и лактозы, не восстанавливает реактив Фелинга, т.к. является невосстанавливающим дисахаридом (олигосахаридом). Для испытания подлинности к раствору сахарозы (1:2) последовательно прибавляют растворы нитрата кобальта и гидроксида натрия. Появляется фиолетовое окрашивание.
Лактоза образует окрашенные продукты с аммиаком и алифатическими аминами. При нагревании на водяной бане (до 80 °С) раствора лактозы в присутствии аммиака возникает красное окрашивание. Аналогичная окраска появляется при нагревании до кипения раствора лактозы с метиламина гидроксидом и гидроксидом натрия.
Растворы глюкозы, галактозы и лактозы образуют с фенилгидразином выпадающие в осадок фенилгидразоны. При последующем нагревании на водяной бане получаются окрашенные в желтый цвет озазоны. Сахароза не дает положительной реакции с фенилгидразином. Озазоны имеют характерную температуру плавления. Глюкоза взаимодействует с тремя молекулами фенилгидразина:
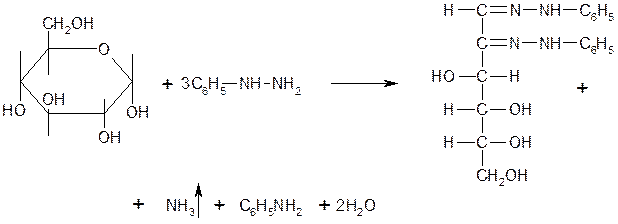
Под воздействием минеральных кислот или щавелевой кислоты моно- и дисахариды превращаются при нагревании в пробирке на пламени горелки в фурфурол или его производные (дисахариды вначале гидролизуются в моносахариды). Из глюкозы образуется оксиметилфурфурол, а из фруктозы — фурфурол:
 |
Фурфурол или оксиметилфурфурол, являясь летучими соединениями, взаимодействуют с анилином или прокаином, нанесенным на фильтровальную бумагу, которой накрывают пробирку. Вначале образуются основания Шиффа, имеющие светло-желтую окраску, а затем фурановый цикл раскрывается и получается полиметиновый краситель — производное оксиглютаконового альдегида (малиново-фиолетовое окрашивание):
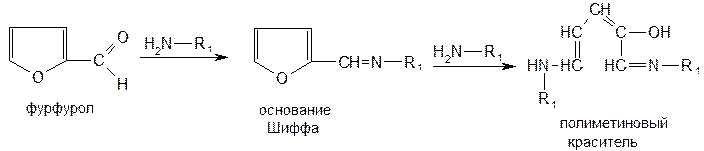
Углеводы образуют со спиртовым раствором a-нафтола и концентрированной серной кислотой соединения хиноидной структуры, окрашенные в красно-фиолетовый цвет. В основе реакции также лежит процесс образования фурфурола или оксиметилфурфурола, которые конденсируются с a-нафтолом в триарилметановое хиноидное соединение.
К этой же группе следует отнести цветные реакции, которые дают моно- и дисахариды с другими фенолами. При нагревании с несколькими кристаллами резорцина и разведенной хлороводородной кислотой молочный сахар образует желтое, а сахароза — розовое окрашивание. При смешении кристаллов глюкозы и тимола после добавления концентрированной серной кислоты появляется темно-красное окрашивание.
Окрашенные продукты конденсации получаются при взаимодействии моносахаридов (или гидролизованных дисахаридов) с раствором антрона в концентрированной серной кислоте:

Появляется зеленое окрашивание, постепенно переходящее в сине-зеленое.
Цветную реакцию с 0,5%-ным раствором хлорида трифенилтетразолия в присутствии раствора гидроксида натрия при нагревании дают глюкоза, галактоза и другие восстанавливающие сахара. Выпадает красный осадок трифенилформазана:

При добавлении раствора сульфата меди и подщелачивании глюкоза образует комплексное соединение фиолетово-синего цвета. Этой реакцией одновременно доказывается наличие как гидроксильных, так и альдегидной групп, восстанавливающих медь (II) до оксида меди (I) при стоянии. Присутствие гидроксильных групп можно также доказать реакцией ацетилирования (происходит образование пентаацетатов со стабильной температурой плавления).
Сахароза и высшие олигосахариды, содержащие её в молекуле, со щелочным раствором диазоурацила дают цветную реакцию (синее окрашивание).
Показателем качества углеводов является удельное вращение растворов, характеризующее их оптическую активность (см. табл. 29.1). Для установления удельного вращения глюкозу и галактозу предварительно сушат при 100–105 °C до постоянной массы.
Измерение угла вращения глюкозы и сахара молочного производят с помощью поляриметра после предварительного прибавления к испытуемому раствору двух капель раствора аммиака. При этом ускоряется процесс мутаротации. Он связан с установлением равновесия в образовании двух эпимеров: 64% a-D(+)-глюкозы и 36% b-D(+)-глюкозы. Это создает усредненное значение удельного вращения раствора глюкозы, равное +52,5° (ФС допускает 51,5–53,0°). Аналогично осуществляют процесс эпимеризации сахара молочного, D-галактозы, которая существует в виде a- и b-эпимеров, отличающихся значениями удельного вращения.
Под действием кислот или фермента инвертазы сахароза гидролизуется. Образующуюся смесь D-глюкозы и D-фруктозы называют инвертным сахаром. Эта смесь является левовращающей, так как оптические свойства ее складываются за счет удельного вращения глюкозы (+52,5°) и левовращающей фруктозы (-93°).
В условиях термической стерилизации растворов глюкозы для инъекций, вне зависимости от присутствия стабилизатора, происходит образование продуктов деструкции: дезоксигексазонов, органических кислот, формальдегида, 5-оксиметилфурфурола. В ФС включены способы определения этих веществ, основанные на использовании фотометрических методов.
Галактозу идентифицируют по НД методами ИК-спектроскопии и ВЭЖХ (по временам удерживания), сравнивая с растворами стандартных образцов.
Количественное определение глюкозы, галактозы, лактозы и сахарозы можно выполнить различными методами.
Содержание глюкозы определяют иодометрическим методом, основанном на окислении альдегидной группы щелочными растворами иода до образования натриевой соли глюконовой кислоты:
 |
+ I2 + 3NaOH ¾® CH2OH(CHOH)4COONa + 2NaI + 2H2O
Аналогичным методом можно определить галактозу и лактозу.
Один из титриметрических методов анализа моносахаридов и дисахаридов основан на использовании реактива Фелинга (2-3 кратный избыток). Его добавляют к навеске точно отмеренное количество, а затем иодометрически устанавливают остаток неизрасходованного на окисление катиона меди (II).
Методика основана на восстановлении углеводами меди (II) до меди (I) из тартратного комплекса:

Избыток реактива Фелинга, содержащего ионы меди (II), восстанавливают иодидом в кислой среде и выделившийся иод титруют тиосульфатом натрия:
2Cu2+ + 5I– ¾® 2CuI¯ + I3–
Поляриметрический метод определения сахаров основан на измерении угла вращения поляризованного света. Угол вращения a (в градусах), измеряемый на поляриметре, и удельное вращение  связаны между собой уравнением:
связаны между собой уравнением:  . Зная удельное вращение, длину трубки l и измерив угол вращения, можно вычислить массовую долю с (%) по формуле:
. Зная удельное вращение, длину трубки l и измерив угол вращения, можно вычислить массовую долю с (%) по формуле:
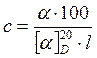
ГЖХ-метод определения глюкозы используют после превращения её в летучие соединения (ацетаты сорбита или нитрил глюконовой кислоты).
Хранят лекарственные препараты углеводов в хорошо укупоренной таре при комнатной температуре. Глюкоза в водных растворах при хранении окисляется, растворы сахарозы и молочного сахара постепенно гидролизуются с образованием моносахаридов. Следует также учитывать гигроскопичность сахаров.
Применяют глюкозу при различных заболеваниях сердца, печени, шоке, коллапсе в качестве источника легко усвояемого организмом питания, улучшающего функции различных органов. Основные пути метаболизма D-глюкозы — гликолиз и аэробное окисление до углекислоты, воды и АТФ. Назначают глюкозу внутрь (по 0,5–1,0 г), внутривенно до 20–50 мл 40%-ного раствора. Галактозу выпускают в виде гранулята по 0,3 г во флаконах вместимостью 20 мл. Его смешивают с 13,5 мл растворителя для получения микронизированной (менее 1 мкм) суспензии. В таком виде галактозу используют для визуализации полостей при УЗИ, эхокардиографии и др. Сахарозу и сахар молочный используют в фармацевтической практике в качестве наполнителей при приготовлении таблеток и порошков. Из сахарозы готовят сиропы, которые применяют как корригирующее средство.
В фармацевтической практике применяют также крахмал (Amylum). Он представляет собой смесь полисахаридов с общей формулой (C6H10O5) x. Молекула крахмала включает остатки a-D-глюкопиранозы, отличающиеся друг от друга степенью полимеризации и характером связей. Полисахариды, входящие в состав крахмала, можно разделить на две фракции: α- и β-амилозу (линейный полисахарид) и амилопектин (разветвлённый полисахарид). Получают крахмал из пшеницы, кукурузы, картофеля. Он представляет собой белый нежный порошок без запаха и вкуса, нерастворимый в холодной воде (в горячей образует клейстер), спирте, эфире. Крахмал используют в качестве наполнителя при изготовлении таблеток.
Практические вопросы
1. Количественное определение 5% раствора глюкозы
Глюкоза (Glucose)
Состав. Глюкозы - 50 г
Натрия хлорида - 0,26 г 0,1 М
Р-ра хлористоводородной к-ты - до рН 3,0-4,1
Воды для инъекций - до 1 л
Описание. Прозрачная бесцветная или слегка окрашенная жидкость.
Количественное определение. 1). Испытуемый препарат и стакан с водой помещают возле рефрактометра в сосуд с водой температуры 20°С на 30 мин. Через рефрактометр в течение 30 мин перед определением и в процессе определения пропускают воду очищенную с температурой 20°С. На призму рефрактометра наносят несколько капель воды и измеряют показатель преломления воды с точностью до 0,0002. Вытирают призму досуха, наносят на нее несколько капель испытуемого раствора и измеряют его показатель преломления, который определяют 3-4 раза, каждый раз беря новую порцию раствора. Для расчета используют среднее значение из всех определений. Содержание глюкозы в препарате в г (Х) рассчитывают по формуле:

n – показатель преломления препарата;
n0 – показатель преломления воды;
0,00142 – величина прироста показателя преломления при увеличении концентрации глюкозы на 1%.
Содержание С6Н12О6 (глюкозы) в 1 мл препарата должно быть
от 0,0485 до 0,0515 г – для 5% раствора.
2). Точно измеренный откалиброванной пипеткой объем препарата, содержащего от 2 до 5 г глюкозы (С6Н12О6), помещают в мерную колбу вместимостью 100 мл, добавляют р-р аммиака конц., доводят объем раствора водой до метки и перемешивают. Содержание глюкозы в препарате в г (Х) определяют поляриметрически и рассчитывают по формуле:

a – угол вращения испытуемого препарата, в градусах;
l – длина кюветы, дм;
52,7 – удельное вращение глюкозы, в градусах;
100 – объем раствора в мерной колбе, мл;
V – объем препарата, взятого на анализ, мл.
Содержание С6Н12О6 (глюкозы) в 1 мл препарата должно быть от 0,0485 до 0,0515 г – для 5% раствора.
Хранение. В сухом месте при температуре не выше 25°С.
2. Подлинность 5% раствора кислоты аскорбиновой


1). К 4-5 каплям р-ра + 2-3 капли р-ра нитрата серебра = образуется металлическое серебро в виде серого осадка
2). К 4-5 каплям р-ра + 1-2 капли р-ра хлорида окисного железа и р-ра феррицианида калия = синее окрашивание.
3). К 4-5 каплям р-ра + 1-2 капли 0,1 Н р-ра йода = р-р йода обесцвечивается
3. Подлинность фурацилина (таблетки 0,02 г)
Состав на одну таблетку:
Фурацилина 0,02 г
Натрия хлорида 0,8 г
Описание. Таблетки желтого или зеленовато-желтого цвета.
Подлинность. 1). 0,1 г порошка растертых таблеток растворяют в 10 мл воды + 0,5 мл разведенной азотистой кислоты + 0,5 мл раствора нитрата серебра = образуется белый творожистый осадок
2). 0,2 г порошка растертых таблеток дают реакции подлинности, характерные для фурацилина.
ЛП растворяют в смеси 5 мл воды и 5 мл раствора едкого натра = появляется оранжево-красное окрашивание. При нагревании полученного раствора выделяется аммиак, обнаруживаемый по запаху или по посинению влажной красной лакмусовой бумаги, внесенной в пары кипящей жидкости.


4. Количественное определение фурацилина
Furacilinum
Фурацилин
Nitrofuralum *
5-Нитрофурфурола семикарбазон

C6H6N404 M. в. 198,1
Описание. Желтый или зеленовато-желтый мелкокристаллический порошок без запаха, горького вкуса.
Растворимость. Очень мало растворим в воде, мало растворим в 95% спирте, практически нерастворим в эфире, растворим в щелочах.
Количественное определение. Около 0,1 г препарата (точная навеска) помещают в мерную колбу емкостью 500 мл, прибавляют 4 г хлорида натрия, 300 мл воды и растворяют при подогревании до 70-80° на водяной бане. Охлажденный раствор доводят водой до метки и перемешивают. К 5 мл 0,01 н. раствора йода, помещенным в колбу емкостью 50 мл, прибавляют ОД мл раствора едкого натра и 5 мл испытуемого раствора. Через 1-2 минуты к раствору прибавляют 2 мл разведенной серной кислоты и выделившийся йод титруют из микробюретки 0,01 н. раствором тиосульфата натрия (индикатор - крахмал). Параллельно проводят контрольный опыт.
I мл 0,01 н. раствора йода соответствует 0,0004954 г C6H6N404, которого в препарате должно быть не менее 97,5 %

хранение. Список Б. В хорошо укупоренных банках темного стекла, в прохладном, защищенном от света месте.
Высшая разовая доза внутрь 0,1 г. Высшая суточная доза внутрь 0,5 г.
Антибактериальное средство.
 2020-04-12
2020-04-12 958
958








