
При каждом соударении молекула, движущаяся перпендикулярно площадке, передаёт импульс 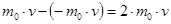 (аргументы – соответственно масса и скорость молекулы).
(аргументы – соответственно масса и скорость молекулы).
За время  площадки
площадки  достигнут только те молекулы, которые заключены в объёме цилиндра с основанием
достигнут только те молекулы, которые заключены в объёме цилиндра с основанием  и высотой
и высотой  . Число этих молекул равно
. Число этих молекул равно  .
.
Пространство трёхмерно, движение молекул происходит в прямом и противоположном направлениях.
Число ударов молекул о площадку  составит:
составит:  .
.
Импульс молекул:
 .
.
Давление газа:
 .
.
Средняя квадратичная скорость характеризует всю совокупность молекул газа: 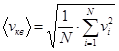 .
.
 – основное уравнение МКТ идеальных газов.
– основное уравнение МКТ идеальных газов.
Но 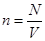 , где N – число молекул в объёме V.
, где N – число молекул в объёме V.
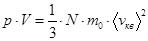
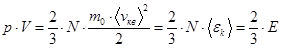
Здесь: Е – суммарная кинетическая энергия всех молекул.
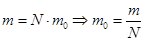
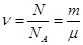


Какова связь между абсолютной температурой и среднеквадратичной скоростью молекул идеального газа?
С одной стороны,  .
.
С другой стороны,  .
.
Приравнивая, получаем:  .
.
Отсюда  .
.

Средняя кинетическая энергия поступательного движения одной молекулы идеального газа:



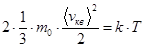

Отсюда 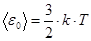 .
.
Среднее число столкновений и средняя длина свободного пробега
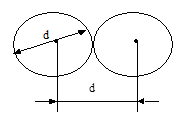
Средняя длина свободного пробега <l> – длина пути, проходимого молекулами между их последовательными столкновениями.
Эффективный диаметр молекул d – минимальное расстояние, на которое сближаются при столкновении центры двух молекул.
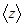 – среднее число столкновений, испытываемое одной молекулой газа за 1 секунду.
– среднее число столкновений, испытываемое одной молекулой газа за 1 секунду.


Здесь: n – концентрация молекул.

Здесь: 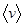 – средняя скорость молекул.
– средняя скорость молекул.
Среднее число столкновений:
 .
.
Расчёты показывают:
 .
.
Средняя длина свободного пробега:
 .
.
 .
.
 2020-04-12
2020-04-12 112
112








