Вариант 1
1. В результате нагревания давление газа в закрытом сосуде увеличилось в 4 раза. Во сколько раз изменилась средняя квадратичная скорость?
2. Сравнить давления кислорода и водорода при одинаковых концентрациях молекул и равных средних квадратичных скоростях их движения.
3. Во сколько раз изменится давление газа при уменьшении его объема в З раза? Средняя скорость движения молекул осталась неизменной.
Вариант 2
1. Каково давление газа, если средняя квадратичная скорость его молекул 500 м/с, а его плотность 1,35 кг/м3?
2. Какова средняя квадратичная скорость движения молекул газа, если, имея массу 6 кг, он занимает объем 5 м3 при давлении 200 кПа?
3. Найти концентрацию молекул кислорода, если при давлении 0,2 МПа средняя квадратичная скорость его молекул равна 700 м/с.
Контрольные вопросы
1. Записать краткий вывод формулы скорости молекул газа
2. Формулу давления газа
3. Что такое давление газа?
Практическое занятие№3.
Решение задач по теме 2.3 «Уравнение состояния идеального газа»
Цель: научиться применять уравнение Менделеева-Клапейрона, газовые законы.
Место проведения: учебная аудитория.
Средства обучения:
методические рекомендации к практическим работам;
линейка и карандаш;
калькулятор.
Виды самостоятельной работы:
Решение тренировочных заданий, работа с дополнительной литературой, с интернет-источниками, создание презентации, написание сообщения.
Краткая теория
Состояние некоторой массы газообразного вещества характеризуют зависимыми друг от друга физические величины, называемые параметрами состояния. К ним относятся объём V, давление р, температура T.
Всякое изменение состояния тела (системы тел) называется термодинамическим процессом.
Для изучения и сравнения различных термодинамических процессов их изображают графически.
Изопроцессами называют термодинамические процессы, протекающие в системе с неизменной массой при постоянном значении одного из параметров состояния системы.
Процесс, протекающий в газе, при котором объём остаётся постоянным, называется изохорным.
Закон Шарля: давление газа данной массы при постоянном объёме возрастает линейно с увеличением температуры:
m=const, V=const, T/p=const
Процесс, протекающий в газе, при котором давление остаётся постоянным, называется изобарным.
Закон Гей-Люссака: объем газа данной массы при постоянном давлении возрастает линейно с увеличением температуры:
m=const, p=const, T/V=const
Процесс, протекающий в газе, при котором температура остаётся постоянным, называется изотермическим.
Закон Бойля-Мариотта: давление газа данной массы при постоянной температуре убывает с увеличением объема:
m=const, T=const, pV=const
Для произвольной массы m газа с молярной массой M справедливо уравнение Менделеева-Клапейрона:
pV=mRT/M
R=8,31 — молярная (универсальная) газовая постоянная.
В другом виде уравнение состояния идеального газа можно записать в виде:
р=nkT,
где n — концентрация газа, то есть число частиц в единице объёма газа,
NA – постоянная Авогадро,
k – постоянная Больцмана.
Задания для аудиторной работы
1. Давление воздуха в автомобильной камере при температуре -130C было 160кПа. Каким стало давление, если в результате длительного движения автомобиля, если воздух в камере нагрелся до 370С?
2. Сосуд объёмом 27 л, содержащий газ при давлении 2·105 Па, соединяют с другим сосудом объёмом 3 л, из которого откачан воздух. Найдите давление газа в сосуде. Процесс изотермический.
3. Постройте график изотермического процесса в координатах (p,T), (p,V), (V,T).
4. Для изобарного нагревания газа, количество вещества которого 800 моль, на 500 К ему сообщили количество теплоты 9,4 МДж. Определить работу газа и изменение его внутренней энергии.
5. Какое количество тепла получил газ, если при этом он совершил работу А=2,103Дж, а его внутренняя энергия увеличилась на 600Дж.
Самостоятельная работа
Вариант 1
1. Газ сжат изотермически от объема 8 л до объема 6 л. Давление при этом возросло на 4 кПа. Каким было начальное давление?
2. Какая масса воздуха требуется для наполнения камеры в шине автомобиля, если ее объем 12 л? Камеру накачивают при температуре 27°С до давления 2,2·105 Па.
3. При температуре 5°С давление воздуха в баллоне равно 104 Па. При какой температуре давление в нем будет 2,6·104 Па?
4. До какой температуры нужно изобарически охладить некоторую массу газа с начальной температурой 37°С, чтобы объем газа уменьшился при этом на одну четверть?
5. Постройте график изобарного процесса в координатах (p,T), (p,V), (V,T).
Вариант 2
1. Баллон емкостью 100 л содержит 5,76 кг кислорода. При какой температуре возникает опасность взрыва, если баллон выдерживает давление до 5·105 Па?
2. В баллоне емкостью 100 л находится газ под давлением 4,9·105 Па. Какой объем займет газ при нормальном атмосферном давлении (1,01·105 Па)? Его температура не меняется.
3. Газ нагрет от 27° до 477° С при постоянном давлении. В результате его объем увеличился на 5 л. Определить первоначальный объем газа.
4. При температуре 52°С давление газа в баллоне равно 200кПа. При какой температуре его давление будет равным 250 кПа?
5. Постройте график изохорного процесса в координатах (p,T), (p,V), (V,T).
Контрольные вопросы
1. Запишите уравнение Клапейрона- Менделеева.
2. Сформулируйте закон Гей-Люссака.
3. Какой процесс называется изотермическим?
4. Сформулируйте первый и второй законы термодинамики.
5. Приведите примеры тепловых двигателей.
Практическое занятие№4.
Решение задач по теме 2.4«Основы термодинамики».
Цель: систематизировать знания по разделу «Основы термодинамики», научиться применять систему знаний на расчет величин, описывающих первый закон термодинамики и процессы, происходящие в тепловых двигателях; приобрести опыт решения задач по данной теме.
Место проведения: учебная аудитория.
Средства обучения:
методические рекомендации к практическим работам;
линейка и карандаш;
калькулятор.
Виды самостоятельной работы:
Решение тренировочных заданий, работа с дополнительной литературой, с интернет-источниками, создание презентации, написание сообщения.
Краткая теория
Внутренняя энергия идеального газа есть кинетическая энергия движения молекул
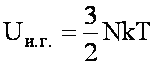
Внутренняя энергия идеального газа - это функция состояния. Она зависит только от состояния газа, а не от пути, по которому он приведён в данное состояние.
Первый закон термодинамики
Закон сохранения энергии в применении к тепловым явлениям называют первым законом термодинамики.
Количество теплоты, сообщенное системе, идет на изменение ее внутренней энергии и на
совершение работы над внешними телами.
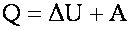
Изохорный процес:
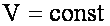
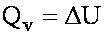
Изобарный процесс:
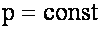
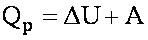
при этом:
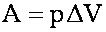
Изотермический процесс:
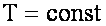
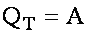
Адиабатный процесс.
Адиабатным называется процесс, при котором система не получает и не отдает энергию посредством теплопередачи, т.есть
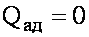
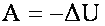
 2020-04-12
2020-04-12 274
274








