В акумуляторах при пропусканні крізь них електричного току від зовнішнього ланцюгу (заряд) йдуть хімічні реакції в електродах і розчинах, близькі до оборотних, і робота електричного току акумулюється у вигляді вільної енергії продуктів реакції. Заряджений акумулятор дає електричний струм при розряді, після чого знову можна його зарядити.
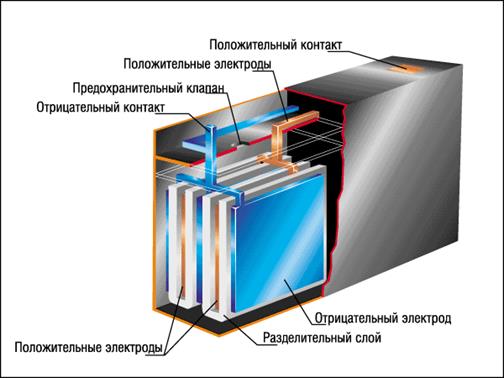
Малюнок 2. Загальна будова акумулятору
Найбільш широко використовують кислотний свинцевий, лужний кадмієво - нікелевий та лужний срібно - цинковий акумулятори.
СВИНЦЕВИЙ КИСЛОТНИЙ АКУМУЛЯТОР
Свинцевий кислотний акумулятор в зарядженому стані являє собою елемент:
(-) Pb, PbSO4(т) | H2SO4 (32-34%) | PbO2, Pb (+)
при роботі якого протікають наступні електродні реакції: на лівому катоді:

на правому електроді:

сумарна реакція процесу:

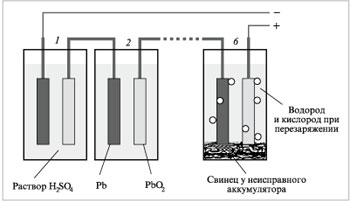 |
Малюнок 3. Схема дії свинцевого акумулятору
Ізобарний потенціал цієї реакції відображає зникнення твердих свинцю і його діоксину, виникнення твердого сульфату свинцю, а також зникнення 2 моль сірчаної кислоти і виникнення 2 моль води:

Так як хімічні потенціали твердих фаз постійні (при даних температурі і тиску), то

Ізобарний потенціал і ЕРС акумулятора залежать від концентрації сірчаної кислоти (точніше - від активності компонентів розчину).
У процесі розряду акумулятора концентрація сірчаної кислоти зменшується, а при зарядженні збільшується.
 2020-04-20
2020-04-20 117
117








