Вихідні дані:
· витрата парогазової суміші на вході в контактний апарат 263,651 кмоль/г;
· температура парогазової суміші на вході у контактний апарат 100-120°С;
· витрата формальдегідного газу 305,287 кмоль/г;
· температура формальдегідного газу на виході з апарата 700 - 750 °С.
Загальне рівняння теплового балансу безперервного процесу має такий вигляд:
1 + Q2 + Q3 = Q4 + Q5 + Q6 + Q7, (3.1)
деQ1 - тепловий потік вступник сировини;2 - тепловий ефект екзотермічних реакцій і фазових переходів;3 - тепловий потік, що надходить в апарат з теплоносієм;4 - фізична теплота продуктів реакцій;5 - тепловий ефект ендотермічних реакцій і фазових переходів;6 - теплота, що відводиться від апарата холодоагентом;7 - теплові втрати поверхнею апарата.
1,4 = ΣЗμ,i·Fi·t, (3.2)
деЗμ,i - молярна теплоємність,  ;i - молярний потік, кмоль/з;- температура речовин, °С.
;i - молярний потік, кмоль/з;- температура речовин, °С.
ΔНо973= ΔHо298 + ΔСр, 298-Т ·(Т - 298), (3.3)2,5 = ΣΔНо973·νi (3.4)
деνi - стехіометричний коефіцієнт;
ΔHi - энтальпія утворення, 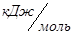 ;
;
Т - термодинамічна температура реакції, К.
Приймаємо Q3,6 = 0, тому що апарат є адіабатичним.
Втрати тепла Q7 приймаємо 3% від приходу тепла (Q1 + Q2).
З довідника [5] визначаємо коефіцієнти а, b, з і с', на підставі яких визначаємо теплоємності за рівняннями:
· для неорганічних речовин
 (3.5)
(3.5)
для органічних речовин
 (3.6)
(3.6)
Таблиця 3.2
Значення коефіцієнтів а, b, з, с' і теплоємкостей продуктів і реагентів
| O2 | CO | H2O | H2 | CO2 | N2 | СН2О(г) | СН3ОН(г) | ||
| а | 31,46 | 28,41 | 30 | 27,28 | 44,14 | 27,87 | 18,82 | 15,28 | |
| в*103 | 3,39 | 4,1 | 10,71 | 3,26 | 9,04 | 4,27 | 58,38 | 105,2 | |
| с*106 | 0 | 0 | 0 | 0 | 0 | 0 | -15,61 | -31,04 | |
| T, K | с' *10-5 | 3,77 | -0,46 | 0,33 | 0,5 | -8,54 | 0 | 0 | 0 |
| 110+273 | Cp T, K | 35,33 | 29,67 | 34,33 | 28,87 | 41,78 | 29,51 | 38,89 | 51,02 |
| 700+273 | Cp T, K | 35,16 | 32,35 | 40,46 | 30,50 | 52,03 | 32,02 | 60,85 | 88,25 |
Таким чином, тепло принесене з реагентами буде:

На підставі довідкових даних энтальпії утворення [5] і середньої теплоємності [5] визначаємо теплоти реакцій:
Таблиця 3.3
Визначення теплоти реакції (1.3)
| СН3ОН(г) | = СН2О(г) | + H2 | | |
| моль | 1 | 1 | 1 | 1 |

| -201,2 | -115,9 | 0 | 85,3 |
| Cp 298-1000 K | 69,22 | 49,5 | 28,77 | 9,05 |

Таблиця 3.4
Визначення теплоти реакції (1.4)
| СН3ОН(г) | + 0,5O2 | = СН2О(г) | + H2O | ||
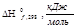 моль моль
| 1 | 0,5 | 1 | 1 | 0,5 |
| -201,2 | 0 | -115,9 | 241,81 | 156,51 | |
| Cp 298-1000 K | 69,22 | 32,43 | 49,5 | 37,07 | 1,135 |
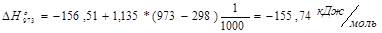
Таблиця 3.5
Визначення теплоти реакції (1.5)
| СН3ОН(г) | + 1,5O2 | = СO2 | + 2H2O | ||
| моль | 1 | 1,5 | 1 | 2 | 0,5 |
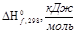
| -201,2 | 0 | -393,51 | -241,81 | -675,93 |
| Cp 298-1000 K | 69,22 | 32,43 | 47,15 | 37,07 | 3,425 |

Таблиця 3.6
Визначення теплоти реакції (1.6)
| СН3ОН(г) | = CO | + 2H2 | | |
| моль | 1 | 1 | 2 | 2 |

| -201,2 | -110,53 | 0 | 90,67 |
| Cp 298-1000 K | 69,22 | 30,92 | 28,77 | 19,24 |

Таким чином, теплота реакції буде

Разом з реагентами з реактора вийде тепла:

Прихід тепла:
1 + Q2 = 416,688 + 2744,678 = 3161,366 кВт.
Втрати тепла в навколишнє середовище складуть:7 = 0,03∙ 3161,366 = 94,841 кВт.
Витрата тепла:
4 + Q7 = 4,11·tx + 94,841.
Звідки температура формальдегідного газу на виході з реактора складе:

що відповідає прийнятому інтервалу температур.
 2020-04-20
2020-04-20 120
120








