ЛАБОРАТОРНАЯ РАБОТА № 8
Тема: «Изготовление моделей молекул органических веществ»
Смотреть по ссылке: https://www.youtube.com/watch?v=c78STfI-3EY
Цель: развитие навыков пространственного изображения молекул метана, этана, этена, этина, бензола
Оборудование: шаростержневые модели, транспортир. Учебное пособие Габриелян О.С. «Химия»
Задание на лабораторную работу:
1. Изготовление моделей молекул органических веществ СH4, C2H6, C2H4, C2H2, C6H6.
1.1 Изготовление шаростержневых моделей молекул.
При изготовлении шаростержневых моделей молекул необходимо знать угол связи и ее кратность. Угол химической связи измеряется траспортиром.
1.2 Заполните таблицу. Зарисуйте молекулы органических веществ.
| Название молекулы, тип связи, угол связи, тип гибридизации, пространственная форма молекулы. | Шаростержневая модель молекулы | Структурная формула | Молекулярная формула |
Основные теоретические положения
В предельных углеводородах (алканы) все углеродные атомы находятся в состоянии гибридизации sp3,
и образуют одинарные σ – связи. Угол связи составляет 109°28'. Форма молекул правильный тетраэдр.
В молекулах алкенов углеродные атомы находятся в состоянии гибридизации sр2, и образуют двойные связи σ и π – связи. Угол связи σ составляет 120°, а π – связь располагается перпендикулярно связи σ. Форма молекул правильный треугольник.
В молекулах алкинов углеродные атомы находятся в состоянии гибридизации sp, и образуют тройные связи одну σ и две π – связи. Угол связи σ составляет 180°, а две π – связи располагаются перпендикулярно друг друга. Форма молекул линейная (плоская).
В молекуле бензола C6H6 шесть атомов углерода связаны σ – связью. Угол связи составляет 120°. Состояние гибридизации sp2. В молекуле образуется 6 π – связь, которая принадлежит шести атомам углерода.
Для пространственного изображения молекул органических веществ важно знать, к какому классу веществ относится соединение, угол связи, форму молекул.
Например: Метан (СH4) относится к классу алканов. Атомы находятся в состоянии гибридизации sp3, значит угол связи 109°28', форма молекулы тетраэдр, между атомами одинарная σ – связь. Для построения молекулы шаростержневым способом нужно заготовить 4 шара из пластилина. Один шар (атом углерода) черного цвета, а три атома (водорода) одинакового размера белого цвета.
Контрольные вопросы:
1. Какие бывают органические соединения по строению углеводородного скелета?
2. Какие бывают органические соединения по наличию функциональных групп?
3. Какие вещества называются гомологами?
4. Какие бывают пространственные формы молекул органических веществ?
5. Какой процесс называется гибридизацией?
Дайте понятие σ и π связи?
Сделать вывод по работе:
УРОК № 55
Тема: Диены и каучуки
Базовые понятия и термины: алкадиены, кратные связи, структурные формулы, изомерия и номенклатура, изомерия по углеродному скелету и по положению кратных связей, межклассовая изомерия
Смотреть по ссылке: https://www.youtube.com/watch?v=jJ1aQ97CoAI
АЛКАДИЕНЫ – алифатически (ациклические), непредельные (ненасыщенные) углеводороды, с двумя двойными связями в цепи c о бщей формулой – CnH2n-2
Строение: Атомы углерода в молекуле бутадиена-1,3 находятся в sp2 - гибридном состоянии, что означает расположение этих атомов в одной плоскости и наличие у каждого из них одной p - орбитали, занятой одним электроном и расположенной перпендикулярно к упомянутой плоскости. p - орбитали всех атомов углерода перекрываются друг с другом, т.е. не только между первым и вторым, третьим и четвертым атомами, но и также между вторым и третьим. Отсюда видно, что связь между вторым и третьим атомами углерода не является простой σ - связью, а обладает некоторой плотностью p - электронов, т.е. слабым характером двойной связи. В молекуле отсутствуют в классическом понимании одинарные и двойные связи, а наблюдается делокализация p - электронов, т.е. равномерное распределение p - электронной плотности по всей молекуле с образованием единого p - электронного облака. Взаимодействие двух или нескольких соседних p - связей с образованием единого p - электронного облака, в результате чего происходит передача взаимовлияния атомов в этой системе, называется эффектом сопряжения. Таким образом, молекула бутадиена -1,3 характеризуется системой сопряженных двойных связей.
Такая особенность в строении диеновых углеводородов делает их способными присоединять различные реагенты не только к соседним углеродным атомам (1,2- присоединение), но и к двум концам сопряженной системы (1,4- присоединение) с образованием двойной связи между вторым и третьим углеродными атомами. Отметим, что очень часто продукт 1,4- присоединения является основным.
Запомнить! sp2 гибридизация; плоское-тригональное строение; связи σ и π (вращение относительно двойной С-С связи не возможно); угол HCH = 120 °
0,135 0,148 0,154
· Длина связи (-С = С – С = С – С – С -)
1. Классификация алкадиенов:
В зависимости от взаимного расположения двойных связей диены подразделяются на три типа:
1) углеводороды с кумулированными двойными связями, т.е. примыкающими к одному атому углерода. Например, пропадиен или аллен CH2=C=CH2
2) углеводороды с изолированными двойными связями, т.е. разделенными двумя и более простыми связями. Например, пентадиен -1,4 CH2=CH–CH2–CH=CH2
3) углеводороды с сопряженными двойными связями, т.е. разделенными одной простой связью. Например, бутадиен -1,3 или дивинил CH2=CH–CH=CH2
Наибольший интерес представляют углеводороды с сопряженными двойными связями.
2. Физические свойства: Бутадиен -1,3 – легко сжижающийся газ с неприятным запахом,
t°пл.= -108,9°C, t°кип.= - 4,5°C; растворяется в эфире, бензоле, не растворяется в воде.
2- Метилбутадиен -1,3 (изопрен) – летучая жидкость, t°пл.= -146°C, t°кип.= 34,1°C; растворяется в большинстве углеводородных растворителях, эфире, спирте, не растворяется в воде.
Изомерия сопряженных диенов
А) Структурная изомерия
1. Изомерия положения сопряженных двойных связей:

2. Изомерия углеродного скелета:
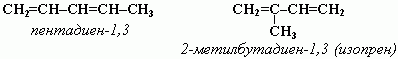
3. Межклассовая изомерия с алкинами и циклоалкенами.
Например, формуле С4Н6 соответствуют следующие соединения:
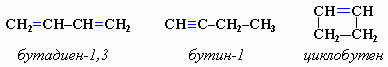
 2020-05-11
2020-05-11 408
408







