В основе получения сложных эфиров лежит реакция этерификации между карбоновой кислотой и спиртом. Реакция катализируется сильными кислотами.

Химические свойства.
- гидролиз
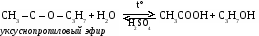
- горение
2CH3 – CО – O – СH3 + 7О2 → 6СО2 + 6 H2O
уксуснометиловый эфир
ЖИРЫ
Жирами называют сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот.

1. Животные жиры.
Животные жиры обычно твердые вещества (исключение - рыбий жир). Животные жиры используются в пищу и для получения твердого мыл.
2. Растительные жиры (масла).
Растительные жиры обычно жидкие (исключение - пальмовое масло). Растительные жиры используются в пищу, для получения маргарина, для получения олифы.
ТЕМА 17: УГЛЕВОДЫ.
- Моносахариды (глюкоза, фруктоза) - гидролизу не подвергаются.
- Дисахарида (сахароза, лактоза) – при гидролизе образуют две молекулы моносахаридов.
- Полисахарида (крахмал, целлюлоза) – при гидролизе образуют много молекул моносахаридов.
ГЛЮКОЗА
1. Физические свойства.
Твердое, белое f кристаллическое вещество, вкус сладкий, растворима в воде.
2. Строение молекулы.
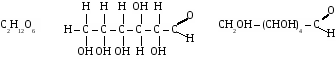
Глюкоза - альдегидоспирт.
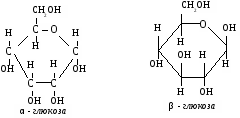
3. Химические свойства.
3.1 Глюкоза как многоатомный спирт реагирует без нагревания с гидроксидом меди, при этом образуется темно-синий раствор глюконата меди.
3.2 Реакции по альдегидной группе.
а) реакция «серебряного зеркала»
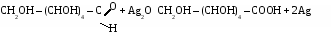
б) с гидроксидом меди

3. Брожение глюкозы.
а) спиртовое
С6Н12О6 → 2С2Н5ОН + 2СО2↑
б)молочнокислое
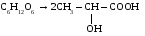
в) маслянокислое
С6Н12О6 → С3Н7СООН + 2СО2↑ + 2Н2↑
3.4 Полное окисление глюкозы.
С6Н12О6 + 6О2 → 2СО2 + 6Н2О
4. Получение и применение глюкозы.
(С6Н10О5)n + nН2О → nС6Н12О6
крахмал
Глюкоза используется в медицине, для получения этанола, при изготовлении зеркал.
ФРУКТОЗА .
Фруктоза является изомером глюкозы.

Фруктоза - кетоноспирт. Вместе с глюкозой входит в состав меда, имеет более сладкий вкус, чем глюкоза.
Задача. Сколько литров раствора этанола (плотность 0,79) с массовой долей С2Н5OH 95 %получится при спиртовом брожении 36 кг глюкозы?
САХАРОЗА.
Физические свойства.
Сахароза - твердое, белое, кристаллическое вещество, растворима в воде, вкус сладкий.
Сахароза в природе.
Сахароза входит в состав сока многих растении. Например, в соке сахарного тростника ее 14-16 %, а в соке сахарной свеклы 16-21 %.
Химические свойства.
1. Гидролиз.
С12Н22О11 + Н2О С6Н12О6 + С6Н12О6
глюкоза фруктоза
- Сахароза как многоатомный спирт реагирует с гидроксидом меди, при этом образуется: ярко-синий раствор сахарата меди.
- Сахароза реагирует с гидооксидом калция. Это свойство лежит в основе получения сахара их свеклы и его дальнейшей очистки.
С12Н22О11 + 2СА(ОН)2 → С12Н22О11 · 2СаО + Н2О
сахарат кальция
С12Н22О11 · 2СаО + 2СО2 → С12Н22О11 + 2 СаСО3↓
Применение сахарозы.
Сахароза используется в кондитерском производстве и для получения, этилового спирта.
Задача. Сколько тонн сахарной свеклы с массовой долей сахарозы 20%будет подвергнуто гидролизу для получения глюкозы массой 1т?
КРАХМАЛ.
Крахмал - природный полимер, макромолекулы которого состоит из остатков α-глюкозы и имеют в основном разветвленное строение.
Физические свойства.
Крахмал - твердое, белое, аморфное вещество без вкуса и запаха. Крахмал нерастворим в холодной воде, в горячей воле образует коллоидный раствор (клейстер).
Крахмал в природе.
Крахмал является одним из продуктов фотосинтеза и поэтому широко распространена в природе. Зерна риса содержат до 86 %крахмала, пшеницы до 75 %, кукурузы - до 72 %. Вклубнях картофеля содержание крахмала достигает 24 %.
Химические свойства.
1. Гидролиз
(С6Н10О5)n + nН2О nС6Н12О6
2. Качественная реакция на крахмал.
Реактивом на крахмал является раствор йода. Результат реакции - синее окрашивание.
Применение крахмала.
Крахмал является одним из важнейших компонентов пищи. Значительное количество крахмала перерабатывается на патоку, глюкозу, пищевой спирт, молочную кислоту. Крахмал используют в текстильной промышленности дляотделки тканей.
Задача. Какую массу кукурузных зерен надо взять для получения спирта массой 115 кг, с массовой долей C2H5OH 96 %, если массовая доля крахмала в кукурузных зернах составляет 70 %?
 2020-05-12
2020-05-12 178
178








