Понятие термодинамической энтропии, впервые введенное в 1865 году Клаузиусом, имеет ключевое значение для понимания основных положений термодинамики.
Рассмотрим обратимый круговой термодинамический процесс, представленный на рис. 3.12. Для этого процесса может быть записано равенство Клаузиуса (3.49) в виде
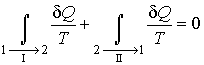 , ,
| (3.50) |
где первый интеграл берется по траектории 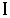 , а второй - соответственно по траектории
, а второй - соответственно по траектории  .
.
|
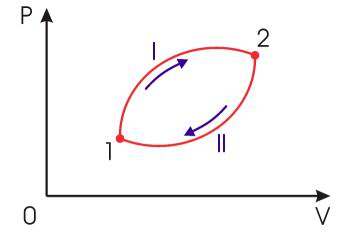
| Рис. 3.12. Обратимый круговой термодинамический процесс |
Изменение направления протекания процесса 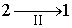 на противоположное
на противоположное 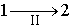 , что можно выполнить вследствие обратимости процесса
, что можно выполнить вследствие обратимости процесса 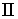 , приводит к замене знака перед вторым интегралом формулы (3.50). Выполнение этой замены и перенос второго интеграла в выражении (3.50) в правую часть дают
, приводит к замене знака перед вторым интегралом формулы (3.50). Выполнение этой замены и перенос второго интеграла в выражении (3.50) в правую часть дают
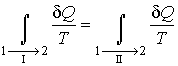 . .
| (3.51) |
Из полученного выражения следует, что для обратимых процессов интеграл 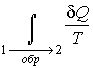 не зависит от конкретного вида траектории, по которой происходит процесс, а определяется только начальным и конечным равновесными состояниями термодинамической системы.
не зависит от конкретного вида траектории, по которой происходит процесс, а определяется только начальным и конечным равновесными состояниями термодинамической системы.
С аналогичной ситуацией мы уже встречались, когда в механике рассматривали определение работы консервативной силы. Независимость работы консервативной силы от формы траектории движения тела позволила ввести функцию, названную потенциальной энергией, которая зависит только от состояния механической системы и не зависит от того, как в это состояние система была переведена.
Из этой аналогии следует, что элементарное приведенное количество теплоты 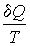 должно представлять собой полный дифференциал некоторой функции
должно представлять собой полный дифференциал некоторой функции 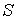 , зависящей только от состояния термодинамической системы, то есть:
, зависящей только от состояния термодинамической системы, то есть:
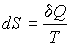 . .
| (3.52) |
Тогда интеграл 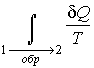 будет равен разности значений функции
будет равен разности значений функции 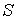 в равновесных состояниях 1 и 2:
в равновесных состояниях 1 и 2:
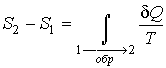 . .
| (3.53) |
Итак, величина 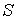 является функцией, зависящей только от равновесного состояния термодинамической системы. Она не зависит от конкретного вида термодинамического процесса, приведшего систему в указанное состояние. Эта функция была названа Клаузиусом термодинамической энтропией. Выражения (3.52) и (3.53) дают математическую формулировку сформулированного выше определения термодинамической энтропии.
является функцией, зависящей только от равновесного состояния термодинамической системы. Она не зависит от конкретного вида термодинамического процесса, приведшего систему в указанное состояние. Эта функция была названа Клаузиусом термодинамической энтропией. Выражения (3.52) и (3.53) дают математическую формулировку сформулированного выше определения термодинамической энтропии.
Из выражения (3.53) следует, что термодинамическая энтропия, так же как и потенциальная энергия, определяется с точностью до произвольной постоянной. Это связано с тем, что формула (3.53) не позволяет определить абсолютное значение термодинамической энтропии, а дает только разность энтропий для двух равновесных состояний, как суммарную приведенную теплоту в обратимом термодинамическом процессе, переводящим систему из одного состояния в другое.
Термодинамическая энтропия, введенная выше, применима для описания равновесного состояния термодинамической системы. Для нахождения энтропии 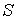 термодинамической системы, находящейся в квазиравновесном состоянии, при котором можно считать, что её отдельные части (подсистемы) находятся в состоянии равновесия, можно воспользоваться свойством аддитивности энтропии:
термодинамической системы, находящейся в квазиравновесном состоянии, при котором можно считать, что её отдельные части (подсистемы) находятся в состоянии равновесия, можно воспользоваться свойством аддитивности энтропии:
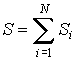 , ,
| (3.54) |
где: 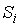 – энтропии подсистем,
– энтропии подсистем, 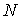 – число подсистем.
– число подсистем.
Следовательно, термодинамическая энтропия макроскопической системы, состоящей из находящихся в равновесии подсистем, равна сумме энтропий этих подсистем.
Свойство аддитивности энтропии позволяет описывать состояния макроскопической системы, не находящейся в равновесии, путем её разбиения на достаточно большое число подсистем, которые можно считать находящимися в состоянии локального равновесия. Такой подход дает возможность распространить результаты равновесной термодинамики на системы, находящиеся в неравновесном состоянии, но которые можно представить как состоящие из некоторого числа равновесных подсистем.
 2020-05-11
2020-05-11 158
158








