Для большинства бинарных смесей состав жидкости и равновесного пара различен. Однако некоторые вещества способны образовывать растворы, при испарении которых получается пар того же состава, что и исходная жидкая смесь. Такие смеси называются азеотропными (или азеотропами).
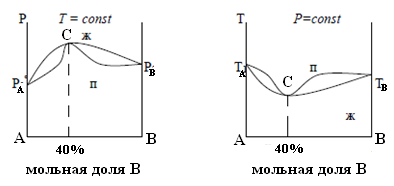
Диаграммы кипения систем, компоненты которых способны образовывать азеотроп, имеют важную особенность: верхняя и нижняя линии на них соприкасаются в некоторой точке «С» (рис.11), соответствующей составу азеотропной смеси. Для таких систем выполняется второй закон Коновалова: системам, для которых при равновесии состав жидкой и парообразной фаз одинаков (азеотропам), соответствуют точки максимума или минимума на кривых температура кипения – состав.
Другими словами верхняя и нижняя линии на диаграмме кипения могут соприкасаться только в точках экстремума (максимума или минимума) (рис.11).
|
| а) б) |
Рис.11 Диаграммы кипения систем, компоненты которых образуют азеотроп:
а) верхняя и нижняя линия соприкасаются в точке минимума (точка «С»), смесь, содержащая 40% В и 60% А является азеотропом;
б) линии соприкасаются в точке максимума (точка «С»), азеотропная смесь содержит 40% В и 60% А.
Важное свойство азеотропа – cостав азеотропных растворов при испарении не меняется, поэтому при данном постоянном давлении температура кипения азеотропа, так же как у индивидуального химического вещества, остается неизменной, а не повышается в процессе кипения, как у большинства растворов. Несмотря на то, что в этом случае свойства индивидуального химического соединения и азеотропа похожи, азеотропная смесь не является химическим соединением; доказательством этого служит тот факт, что при изменении внешнего давления состав ее меняется.
В соответствии с определением, азеотропные растворы следует считать однокомпонентными системами. Число степеней свободы (С), которыми обладает азеотропная смесь, находящаяся в равновесии со своим паром при постоянном давлении (Р = const), в соответствии с правилом фаз равно нулю:
С = К – Ф + n = 1 – 2 +1 = 0
Это означает, что двухфазная равновесная смесь азеотропного состава безвариантна (С = 0): существует только один набор параметров (Р, Т, NА), при которых она может существовать.
РАЗДЕЛЕНИЕ НЕОГРАНИЧЕННО СМЕШИВАЮЩИХСЯ ЖИДКОСТЕЙ
МЕТОДОМ ПЕРЕГОНКИ
Различием в составах жидкости и пара, полученного при ее кипении, пользуются для разделения смесей с помощью перегонки. Различают простую и фракционную перегонку. При простой перегонке (рис. 12) смесь нагревают и отводят получающийся пар в холодильник, где он конденсируется.

Рис. 12 Аппарат для простой перегонки
Простую перегонку применяют, если один из компонентов смеси (растворенное вещество В) не летуч или очень мало летуч по сравнению с другим компонентом (растворителем А).
Тогда конденсат в колбе-приемнике будет представлять собой чистую жидкость А, практическине содержащую примесей.
 2020-05-21
2020-05-21 591
591








