Относительная молекулярная масса.
Относительной молекулярной (атомной) массой вещества называется величина, равная отношению массы молекулы (атома) данного вещества к 1/12 массы атома углерода

Правило для расчёта относительной молекулярной массы:
Чтобы определить относительную молекулярную массу вещества, надо сложить атомные массы всех химических элементов, входящих в молекулу. Атомную массу элемента найдём в таблице Менделеева.
Например,
Мr (О2) = 16 ∙2 = 32
Мr (H2O) = 1∙2 + 16 = 18
Mr (H2SO4) = 1∙2 + 32 + 16∙4 = 98
2.Молярная масса вещества.
Молярная масса вещества – это масса 1 моля вещества
- обозначение, единица измерения в СИ: М 
- правило для определения М:
Чтобы определить молярную массу вещества, надо относительную молекулярную массу умножить на 10 -3
- формула для расчёта: М = Мr∙10 -3
Количество вещества
Количество вещества - это величина, характеризующая количество частиц в веществе.
- обозначение, единица измерения в СИ: ν 
1 моль – это такое количество вещества, в котором содержится столько же частиц (атомов или молекул), сколько частиц содержится в 0,012 кг углерода
Постоянная Авогадро
Исходя из определения 1 моля следует, что в 1 моле любого вещества содержится одинаковое количество частиц. Это число частиц называют числом Авогадро и обозначают NА
NА = 6∙1023 моль-1 - столько частиц (молекул, атомов) содержится в 1 моле любого вещества
5. Формулы для расчёта:
М = Мr∙10 -3 ν =  ν =
ν =  m0 =
m0 = 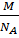
 2020-05-25
2020-05-25 187
187








