Практическая работа №4
Тема: Приготовление раствора соли с определенной массовой долей растворенного вещества
Цель: научиться готовить раствор соли с определенной массовой долей растворенного вещества, усовершенствовать навыки работы с лабораторным оборудованием.
Реактивы: калий хлорид, дистиллированная вода.
Оборудование: технохимические весы с гирьками, химический стакан, стеклянная палочка, шпатель.
Правила техники безопасности во время выполнения практической работы
Для насыпания твердых веществ следует пользоваться шпателем. Брать реактивы не защищенными руками брать нельзя. Перемешивать жидкость в стеклянном стакане следует перемешивать стеклянной палочкой. Во время работы со стеклом необходимо быть осторожными, особенно необходимо беречь глаза.
Задания
Приготовить 20 г раствора с массовой долей калий хлорида 0,05;
Порядок выполнения работы
1. Вычислить массы соли и воды, которые необходимо взять для приготовления определенного раствора. Массовая доля w – это отношение массы растворенного вещества к массе раствора. Выражается в процентах. m(E) – масса раствореного вещества

Определяем массу растворенного вещества (соли), которая необходима для приготовления раствора по формуле:
m (рас. в-ва)= w 
Находим массу воды. Посколько масса раствора состоит из массы растворенного вещества и массы воды, то масса воды равна разницы между массой растворенного вещества и массой раствора.
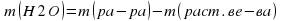
Вычисляем объем воды, так как взвешивать воду на весах нельзя. Плотность воды при температуре +25°С равна 1 г/см3.
V=  ;
; 
После вычисления массы соли и объема воды необходимо взвесить на весах необходимую массу соли. Для этого используют технохимические весы, которые дают результаты с точностью до 0,01 г.
2. Отмеряем с помощью мерного цилиндра необходимый объем дистиллированной воды. Наливаем в мерный цилиндр дистиллированную воду так, чтобы нижний уровень вещества касался выбранной отметки. Во время измерения цилиндр должен находиться в вертикальном положении, а глаза наблюдающего и значение объема на одном расстоянии.
3. Вливаем отмеренный объем воды в химический стакан с солью. Аккуратно перемешиваем содержимое стеклянной палочкой до полного растворения соли.
Выводы: взята соль с растворенным веществом. В данном растворе ______ является растворенным веществом, ______ – растворитель. Во время выполнения практической работы научились готовить раствор соли с определенной массовой долей растворенного вещества.
 2020-05-25
2020-05-25 102
102






