1 Приведите формулы двух непредельных кислот, одна из которых имеет цис-транс- изомеры, а другая нет.
2 Приведите формулы пяти углеводородов, не имеющих изомеров.
3 Из перечисленных соединений выберите для 4,4-диметилпентина-1: а) изомеры; б) гомологи. Диметилэтилнонан, ацетилен, гептадиен, этилпентадиен, этан, диметилоктин, этилен, гексан. Напишите формулы.
4 Среди горючих газов выделяют болотный, рудничный, водяной, коксовый. А какие газы носят названия «тощий» и «жирный»?
5 Из перечисленных соединений выберите для диметилпентена: а) изомеры; б) гомологи. Бутан, 4-метилнонан, гептен-2, триметилбутен, этилен, этилпентен, ацетилен, диметилбутен, бутадиен-1,3. Напишите формулы.
6 Из перечисленных соединений выберите для гексадиена: а) изомеры; б) гомологи. Циклогексан, ацетилен, гексин-2, диметилбутил, бутадиен-1,3, октадиен-1,3, октан, гептан-3, метилциклопентан. Напишите их формулы.
7 Приведите формулу любого соединения, описываемого формулой СпН2пО и существующего в форме цис- и транс- изомеров.
8 Напишите структурные формулы всех изомерных углеводородов состава С5Н12.
9 В 1812 г. на шахте близ Ньюкалса в Англии взрывом рудничного газа за несколько секунд было убито более ста шахтеров, а сотни остались калеками. Власти обратились к известному химику Гемфри Дэви. После многочисленных опытов, от которых у Дэви и его помощника Майкла Фарадея лица и руки покрылись ссадинами, было предложено защищать пламя горняцких ламп металлической сеткой. Что такое рудничный газ?
10 Приведите уравнение реакции крекинга гексадекана.
11 Рассчитайте, какой объем метана (н.у.) можно получить при сплавлении 10 г безводного ацетата натрия с избытком гидроксида натрия.
12 Напишите все изомеры соединений состава С8Н18, С4Н7Вr.
13 С помощью каких химических превращений, можно получить метан из хлорэтена? Напишите уравнения реакций и укажите условия их проведения.
14 Составьте уравнения реакций, с помощью которых можно осуществить превращения:
Этилен → … → этиловый эфир муравьиной кислоты
Метан → … → бензол → … → анилин
C2H5OC2H5 → C2H5OH → C2H5ONa →... → C2H5Cl
Ca → CaO → CaC2 → C2H2 → C2H4(OH)2
Карбид кальция → ацетилен →... → 1,2-дихлорэтан
15 Вычислите массу уксусной кислоты, которую можно получить из 44,8 л (н.у.) ацетилена, если потери на каждой стадии получения составляют в среднем 20%.
16 В лабораторной установке из 120 л ацетилена (н.у.) получили 60 г бензола. Найдите практический выход бензола.
17 Предложите схему получения 2,3-диметилбутана из 1-бромпропана.
18 Напишите уравнение реакции присоединения 1 моль брома к 1 моль бутадиена-1,3.
19 Рассчитайте выход продукта реакции (в % от теоретического), если при взаимодействии 5,6 л этилена (н.у.) с бромом получено 43,2 г 1,2-дибромэтана.
20 Напишите уравнение реакции присоединения бромоводорода к 2,3,3-трифторпентену-1.
21 Какое количество вещества хлора вступило в реакцию с 0,5 моль этилена, если при этом образовался 1 моль хлороводорода?
22 Болотный газ, пузырьками выделяющийся из тинистой пучины, пугал своим поведением. Если в месте выделения газ поджигали, то по болоту начинали блуждать огоньки. В 1777 г. итальянский физик Алесандро Вольта, взрывая смеси болотного газа с воздухом, пытался выяснить сущность происходящих процессов, но потерпел неудачу. Химики разных стран пытались получить болотный газ искусственным путем. Впервые это удалось сделать французскому химику Марселену Бертло только в 1856 г. путем пропускания смеси сероуглерода и сероводорода через трубку с раскаленной медной стружкой. Много позже болотный газ выделили, действуя водой на карбид алюминия или нагревая смесь ацетата и гидроксида натрия. Каков состав болотного газа?
23 Как, используя лишь один реактив, отличить друг от друга следующие вещества: а) этиленгликоль; б) ацетальдегид; в) этанол? Составьте уравнения соответствующих реакций.
24 Составьте уравнения реакций, с помощью которых можно осуществить превращения:
Метан → хлорметан → метанол → формальдегид
CH4 → ацетилен → CH3CH(O)
Ацетилен → уксусный альдегид → уксусная кислота →
→ уксусный ангидрид
Этилацетат → уксусная кислота → ацетат кальция
Метан → … → бутадиеновый каучук
25 Какой объем водорода (н.у.) получится при взаимодействии 2 моль металлического натрия с 96%-ным раствором этанола в воде (V = 100 мл, плотность ρ = 0,8 г/мл).
26 Напишите реакцию последовательного замещения водорода хлором в метане СН4, как пример цепной радикальной реакции. Смесь каких производных метана образуется при этом?
27 Чем отличаются спирты от фенолов? С какими веществами взаимодействуют спирты, и с какими - фенолы: металлический натрий; щелочь NaOH; уксусная кислота СН3СООН? Напишите соответствующие уравнения реакций.
28 Приведите формулу какого-либо сложного эфира, входящего в состав жиров. Напишите уравнение гидролиза (омыления) данного эфира раствором щелочи NaOH.
29 Какое практическое значение имеют вещества, получаемые при взаимодействии ацетилена: а) с водой, б) с хлористым водородом? Представьте уравнения реакций их получения.
30 Немецкий алхимик и врач Иоганн Бехер в 1669 г., прибавив к серной кислоте этиловый спирт, наблюдал, как раствор сильно вспенился, выделяя неизвестный газ, похожий на метан. Однако в отличие от метана новый газ горел коптящим пламенем и обладал слабым чесночным запахом. Бехер назвал новый газ «маслородный», так как его соединение с хлором С2Н4Сl2 представляло собой маслообразную жидкость, которую с 1795 г. называли «маслом голландских химиков». Какой газ открыл Бехер?
31 Могут ли быть изомеры у веществ, имеющих следующий состав: СОСl2, С2Н4Сl2? Дайте обоснованный ответ.
32 Можно ли обнаружить появление метана в шахте органолептическим путем, т.е. по запаху, вкусу и другим признакам? Почему?
33 В присутствии катализатора метан может частично окисляться с образованием оксида углерода (II). Что еще при этом образуется и может ли эта реакция иметь практическое значение?
34 Эффективным средством борьбы с огнем является тетрафтордибромэтан, в молекуле которого атомы галогенов распределены симметрично между атомами углерода. Напишите структурную формулу этого соединения и его возможных изомеров.
35 Дифтордихлорметан, применяющийся в качестве хладоносителя в холодильниках, получается действием фтороводорода на тетрахлорметан. Составьте уравнение этой реакции.
36 Через трубку с нагретым оксидом алюминия пропустили 100 г чистого этилового спирта. В результате было получено 33,6 л углеводорода. Сколько спирта (в % по массе) прореагировало при этом?
37 Ацетилен взрывается, разлагаясь на простые вещества. Является ли синтез ацетилена из простых веществ эндо- или экзотермической реакцией? Напишите уравнение реакции.
38 Карбид кальция, идущий для получения технического ацетилена, должен отвечать определенным требованиям: при действии воды на 1 кг его должно выделяться около 260 л. Каково содержание СаС2 (в % по массе) в таком карбиде?
39 Качество карбида кальция определяется литражом - объемом газа (н.у.), образующегося при действии воды на 1 кг карбида. Каков литраж химически чистого карбида?
40 Эффективным средством борьбы с филлоксерой является гексахлорбутадиен-1,3 - продукт замещения хлором всех атомов водорода молекулы бутадиена. Составьте формулу этого соединения.
41 Для протравливания семян зерновых культур применяется гексахлорбензол. Составьте его формулу и укажите, не прибегая к вычислениям, чего в нем больше по массе - углерода или хлора.
42 Охарактеризуйте понятие «мезомерный эффект». Какие условия должны выполняться для возникновения мезомерного эффекта? Назовите виды мезомерного эффекта.
43 Как физические и химические свойства предельных углеводородов зависят от строения и характера химических связей?
44 Напишите уравнения реакций алкилирования изобутана следующими алкенами: изобутиленом, пропиленом, бутеном-2. Укажите условия их проведения. Опишите механизм реакции алкилирования изобутана изобутиленом. Какое практическое применение находят полученные соединения?
45 Предложите схемы получения бутадиена-1,3 и изопрена из бутановой и пентановой фракций нефти соответственно. Напишите уравнения реакций; укажите условия их протекания.
46 Приведите схему и укажите условия проведения промышленного синтеза формальдегида.
47 В промышленности уксусную кислоту получают из ацетилена, окислением непредельных углеводородов и этилового спирта. Напишите уравнения реакций; укажите условия их протекания.
48 Какие вещества образуются при взаимодействии аминокислот с этиловым спиртом в присутствии соляной кислоты? Напишите уравнения реакции спирта с глицином и глутаминовой кислотой.
49 При действии азотистой кислоты на 0,4 г смеси, содержащей глицин, образовалось 44,8 мл азота (н.у.). какова массовая доля глицина в смеси?
50 При гидролизе 1 т древесины, содержащей 60% целлюлозы, получили 280 кг глюкозы. Напишите схему гидролиза целлюлозы; вычислите выход глюкозы в процентах.
 ТЕМА 11 ПОЛИМЕРЫ
ТЕМА 11 ПОЛИМЕРЫ
Наука о полимерах стала развиваться как самостоятельная область знания в 50-х гг. XX столетия, когда была выявлена роль полимеров в развитии технического прогресса и жизнедеятельности биологических объектов. Она тесно связана с физикой, физической, коллоидной и органической химией и может рассматриваться как одна из базовых основ современной молекулярной биологии, объектами изучения которой являются биополимеры.
Полимеры (греч. πολύ - много; μέρος - часть) - неорганические и органические, аморфные и кристаллические вещества, получаемые путём многократного повторения различных групп атомов, называемых «мономерными звеньями», соединённых в длинные макромолекулы химическими или координационными связями. Полимер - это высокомолекулярное соединение: количество мономерных звеньев в полимере (степень полимеризации) должно быть достаточно велико. Количество звеньев может считаться достаточным, чтобы отнести молекулу к полимерам, если при добавлении очередного мономерного звена молекулярные свойства не изменяются. Как правило, полимеры - вещества с молекулярной массой от нескольких тысяч до нескольких миллионов.
Если связь между макромолекулами осуществляется с помощью слабых сил Ван-Дер-Ваальса, они называются термопласты, если с помощью химических связей - реактопласты. К линейным полимерам относится, например, целлюлоза, к разветвленным, например, амилопектин. Есть полимеры со сложными пространственными трёхмерными структурами.
В строении полимера можно выделить мономерное звено - повторяющийся структурный фрагмент, включающий несколько атомов. Например, поливинилхлорид (—СН2—CHCl—)n, каучук натуральный и др. Высокомолекулярные соединения, молекулы которых содержат несколько типов повторяющихся группировок, называют сополимерами или гетерополимерами.
Полимер образуется из мономеров в результате реакций полимеризации или поликонденсации. К полимерам относятся многочисленные природные соединения: белки, нуклеиновые кислоты, полисахариды, каучук и другие органические вещества. В большинстве случаев понятие относят к органическим соединениям, однако существует и множество неорганических полимеров. Большое число полимеров получают синтетическим путём на основе простейших соединений элементов природного происхождения путём реакций полимеризации, поликонденсации и химических превращений. Названия полимеров образуются из названия мономера с приставкой поли-: поли этилен, поли пропилен, поли винилацетат и т. п.
Конфигурация цепи отражает химическую структуру макромолекулы. Под конфигурацией понимается взаимное расположение атомов вытянутой цепи, определяемое фиксированными значениями длин связей и валентных углов. Конфигурация цепи может быть изменена лишь путем разрыва химических связей, т. е. путем химической реакции. Вращение вокруг связи основной цепи не может ее изменить.
Конфигурация повторяющихся участков цепи определяется ориентацией мономерных звеньев вдоль цепи, пространственным расположением заместителей относительно плоскости полимерной цепи и геометрической (цис‑транс) изомерией в случае наличия ненасыщенных звеньев.
Пространственное расположение заместителей обычно представляется относительно плоскости, в которой расположена вытянутая цепь, представляющая собой зигзаг с углом между С—С связями равным 109° (sp3 гибридизация атомов углерода). Атомы углерода основной цепи, связанные с двумя различными заместителями R1 и R2, являются асимметрическими и могут находиться в L или D ‑форме. Если все асимметрические атомы основной цепи находятся только в L или D ‑форме, то все одинаковые заместители расположены по одну сторону относительно плоскости зигзага цепи. Такая макромолекула называется изотактической. Если L и D ‑формы чередуются, то заместители последовательно располагаются по обе стороны от плоскости зигзага основной цепи. В таком случае макромолекула называется синдиотактической:
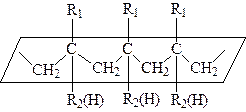
|
| изотактическая цепь |

|
| синдиотактическая цепь |
Изо- и синдиотактические макромолекулы называются стереорегулярными или тактическими. Макромолекулы с нерегулярным пространственным расположением заместителей называются стереонерегулярными или атактическими.
Как стереорегулярность цепи, так и цис - и транс -изомерия повторяющихся звеньев макромолекул оказывают существенное влияние на свойства полимера. Полимеры со стереорегулярными макромолекулами часто являются кристаллическими, тогда как полимеры со стереонерегулярными макромолекулами, как правило, аморфны. Пример влияния стереоизомерии звеньев на свойства молекул в полиизопрене: цис -изомер этого полимера является каучуком, транс -изомер, известный как гуттаперча, по своим свойствам напоминает пластик.
Изолированные макромолекулы (т.е. макромолекулы, находящиеся в растворе) совершают хаотическое макроброуновское движение, перемещаясь как целое. Вместе с этим, вследствие гибкости цепи отдельные ее части совершают микроброуновское движение независимо друг от друга. Такое движение может быть не только в растворе, но и в полимере, находящемся в высокоэластическом состоянии (характерном для каучуков). Вследствие микроброуновского движения макромолекулы принимают различные, постоянно меняющиеся формы, или конформации. Под конформацией понимается пространственное расположение атомов макромолекулы в данный момент времени, определяемое фиксированными значениями длин связей, валентных углов и углов вращения вокруг связей основной цепи. Одна конформация переходит в другую путем простого вращения вокруг связей основной цепи, поэтому макромолекула может реализовать последовательно множество конформаций.
К предельным случаям относятся конформации вытянутой цепи и плотного клубка (глобулы). Вытянутые конформации характерны для макромолекул жесткоцепных полимеров, у которых практически отсутствует вращение вокруг связей основной цепи. Условием возникновения глобул является сильное межмолекулярное взаимодействие между звеньями цепи за счет сил Ван-дер-Ваальса или водородных связей. Для макромолекул гибкоцепных полимеров характерны конформации, отвечающие форме рыхлого статистического клубка.
Полимеры применяются в машиностроении, текстильной промышленности, сельском хозяйстве и медицине, авто- и судостроении, авиастроении, в быту (текстильные и кожевенные изделия, посуда, краски, клей и лаки, украшения и другое). Все ткани живых организмов представляют собой высокомолекулярные соединения.
Особые механические свойства полимеров:
· эластичность – способность к высоким обратимым деформациям при относительно небольшой нагрузке (каучуки);
· малая хрупкость стеклообразных и кристаллических полимеров (пластмассы, органическое стекло);
· способность макромолекул к ориентации под действием направленного механического поля (используется при изготовлении волокон и плёнок).
Особенности растворов полимеров:
· высокая вязкость раствора при малой концентрации полимера;
· растворение полимера происходит через стадию набухания.
Особые химические свойства полимеров:
· способность резко изменять свои физико-механические свойства под действием малых количеств реагента (вулканизация каучука, дубление кож и т.п.).
По химическому составу полимеры делятся на органические, неорганические и элементорганические.
По составу атомов основной цепи полимеры бывают гомоцепные и гетероцепные. В гомоцепных полимерах цепь состоит из одинаковых атомов, а в гетероцепных – различных.
Органические полимеры содержат связи С–Н и функциональные группы, включающие атомы азота, кислорода, галогенов. Примером карбоцепных полимеров органических полимеров являются полиолефины и полимеры виниловых мономеров общей формулы [СН2 – СНR(Н)-]n, нитрильная и другая функциональная группа. Например, полиэфиры, полиамиды, полиуретаны, полиангидриды, полиацетали.
Неорганические полимеры не содержат связей C-H. Элементы I группы не образуют полимерных соединений; элементы II группы (бериллий, кадмий и т.д.) образуют гетероцепные полимеры. Окись магния, например, представляет собой полимер следующего строения:
…-Mg-O-Mg-O-Mg-O-…
Основная цепь большинства полимеров построена из элементов III и IV групп. Все элементы IV группы могут образовывать линейные цепи, аналогичные цепям полиэтилена. Элементы V группы обычно образуют только низкомолекулярные соединения, которые в определенных условиях могут превратиться в полимер. Так, белый фосфор, состоящий из молекул P4 в форме тетраэдра, при нагревании превращается в полимер. При нагревании белого фосфора до 5000С образуется красный фосфор. Это менее упорядоченная форма полимерного фосфора. Наиболее упорядоченной формой является черный фосфор. Это полимерное соединение, имеющее подобно графиту, слоистую решетку.
Очень склонны к образованию линейных гомоцепных полимерных соединений сера и селен (VI группы). Обычная ромбоэдрическая сера имеет циклические молекулы, содержащие восемь атомов серы. При нагревании в расплавленном состоянии происходит превращение цикла в линейный полимер:

Полимерное, гетероцепное строение имеет бороводород, который полимеризуется при комнатной температуре:

Типичным полимерным веществом является аморфная двуокись кремния:

Элементорганические полимеры содержат как органические, так и неорганические группы. Примером гетероцепного элементорганического полимера является полидиметилсилоксан: [—Si(CH3)2O—]n или полиорганофосфазены: [—PR2=N—]n.
Полимеры, макромолекулы которых состоят из повторяющихся звеньев одного типа, называются гомополимерами. В сополимерах макромолекулы содержат мономерные звенья нескольких типов. Ниже приведена классификация сополимеров, содержащих повторяющиеся звенья двух типов, условно обозначенные как А и В:
| Тип сополимера | Строение цепи |
| статистический | —А—А—В—А—В—В—А— |
| чередующийся | —А—В—А—В—А—В—А— |
| блок-сополимер | —ААААААААА—ВВВВВВВ— |
| привитой | 
|
По строению основной цепи макромолекулы подразделяются на линейные, двухтяжевые (две параллельные цепи, скрепленные различным образом), разветвленные и сшитые (сетчатые). Ниже приведена классификация макромолекул по строению основной цепи:
| Тип конфигурации | Строение цепи |
| Линейные макромолекулы | 
|
| Двухтяжевые макромолекулы лестничные спирополимеры | 
|

| |
| Разветвленные макромолекулы | |
| статистические | 
|
| гребнеобразные | 
|
| звездообразные | 
|
| Сшитые (сетчатые) | |
| в плоскости (паркетные) | 
|
| в пространстве | 
|
Полимеры подразделяют по полярности (влияющей на растворимость в различных жидкостях). Полярность звеньев полимера определяется наличием в их составе диполей – молекул с разобщенным распределением положительных и отрицательных зарядов. Полимеры, звенья которых обладают значительной полярностью, называют гидрофильными или полярными. Полимеры с неполярными звеньями - неполярными или гидрофобными. В неполярных звеньях дипольные моменты связей атомов взаимно компенсируются. Полимеры, содержащие как полярные, так и неполярные звенья, называются амфифильными. Гомополимеры, каждое звено которых содержит как полярные, так и неполярные крупные группы, предложено называть амфифильными гомополимерами.
По отношению к нагреву полимеры подразделяют на термопластичные и термореактивные. Термопластичные полимеры (полиэтилен, полипропилен, полистирол) при нагреве размягчаются, даже плавятся, а при охлаждении затвердевают. Этот процесс обратим. Термореактивные полимеры при нагреве подвергаются необратимому химическому разрушению без плавления. Молекулы термореактивных полимеров имеют нелинейную структуру, полученную путём сшивки (например, вулканизация) цепных полимерных молекул. Упругие свойства термореактивных полимеров выше, чем у термопластов, однако термореактивные полимеры практически не обладают текучестью, вследствие чего имеют более низкое напряжение разрушения.
Для полимеров существует два основных типа температур перехода: температура плавления (Tпл.) и температура стеклования (Tст.). Температура плавления – это температура плавления кристаллической фазы полимера. Температурой стеклования называется температура, при которой аморфные области полимера приобретают свойства, характерные для стеклообразного состояния: хрупкость, жесткость и прочность. Различия между двумя указанными тепловыми переходами можно легко понять, рассматривая изменения, происходящие в различном жидком полимере при его охлаждении. С уменьшением температуры уменьшается поступательная, вращательная и колебательная энергия в молекуле полимера. Когда суммарная энергия молекулы уменьшится до величины, при которой поступательная и вращательная энергия уже практически отсутствуют, становится возможной кристаллизация полимера. При этом если удовлетворяются определенные требования симметрии, то молекулы могут принимать упорядоченное расположение и, таким образом, реализуется кристаллизация. Температура, при которой происходит этот процесс, и есть Tпл. . Однако не у всех полимеров создаются необходимые условия для кристаллизации. Если требования симметрии не удовлетворяются, то кристаллизация не протекает, но, по мере дальнейшего снижения температуры, энергия молекулы продолжает уменьшаться. При достижении Tст. сегментальное движение полимерных цепей прекращается из-за сильного ослабления вращения связей.
Возможность реализации одного или обоих тепловых переходов зависит от его морфологии. Полностью аморфные полимеры характеризуются только Tст., тогда как полимеры полностью кристаллические имеют только Tпл.. Большинство же полимеров при Tпл. подвергаются кристаллизации лишь частично, подобные полукристаллические полимеры характеризуются температурой плавления и температурой стеклования. Тепловые переходы легко измерить по изменению таких свойств, как удельный объем, теплоемкость. На рисунке 6 приведена зависимость удельного объема от температуры для полностью аморфного и полностью кристаллического полимера (сплошные линии). Соответствующая кривая для полукристаллического полимера состоит из кривой для кристаллического полимера и пунктирной линии, соответствующей переходной области в стеклообразное состояние (рисунок 6).

Рисунок 6 – Определение температуры стеклования и температуры плавления полимера по изменению его удельного объема
Температуры плавления и стеклования влияют на механические свойства полимера и определяют температурный интервал его использования. На тот и другой термический переход, как правило, одинаково влияют молекулярная симметрия, структурная жесткость и межмолекулярное взаимодействие. Сильное межмолекулярное взаимодействие (из‑за высокой полярности или водородных связей) приводит к сильным кристаллизационным силам, что обуславливает высокие Tпл .. Сильное межмолекулярное взаимодействие понижает также подвижность цепей аморфного полимера, в результате и Tст. имеют высокие значения.
На величину Tс т . и Tпл. также сильно влияет молекулярная симметрия полимерных цепей. Полимеры, структурно асимметричные (например, поливинилхлорид и полипропилен), имеют более высокие Tст. и Tпл., чем их симметричные аналоги (поливинилиденхлорид и полиизобутилен). Асимметричные цепи являются более полярными, и поэтому могут упаковываться плотнее, обеспечивая более сильное межмолекулярное взаимодействие.
На основе полимеров получают волокна, пленки, резины, лаки, клеи, пластмассы и композиционные материалы (композиты).
Волокна – высокомолекулярные вещества природного происхождения или синтезируемые химическим путем, имеющие линейное строение, сформированные в виде нитей. Классификация волокон представлена на рисунке 7.
| Целлюлоза | Белки | |||

|
| 
| 
| |
 Льняное Льняное
| Хлопковое |  Шерстяное Шерстяное
| Шелковое | |
 
|
|  
| 
| |
| Растительного происхождения | Животного происхождения | |||
|
|
| |||
| Природные | ||||
|
| ||||
| ВОЛОКНА | ||||
|
| ||||
| Химические | ||||
|
|
| |||
|
|
| |||
|
| ||||
|
|
| |||
|
|
| |||
Рисунок 7 – Классификация волокон
Искусственные волокна получают на основе природного сырья (целлюлозы). Синтетические волокна получают из синтезируемых низкомолекулярных веществ.
Искусственные волокна хуже, чем хлопковые, впитывают влагу. смоченные водой волокна на 40% имеют меньшую прочность, но они не подвержены воздействию бактерий и плесневых грибов. Ацетатные волокна и обычная вискоза идут на изготовление тканей. Из прочного вискозного волокна изготавливают искусственную кожу (кирзу), корд для автомобильных покрышек.
Синтетические волокна высокопрочные, эластичные, не мнутся, устойчивы к истиранию, не подвержены разрушительному воздействию некоторых насекомых, плесени. Но плохо впитывают влагу, способны накапливать статическое электричество при трении, их нельзя гладить горячим утюгом. К синтетическим волокнам относят полиэфирные волокна, например, лавсан, и полиамидные волокна, например, капрон, найлон. Полиэфирные волокна идут на изготовление тканей для одежды, технических тканей (транспортные ленты, пожарные рукава, канаты), тюля, бутылок для напитков. Полиамидные волокна идут на производство автомобильного корда, парашютных тканей, обивочных тканей, ковров, искусственного меха, одежды.
Каучук. Натуральный каучук получают из сока бразильской гевеи. Этот сок (латекс) представляет собой молокоподобную жидкость, в которой каучук суспензирован в виде микроскопических глобул. Есть и другое дерево, сок которого содержит сорт каучука, называемого гуттаперчей. Молекулы гуттаперчи и каучука построены из одних и тех же звеньев (изопрена), отличающихся только структурой:
Н2С=С-СН=СН2
|
СН3
изопрен (цис -2-метилбутадиен-1,3)
Наиболее важным из синтетических каучуков до Второй мировой войны был буна‑каучук: повторяющимся звеном в цепи является бутадиен. Поиски различных каучуконосов велись в Африке, и хотя ряд нужных растений был найден, их потенциальный вклад оказался незначительным. Положение облегчилось с появлением американского синтетического каучука, известного как GR—S. Он имеет более сложное строение, чем немецкий буна‑каучук, является сополимером, состоящим из двух компонентов - бутадиена и стирола. Этот каучук оказался по ряду свойств хуже натурального, его недостаточная «липкость», или адгезия, создавали трудности, например, при производстве автомобильных шин, однако эта проблема была решена после разработки технологий смешения его с небольшими количествами натурального каучука. Другим важным синтетическим каучуком является бутил‑каучук‑полимер, получаемый из изобутилена. Одно из особенностей бутил‑каучука в том, что воздух диффундирует через него значительное медленнее, чем сквозь натуральный каучук, поэтому бутил‑каучук ценен, как основа при производстве автомобильных камер. Однако, по сравнению с натуральным каучуком, эластические свойства его значительно хуже. В противоположность волокнам каучуки, как правило, некристалличны; их молекулы расположены неупорядоченно. Структура каучуков, во многом подобная структуре жидкости, называется аморфной. Именно этой рыхлой структуре (в отличие от плотно упакованной регулярной структуры кристалла) каучуки обязаны своей мягкостью и гибкостью.
Биологические полимеры. Строение тела животных и человека дает многочисленные примеры использования природой физических и химических свойств разнообразных полимерных материалов. Так, мышцы построены из связок волокон, представляющих собой одну из форм белка. Главной функцией мышц является перевод химической энергии, полученной из мышц в механическую работу. Мышцы обладают и некоторыми эластическими свойствами каучуков, т.е. выполняют функции прокладки, амортизирующей удары и защищающей внутренние организмы от повреждений.
Природные органические полимеры образуются в растительных и животных организмах. Это полисахариды, белки и нуклеиновые кислоты, из которых в значительной степени состоят тела растений и животных. Считается, что решающим этапом в возникновении жизни на Земле явилось образование из простых органических молекул более сложных – высокомолекулярных.
Человек давно использует природные полимерные материалы в своей жизни. Это кожа, меха, шерсть, шёлк, хлопок и т. п., используемые для изготовления одежды, различные связующие (цемент, известь, глина), образующие при соответствующей обработке трёхмерные полимерные тела, широко используемые как строительные материалы. Однако промышленное производство цепных полимеров началось в начале XX в., хотя предпосылки для этого появились ранее.
Клей и желатин получают из другого фибриллярного белка - коллагена, основного белка кожи.
Кристаллические полимеры. Третий и во многих отношениях наиболее интересный класс синтетических полимеров - это кристаллические полимеры. В отличие от обычных кристаллических твердых тел полимеры не полностью кристалличны, а содержат множество очень мелких кристаллов, существующих наряду с остальным разупорядоченным или аморфным веществом. В неориентированном состоянии они не имеют аналогов в природе, и их свойства отличаются от свойств веществ, которые были известны до сих пор.
Одним из наиболее широко и многосторонне используемых кристаллических полимеров является полиэтилен. Он обладает превосходными изоляционными свойствами, а также легкостью и эластичностью. Полиэтилен имеет один недостаток —OH плавится при сравнительно низкой температуре (110°С-130°С)
Еще один важный кристаллический полимер - это нейлон, который имеет отличные волокнообразующие свойства, однако он может быть также получен в виде блоков для производства изделий методом литья под давлением. Tпл. (нейлона) равна 265°С.
Заменой всех атомов водорода в полиэтилене на атом фтора получают кристаллический полимер с интересными свойствами. Этот полимер, известный под названием политетрафторэтилена (тефлон), имеет еще более высокую температуру плавления, а именно 360°С.
Стекла и смолы. Стекла выделяются среди других полимеров своей высокой оптической прозрачностью и хрупкостью. Их прозрачность - результат того, что они некристалличны. Как и у каучуков, расположение молекул в стеклах беспорядочно, структура стекол разупорядочена или аморфна. Отдельные кристаллы таких веществ, как кварц или алмаз, могут иметь прозрачность стекла, но, как правило, кристаллические вещества не существуют в форме отдельных единичных кристаллов, а представляют собой агломераты большого числа мелких кристаллов. Подобно тому, как белый цвет снега обусловлен отражением света от многочисленных поверхностей мельчайших кристаллов льда, так и молочно‑белая окраска кристаллических полимеров (полиэтилена), объясняется рассеянием света от межкристаллических поверхностей. В аморфной структуре стекла, как и в жидкости, нет разрывов непрерывности или различий в геометрическом расположении молекул по всему образцу и, следовательно, нет граней, от которых свет мог бы рассеиваться или отражаться. Следовательно, поскольку сами молекулы не поглощают свет, такие материалы прозрачны. Среди хорошо известных стеклообразных полимеров можно назвать полистирол, плексиглас, поливинилхлорид. Прозрачность не является самым важным свойством стекла, и значительное число полимеров, обладающих механическими свойствами, аналогичными свойствам стекол, не имеют прозрачности плексигласа или полистирола - эти вещества называют синтетическими смолами. Из первых смол, получивших промышленное применение, был бакелит, получивший название в честь его открывателя Бакеленда. Бакелит - это темно-окрашенный материал, широко использовался (и используется до сих пор) как электроизолятор.
В заключение данной темы, хотелось бы сказать еще об одном полимере – это полимочевина. Полимочевина – синтетический эластичный полимер (эластомер), содержащий в главной цепи фрагменты мочевины –NH-CO-NH-. Полимочевинные защитные покрытия характеризуются рядом высоких физико-химических показателей, выделяющих их среди других пленкообразующих полимеров, таких как: эпоксид, полиэфир, акрил, каучук. Это достигается благодаря сочетанию конечных потребительских свойств поликарбамида (высокая твердость, гибкость, эластичность, сопротивление на разрыв и истирание, прочность при растяжении, сжатие, с превосходной адгезией, химическая и биологическая стойкость, с самой низкой паропроницаемостью) и технологическими свойствами (высокая скорость полимеризации, отсутствие температурной зависимости, зависимости к влаге). Именно благодаря этим свойствам полимочевина признана защитным покрытием XXI века.
 2020-05-25
2020-05-25 616
616






 Искусственные
Искусственные
 Синтетические
Синтетические Вискозное
Вискозное Полиэфирные
Полиэфирные






