Контрольная работа № 4 по теме: Химическая связь. Строение вещества. Растворы
8 класс.
1 Вариант
Часть 1
1.Из формул веществ, формулы которых приведены ниже, выпишите формулы веществ, молекулы которых образованы ковалентной полярной связью
а)N:::N в) K+ (:Вr:)-
б)H:Cl: Г) H:O:H
2. К какому виду связи относится связь между натрием и хлором в хлориде натрия?
а) ионная б) металлическая в)ковалентная полярная
3.В какой молекуле степень окисления равна нулю, а валентность – трём?
1) О2 2)BF3 3) N2 4) CO
4. Укажите номера оксидов, где связь ионная:
1) оксид хлора (V) 4)оксид цезия
2)оксид серы (VI) 5) оксид фосфора
3)оксид азота (II) 6)оксид кальция
5. В каком веществе образуется металлическая связь?
1) NH 2)CO2 3) H2O 4) Fe
6. В какой из данных молекул полярность связи выше?
1) HCl 2)HJ 3) HBr 4) HF
7. Какое из веществ имеет ионный тип связи:
1) NaCl 2)HCl 3) Cl2 4) HClO
8. В какой молекуле полярность связи выше?
1) NH3 2)AlH3 3)PH3 4)SвH3
9.В какой молекуле степень окисления элемента равна нулю, а валентность –единице?
1) Cl2 2)HCl 3) N2 4)NH3
10. Расположите номера соединний в порядке возрастания полярности с кислородом:
1) NaO2 2)B2O3 3) CO2 4) H2O 5) NO
Часть 2
Рассчитайте массы воды и соли, необходимые для приготовления 200 г раствора с массовой долей
соли 25%.
Класс. Химия.
Тема. Контрольная работа №4.
Выполнить контрольную работу чисто, аккуратно, разборчиво.
Вариант 1
Часть I Один правильный ответ
1. К реакциям разложения относиться реакция
1). CaO+SiO2=CaSiO3; 2). 2HgO=2Hg+O2
3). Zn+2HCI=ZnCI2+H2; 4). 2Mg+O2=2MgO
2. Вещества, формулы которых — Al2O3 и K2SO4, являются соответственно
1) оснόвным оксидом и кислотой 2) амфотерным гидроксидом и солью
3) амфотерным оксидом и солью 4) оснόвным оксидом и основанием
3. Оксиду N(III) соответствует кислота
1) HNO2 2) HNO3 3) NH3 4) NaNO2
4. Верны ли суждения о способах разделения смесей?
А. Выпаривание относят к физическим способам разделения смесей.
Б. Разделение смеси воды и этанола возможно способом фильтрования.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
5. В реакции 3CuO + 2NH3 =3Cu+ N2+ 3H2O
изменение степени окисления окислителя соответствует схеме
1) +2 → 0; 2) −3 → 0; 3) −2 → 0; 4) 0 → +2
Часть 2
6. Выбрать 2 правильных ответа.
Для метилового спирта верны следующие утверждения
1) является газообразным веществом (н. у.)
2) в молекуле имеется гидроксильная группа
3) ядовит
4) плохо растворим в воде
5) вступает в реакцию с серебром
7. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
| ВЕЩЕСТВА | РЕАКТИВ | |
| А) NaNO3 и Ca(NO3)2 Б) FeCl2 и FeCl3 В) H2SO4 и HNO3 | 1) BaCl2 2) Na2CO3 3) HCl 4) NaOH |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Часть 3.
8 Вычислить объём водорода (н.у.), образовавшийся при взаимодействии 26 г цинка с раствором серной кислоты.
Класс
Тема. Контрольная работа №2.
Выполнить контрольную работу чисто, аккуратно, разборчиво.
В тетрадях пишите: Седьмое мая. Контрольная работа №2.
1 Вариант.
Часть 1
1. Из предложенного перечня выберите два вещества, с которыми реагирует этиламин.
1) пропан; 2) хлорметан; 3) водород; 4) гидроксид натрия; 5) соляная кислота.
2. Из предложенного перечня выберите два вещества, с которыми может взаимодействовать аминобутановая кислота:
1) оксид кремния; 2) бутанол; 3) бутадиен-1,3; 4) гидроксид калия; 5) сульфат кальция.
3. Продуктами полного сгорания аминов являются.
1) углекислый газ, вода и оксид азота(II); 2) оксид углерода (II), вода и аммиак; 3) углекислый газ, вода и азот; 4) углекислый газ, водород и азот.
4. Из предложенного перечня веществ выберите два вещества, которые подвергаются гидролизу.
1) глюкоза; 2) сахароза; 3) фруктоза; 4) рибоза; 5) крахмал.
5. Составьте уравнения реакций, соответствующих схеме превращений: крахмал 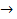 глюкоза
глюкоза 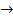 этиловый спирт. Укажите условия протекания реакций, назовите органические вещества.
этиловый спирт. Укажите условия протекания реакций, назовите органические вещества.
Часть 2
6. Дан перечень свойств вещества:
1) дисахарид; 2) слаще глюкозы; 3) окрашивается иодом в фиолетовый цвет; 4) дает реакцию «серебряного зеркала»; 5) реагирует с гидроксидом меди (II); 6) при гидролизе образует глюкозу и фруктозу.
7. Рассчитайте массу этанола, который можно получить при брожении 45г глюкозы.
Часть 3
8. Рассчитайте массу кислоты, полученной при нагревании 55г 40%-го раствора этаналя с избытком гидроксида меди (II)
10 класс. Факультатив. Тема. Уравнения с параметрами.
Выполнить. Подобрать 1 уравнение с параметром и решить.
 2020-06-08
2020-06-08 162
162







