Для пищевых целей уксусную кислоту получают уксуснокислым брожением жидкостей, содержащих спирт (вино, пиво): фермент
СН3 – СН2 – ОН + О2 → СН3СООH + Н2О
воздух
Синтетическую уксусную кислоту для химических целей получают различными методами:
а) окислением ацетальдегида:
СН3 – СОН + [О] → СН3СООH
б) синтезом метанола и оксида углерода (II)
t, кат.
СН3 – ОН + СО → СН3СООH
ДОМАШНЕЕ ЗАДАНИЕ
Ответьте на вопросы (письменно):
1. Выучить тривиальные названия низших карбоновых кислот.
2. Напишите уравнения реакций следующих превращений:
этан → хлорэтан → этанол → этаналь → уксусная кислота
3. По желанию: подготовить презентацию о важнейших представителях ненасыщенных монокарбоновых кислот или составить кроссворд по изученной теме.
. УРОК № 66, 67
Тема: Сложные эфиры и жиры
Смотреть по ссылке: https://www.youtube.com/watch?v=kZX6bV9c1JQ
Сложные эфиры можно рассматривать как производные кислот, у которых атом водорода в карбоксильной группе замещен на углеводородный радикал:

Номенклатура.
Сложные эфиры называют по кислотам и спиртам, остатки которых участвуют в их образовании, например Н—СО—О—СН3 — метилформиат, или метиловый эфир муравьиной кислоты; этилацетат, или этиловый эфир уксусной кислоты.
Способы получения.
1. Взаимодействие спиртов и кислот (реакция этерификации):

2. Взаимодействие хлорангидридов кислот и спиртов (или алкоголятов щелочных металлов):

Физические свойства.
Сложные эфиры низших кислот и спиртов — жидкости легче воды, с приятным запахом. В воде растворимы только сложные эфиры с наименьшим числом атомов углерода. В спирте и диэтиловом эфире сложные эфиры растворимы хорошо.
Химические свойства.
1. Гидролиз сложных эфиров — важнейшая реакция этой группы веществ. Гидролиз под действием воды — обратимая реакция. Для смещения равновесия вправо используются щелочи:
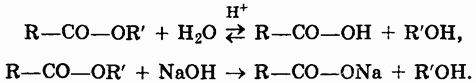
2. Восстановление сложных эфиров водородом приводит к образованию двух спиртов:

3. Под действием аммиака сложные эфиры превращаются в амиды кислот:

Жиры. Жиры представляют собой смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая формула жиров:
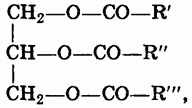
где R — радикалы высших жирных кислот.
Наиболее часто в состав жиров входят предельные кислоты пальмитиновая и стеариновая и непредельные кислоты олеиновая (С17Н33COOH) СН3(СН2)7СН=СН(СН2)7СООН и линолевая (С17Н31COOH) CH3(CH2)3-(CH2CH=CH)2(CH2)7COOH/
Получение жиров.
В настоящее время практическое значение имеет лишь получение жиров из природных источников животного или растительного происхождения.
Физические свойства.
Жиры, образованные предельными кислотами, — твердые вещества, а непредельными — жидкие. Все очень плохо растворимы в воде, хорошо растворимы в диэтиловом эфире.
Химические свойства.
1. Гидролиз, или омыление жиров происходит под действием воды (обратимо) или щелочей (необратимо):

При щелочном гидролизе образуются соли высших жирных кислот, называемые мылами.
2. Гидрогенизацией жиров называется процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жиров. При этом остатки непредельных кислот переходят в остатки предельных кислот, и жиры из жидких превращаются в твердые.
Из важнейших пищевых веществ — белков, жиров и углеводов — жиры обладают наибольшим запасом энергии.
 2020-06-08
2020-06-08 270
270








