03.06.20
Запишите в рабочую тетрадь тему: сначала формулы для расчетов в задаче, затем алгоритм решения задачи.
Списывая алгоритм, старайтесь разобраться в решении, поскольку на следующем занятии каждый будет решать задачу самостоятельно.
3. Решите вторую задачу по алгоритму. Отправьте выполненные задания в комментарии к уроку до 11-30.
Фамилия Имя обучающегося
Тема. Решение расчетных задач на определение молекулярной формулы органического вещества по массовым долям элементов и относительной плотности
Относительная плотность первого газа по второму (D):
D2 =  ,
,
где Mr1 и Mr2- относительные молекулярные массы газа 1 и газа 2.
D2 - относительная плотность первого газа по второму.
Например:
а)Если в условии задачи дана относительная плотность газа по кислороду (DO2), то, исходя из формулы относительной плотности:
|
| |
 =
= 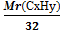 , находим относительную молекулярную массу вещества
, находим относительную молекулярную массу вещества
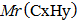 по формуле:
по формуле: 
б) Если в условии задачи дана относительная плотность газа по водороду (DН2), то,
находим относительную молекулярную массу вещества  по формуле:
по формуле:
|
в) Если в условии задачи дана относительная плотность газа по азоту (DN2), то,
находим относительную молекулярную массу вещества  по формуле:
по формуле:
|
 г) Если в условии задачи дана относительная плотность газа по воздуху (Dвозд), то,
г) Если в условии задачи дана относительная плотность газа по воздуху (Dвозд), то,
|
 по формуле:
по формуле: 
Массовые доли элементов в веществе (ω)
|
1. Для вещества  формула массовой доли углерода:
формула массовой доли углерода:
Из этой формулы выражаем индекс x (количество атомов С):
|
2. Индекс y (количество атомов H) находим по формуле:
|
3. Индекс z (количество атомов O) находим по формуле:
|
где ω -массовые доли элементов: углерода, водорода и кислорода (%)
 - относительная молекулярная масса вещества
- относительная молекулярная масса вещества 
Относительная атомная масса углерода Ar (C) = 12
Относительная атомная масса водорода Ar (Н) = 1
Относительная атомная масса кислорода Ar (О) = 16
Алгоритм решения задачи
Задача 1. Определите молекулярную формулу вещества, если плотность паров его по водороду равна 23, а массовые доли элементов соответственно равны: углерода - 52,18%, водорода - 13,04%, кислорода - 34,78%.

 2020-06-29
2020-06-29 278
278 = DO2 ∙ 32
= DO2 ∙ 32
 = DН2 · 2
= DН2 · 2

 =
= 
 =
= 
 =
= 







