- Какие элементы входят в состав белков? Среднее содержание химических элементов в белках
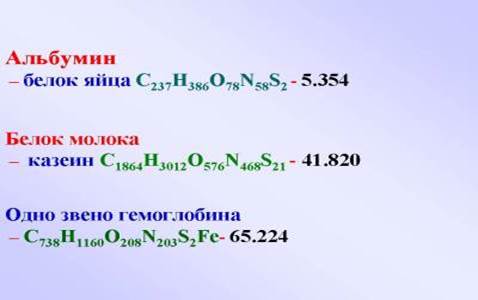
С (углерод)- 50-55%; О (кислород) – 19-24%; N (азот) – 15-18%; Н (водород)- 6-8 %;
S(сера) – 0,3- 2,5%; Р (фосфор) – до 0-5%.
В состав белков также могут входить: хлор, фтор, йод, а также металлы: цинк, магний, железо, медь.
- Какова средняя масса белковых молекул?
Огромна. Альбумин – белок яйца C237H386O78N58S2 = 5.354;
Белок молока – C1864H3012O576N468S21=41.820
Одно звено гемоглобина – C738H1160O208N203S2Fe=65.224
Вывод: Ни одно из природных соединений не обладает такими безграничными потенциальными возможностями изомерии, как белки. Именно так реализуется в природе бесконечное разнообразие структуры белковых тел, дающее начало миллионам растительных и животных видов. Каждый вид обладает собственными видами белков. Если бы в первичной структуре белка не было бы заложено этого качества, то не было бы такого разнообразия жизненных форм, к которым относимся и мы.
- Какая структура является самой прочной? Почему?
(Ответ: Первичная, т.к. связи прочные, ковалентные.)
Именно при помощи радикалов реализуется одно из выдающихся свойств белков – их необыкновенная многогранная химическая активность. (причинно- следственные связи: функции - строение- конфигурация - свойства).
Ученические эксперименты. Исследуем свойства белков с соблюдением правил ТБ.
Доказательство наличие белка только в живых организмах.
В 3 пробирки – свежевыжатый сок картофеля, кусочки сырого картофеля, вареный картофель. К ним добавили перекись водорода. Делаем вывод.
Оборудование и реактивы: альбумин, нагревательный прибор, конц. азотная кислота,
гидроксид натрия, сульфат меди (II), раствор поваренной соли, вода, набор пробирок.
• 1. Это интересно: Зачем маринуют мясо?

Под воздействием уксусной кислоты или лимонной происходит частичный гидролиз белков. Белки распадаются на поли – и дипептиды. В желудке под влиянием ферментов этот процесс продолжается и в итоге приводит к образованию аминокислот. Таким образом, маринование облегчает переваривание белка.
Белки + Н2О → полипептид + Н2О → дипептиды + вода → α – аминокислоты.
2. Отношение к воде – белки образуют коллоидные растворы

Альбумин + вода; желатин + вода, прорастание семян фасоли, гороха и т.д.
• Это интересно: В чем причина образования пены на поверхности мясных бульонов, жареных, рыбных, и мясных изделий?

(Объясняется свертыванием растворимых в воде белков (альбумины, глобумины).
• 3. Осаждение белков: Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остается в виде полипептидной цепи. Этот процесс частично обратим: если не разрушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенности строения макромолекулы белка определяются его первичной структурой - обратимое (высаливание):
Необратимое -?
Какой реакцией можно доказать наличие в белках углерода, водорода, кислорода?
(Реакцией разложения при температуре яичного белка. При этом образуются летучие продукты - запах жженых перьев. Эта особенность белков используется для их обнаружения). Разрушаются все структуры белка.
Вывод: Денатурация белков - потеря естественных свойств (растворимости и др.) вследствие нарушения структуры молекул.
4. Цветные (качественные) реакции на белок:
• Ксантопротеиновая реакция: желтое окрашивание- (обнаружение бензольных ядер в аминокислотных остатках). Поместите кусочек прессованного творога в пробирку и добавьте несколько капель азотной кислоты. Осторожно нагрейте. (Дают не все белки).
Белок + HNO3конц → ярко желтое окрашивание
• Биуретовая реакция: фиолетовое окрашивание- (распознавание пептидных связей). Налейте в пробирку 2 мл яичного белка. Добавьте такой же объем концентрированного раствора гидроксида натрия и несколько капель раствора медного купороса.
Белок + NaOH+CuSO4 → фиолетовое окрашивание.
Биологическое значение белков
Белки входят в состав мозга, всех внутренних органов, скелета и суставов, кожи, волосяного покрова и т. д. В крови в растворенном виде содержится белок гемоглобин, обеспечивающий перенос кислорода по всему организму.
Многие белки выполняют роль ферментов ― катализаторов обмена веществ в живых организмах. В растениях белки концентрируются в основном в семенах. Белковый обмен тесно взаимосвязан с обменом углеводов и нуклеиновых кислот. Существенное влияние на белковый обмен оказывает характер питания, качественный и количественный белковый состав пищи.
Источниками белков могут служить не только животные продукты (мясо, рыба, яйца, творог), но и растительные, например, плоды бобовых (фасоль, горох, соя, арахис, которые содержат до 22-23 % белков по массе), орехи и грибы. Однако больше всего белка в сыре (до 25 %), мясных продуктах (в свинине 8–15 %, баранине 16-17 %, говядине 16-20 %), в птице (21 %), рыбе (13-21 %), яйцах (13 %), твороге (14 %). Молоко содержит 3 % белков, а хлеб 7-8 %.
Среди круп чемпион по белкам ― гречневая (13 % белков в сухой крупе), поэтому именно ее рекомендуют для диетического питания. Чтобы избежать «излишеств» и в то же время обеспечить нормальную жизнедеятельность организма, надо, прежде всего, дать человеку с пищей полноценный по ассортименту набор белков.
Если белков в питании недостает, взрослый человек ощущает упадок сил, у него снижается работоспособность, его организм хуже сопротивляется инфекции и простуде. Что касается детей, то они при неполноценном белковом питании сильно отстают в развитии: дети растут, а белки ― основной «строительный материал» природы.
Каждая клетка живого организма содержит белки. Мышцы, кожа, волосы, ногти человека состоят главным образом из белков. Более того, белки ― основа жизни, они участвуют в обмене веществ и обеспечивают размножение живых организмов. Присутствие протеинов в кремах против морщин, тониках, пене для ванны и др. оберегает кожу от высушивания, придает ей мягкость и упругость.
Применяются протеины также в косметических средствах для ногтей. Являются активными веществами в средствах ухода за волосами (лечебные бальзамы, кондиционеры для волос). Благотворно действуют на нарушенную структуру волос, укрепляют их корни.
 Таким образом, можно сказать белки = жизнь!
Таким образом, можно сказать белки = жизнь!
1.Белки.
 2020-06-29
2020-06-29 99
99








