Нитрата аммония с гидроксидом натрия
Сульфата аммония с гидроксидом калия
Задание 14
При взаимодействии с каким из указанных веществ водород является окислителем?
1) бром 2) калий 3) кальций 4) азот 5) натрий
Запишите номера выбранных веществ в порядке возрастания.
Задание 15
Верны ли следующие суждения о правилах хранения витаминов и предназначении моющих средств?
А. Хранение витаминов не требует строгого соблюдения указанных в инструкции правил.
Б. Для удаления жирных пятен с поверхности посуды целесообразно использовать моющие средства, имеющие щелочную среду.
1) верно только А 2) верно только Б 3) верны оба утверждения 4) оба утверждения неверны
Задание 16
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
| ВЕЩЕСТВА | РЕАКТИВ | |
А) 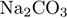 (р-р) и (р-р) и 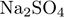 (р-р)
Б) (р-р)
Б) 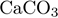 (тв.) и (тв.) и 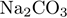 (тв.)
В) (тв.)
В) 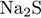 (р-р) и (р-р) и 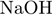 (р-р) (р-р)
| 1)  2)
2) 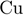 3)
3) 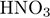 (р-р)
4) (р-р)
4)  (р-р) (р-р)
|
| А | Б | В |
| 3 | 1 | 2 |
Задание 17
Используя метод электронного баланса, составьте уравнение реакции по схеме:

3H2S + KClO3 = 3S + KCl + 3H2O
S2- -2e = S0 | 2 | 3
Cl5+ +6e = Cl- | 6 | 1
Определите окислитель и восстановитель
Задание 18
Дана схема превращений:
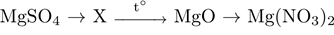
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для последней реакции составьте сокращённое ионное уравнение.
MgSO4 + Ba(OH)2 = BaSO4 + Mg(OH)2
Mg(OH)2 =t°= MgO + H2O
MgO + 2HNO3 = Mg(NO3)2 + H2O
2H+ + O2- = H2O
Задание 19
170 г раствора нитрата серебра смешали с избытком раствора хлорида натрия. Выпал осадок массой 8,61 г. Вычислите массовую долю соли в растворе нитрата серебра.
AgNO3 + NaCl = AgCl + NaNO3
m(AgCl) ÷ M(AgCl) = 8,61÷143,5 = 0,06 моль
m(AgNO3) = 0,06 × 170 = 10,2 г
w (Ag) = 10,2 ÷ 170 = 0,06
Ответ: массовая доля AgNO3 в растворе = 6%.
 2020-07-01
2020-07-01 149
149







