При расчетах тепловых установок приходится встречаться со смесями газов, а в таблицах приводятся теплоемкости только для отдельных идеальных газов; поэтому нужно уметь определить теплоемкость газовой смеси. Если смесь газов задана массовыми долями, то массовая теплоемкость смеси определяется как сумма произведений массовых долей на массовую теплоемкость каждого газа:
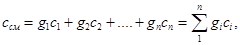 (5.15)
(5.15)
где g1, g2, gn—массовые доли каждого газа, входящего в смесь.
Если смесь газов задана объемными долями, то объемная теплоемкость смеси равна сумме произведений объемных долей на объемную теплоемкость каждого газа:
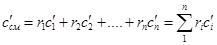 . (5.16)
. (5.16)
Массовая теплоемкость смеси газов может быть определена, если известны плотность и удельный объем смеси газов при нормальных физических условиях:
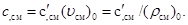 (5.17)
(5.17)
Энтропия.
Разделив обе части уравнения первого закона термодинамики на Т, получим:
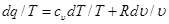 . (5.18)
. (5.18)
Отсюда выражение dq/T при обратимом изменении состояния газа есть полный дифференциал некоторой функции переменных Т и υ (сυ зависит только от температуры, а R— величина постоянная). Клаузиус назвал эту функцию энтропией и обозначил буквой S. Измеряется полная энтропия S в джоулях на градус (Дж/град), а удельная энтропия s — в джоулях на килограмм на градус [Дж/(кг · град)].
Таким образом, дифференциал энтропии для обратимого изменения состояния определяется как
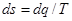 . (5.19)
. (5.19)
Энтропия есть однозначная функция состояния газа, принимающая для каждого его состояния вполне определенное значение. Энтропия может быть определена как функция основных параметров состояния:
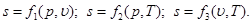
Величина дифференциальа энтропии как функции Т и υ определяется уравнением:
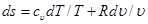 . (5.20)
. (5.20)
Интегрируя при сυ = const найдем для идеального газа
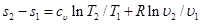 . (5.21)
. (5.21)
В случае когда энтропия является функцией p и T, полуаем:
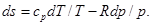 (5.22)
(5.22)
Интегрируя при ср = const, находим
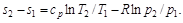 (5.23)
(5.23)
При условии s=f (p,υ), будем иметь
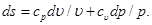 (5.24)
(5.24)
Интегрируя, определяем
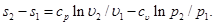 (5.25)
(5.25)
 2020-08-05
2020-08-05 378
378








