Как уже указывалось, печень участвует в обезвреживании ряда эндогенных токсических продуктов клеточного метаболизма или веществ, поступивших извне. Детоксикации подвергаются вещества, образуемые микробами в кишечнике и через портальную систему попадающие в печень. Это токсические продукты обмена аминокислот - фенол, крезол, скатол, индол, аммиак. Реакции детоксикации осуществляются с помощью ферментов, связанных с гладким эндоплазматическим ретикулумом и митохондриями.
Окислительные процессы нейтрализуют ароматические углеводороды, некоторые стероидные гормоны, атофан. К окислительным процессам относятся дегидрирование этанола под действием алкогольдегидрогеназы. Последняя превращает этиловый алкоголь в альдегид с последующим его окислением.
Восстановительные реакции делают безвредными многочисленные нитросоединения, в том числе 2,4-динитрофенол, превращающиеся в аминосоединения.
Детоксикация ряда лекарственных веществ, например сердечных гликозидов, алкалоидов, происходит в результате гидролиза.
Некоторые вещества детоксицируются путем включения в синтез веществ, безразличных для организма или используемых в различных метаболических процессах (включение аммиака в синтез мочевины, нуклеиновых кислот).
Важнейшей реакцией детоксикации является конъюгация, ведущая к инактивированию или повышению растворимости и ускорению выведения образующихся продуктов. Обезвреживание происходит за счет соединения с глюкуроновой или серной кислотой. С помощью конъюгации инактивируются стероидные гормоны, билирубин, жлечные кислоты, ароматические углеводороды и их галогенопроизводные. В качестве обезвреживающих веществ в организме используются также глицерин, таурин, цистеин для образования парных соединений ЖК, бензойной кислоты, никотиновой кислоты.
Химический клиренс крови может осуществляться печенью путем избирательного поглощения вещества из крови и выделения его из организма желчью без химических превращений, например, холестерин может частично выделяться с желчью в неизмененном виде.
Нерастворимые частички удаляются из крови путем активного фагоцитоза купферовскими клетками. Фагоцитарные клиренсные функции купферовских клеток связаны прежде всего с их иммунной защитной ролью, они выступают в качестве фиксаторов иммунных комплексов. Купферовские клетки наряду с другими клетками ретикулоэндотелиальной системы фагоцитируют различные инфекционные агенты, удаляют из тока крови разрушенные эритроциты.
Обмен гормонов и витаминов
Стероидные гормоны (глюкокортикостероиды, андрогены, эстрогены, альдостерон) образуются вне печени, но ей принадлежит важнейшая роль в их инактивации и распаде. Именно печень осуществляет ферментативную инактивацию и конъюгацию стероидных гормонов с глюкуроновой и серной кислотами. Печень активно влияет на гомеостатическую регуляцию уровня глюкокортикоидных гормонов. Она синтезирует также специфический транспортный белок крови - транскортин, который связывает гидрокортизон, делая его временно неактивным.
Инактивация серотонина и гистамина
совершается путем окислительного дезаминирования с участием высокоактивной МАО и гистаминазы. Повышение концентрации гистамина может быть одной из причин кожного зуда и язвообразования в желудочно-кишечном тракте.
Печень участвует в обмене почти всех витаминов, в ней происходит их депонирование и частично разрушение. Обмен витамина А на всех этапах прямо зависит от функции печени. Всасывание поступающего с пищей жирорастворимого витамина А в кишечнике вместе с другими веществами липидной природы происходит благодаря эмульгирующему действию желчи. Большая часть витамина А накапливается печенью в мельчайших жировых капельках в цитоплазме печеночных и купферовских клеток. Так же, как и в кишечнике, в печени каротин превращается в витамин А.
При заболеваниях печени нарушаются всасывание в кишечнике, накопление в печеночной ткани и поступление витамина в кровь. Присутствие желчи в кишечнике - необходимое условие всасывания и других жирорастворимых витаминов - D, Е, К. Витамин Е (токоферол) ингибирует процессы окисления, и его недостаток в организме ведет к повреждению паренхимы печени. Витамин К участвует в синтезе факторов протромбинового комплекса, осуществляемом гепатоцитами, и недостаточное его всасывание в кишечнике служит одной из причин гипопротромбинемии и геморрагического диатеза при патологии печени.
Обмен большинства витаминов комплекса В непосредственно связан с функцией печени. Многие из них входят в состав коферментов. Функции окислительных дыхательных ферментов связаны, в частности, с присутствием в ткани витамина В1, депонируемого в форме кокарбоксилазы и участвующего в декарбоксилировании?-кетокислот. Витамин В2 (рибофлавин) активно участвует в окислительном дезаминирования аминокислот. Витамин В5 (пантотеновая кислота) входит в состав ацетилкоэнзима А и непосредственно связан с последними этапами цикла Кребса в образовании конечных продуктов метаболизма белков, жиров, углеводов, детоксикацией ароматических аминов, сульфонамидов и др. Витамин В6 (пиридоксин) является коэнзимом ферментов, участвующих в трансаминировании и декарбоксилировании аминокислот, в катализе основных жирных кислот, входит в состав фосфорилазы, гистаминазы.
Обмен ферментов
Все метаболические процессы в печени осуществляются только благодаря содержащимся в гепатоцитах соответствующим ферментам. Синтез ферментов является одной из важнейших функций печени, а динамическое постоянство ферментных констелляций в печени - необходимое условие ее нормального функционирования. Ферменты имеют белковую природу и синтезируются рибосомами. Вместе с тем все клеточные органеллы обладают своим специфическим набором ферментов, определяющим их биологическую роль. Митохондрии содержат главным образом ферменты энергетического обмена (ферменты окислительного фосфорилирования, цикла Кребса, АТФ-азу и др.). С гранулярным эндоплазматическим ретикулумом связаны ферменты белкового синтеза, с гладкой его частью - ферменты углеводного, липидного обмена, большинства реакций детоксикации, с лизосомами - основные гидролазы.
В процессе распада большинство ферментов подвергается протеолизу. Другой путь разрушения ферментов состоит в прижизненной термической инактивации. Некоторые ферменты выделяются с желчью (щелочная фосфатаза, лейцинаминопептидаза) или с мочой (амилаза).
Патологические процессы в печени вызывают различные нарушения ферментативного равновесия в ней и изменение активности ферментов печеночного происхождения в сыворотке крови. Определение активности тех или других ферментов в сыворотке крови позволяет судить о характере и глубине поражения различных компонентов гепатоцитов.
В клинической практике ферменты разделяют по функции клеток печени и их мембран, определяющих активность этих ферментов в сыворотке крови [Хазанов А. И., 1968; Блю-гер А. Ф., 1975]. Это разделение весьма удобно для клинического анализа ферментных сдвигов. Выделяют следующие группы ферментов.
Секреторные синтезируются гепатоцитами и в физиологических условиях выделяются в плазму, выполняя в ней определенные функции. И. Тодоров называет эти ферменты собственными ферментами плазмы (сыворотки) крови. К ним относятся холинэстераза, церулоплазмин, про- и частично антикоагулянты.
Индикаторные ферменты выполняют определенные внутриклеточные функции. Некоторые из них (лактатдегидрогеназа, аланин- и аспартатаминотрансферазы, альдолаза) в физиологических условиях в небольших количествах постоянно присутствуют в плазме крови, другие выявляются в сыворотке только при глубоких повреждениях печени. Физиологическая роль ферментов, постоянно присутствующих в плазме, неясна. Предполагают, что выход ферментов в кровь в физиологических условиях связан с состоянием клеточной мембраны, так как для поддержания определенной плотности мембраны нужен постоянный расход энергии.
Вероятно, присутствие ферментов в плазме в нормальных условиях зависит от места расположения фермента в гепатоците и его способности проникать через клеточную мембрану. Индикаторные ферменты в зависимости от расположения в клетке разделяются на цитоплазматические (лактатдегидрогеназы, аланинаминотрансфераза), митохондриальные (глютаматдегидрогеназа) и ферменты, встречающиеся в обеих клеточных структурах - аспартатаминотрансфераза и малатдегидрогеназа.
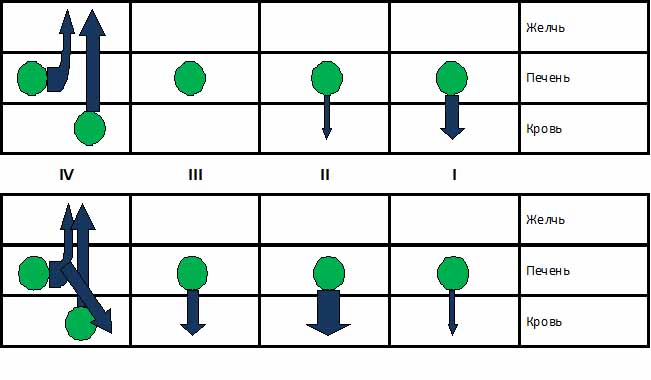
Рис. 3.Схема изменения активности различных ферментов в норме и при заболеваниях печени (по А. И. Хазанову).
А - в норме; Б - в патологии. I - секреционные ферменты (холинэстераза); II - III - индикаторные ферменты (аминотрансферазы, сорбитдегидрогеназа); IV - экскреционные ферменты (щелочная фосфатаза, частично лейцинаминопептидаза).
Экскреторные ферменты образуются в печени и частично в других органах, в физиологических условиях выделяются с желчью (лейцинаминопептидаза, (3-глюкуронидаза, 5-нуклеотида за, щелочная фосфатаза).
Изменение активности этих групп ферментов в физиологических условиях и при различных заболеваниях печени схематично представлено на рис. 13.
Достижения клинической энзимологии в определении. места образования ферментов позволили разделить их по локализации:
1) универсально распространенные ферменты, активность которых обнаруживается не только в печени, но и в других органах - аминотрансферазы, фруктозо-1-б-дифосфатальдолаза;
2) печеночноспецифические (органоспецифические) - ферменты, активность которых исключительно или наиболее выявляется в печени. К ним относятся уроканиназа, аргиназа, фруктозо-1-фосфатальдолаза, холинэстераза, орнитинкарбамилтрансфераза, сорбитдегидрогеназа и др.;
3) клеточноспецифические ферменты печени относят преимущественно к гепатоцитам, купферовским клеткам или желчным канальцам, (5I-нуклеотидаза, щелочная фосфатаза, аденозинтрифосфатаза);
4) органеллоспецифические ферменты, как уже указывалось выше, являются маркерами определенных органелл гепатоцита: митохондриальные (глютаматдегидрогеназа, сукцинатдегидрогеназа, цитохромоксидаза), лизосомальные (кислая фосфатаза, дезоксирибонуклеаза, рибонуклеаза), микросомальные (глюкозо-6-фосфатаза).
Подобная классификация не лишена недостатков хотя бы потому, что ряд печеночноспецифических ферментов не являются абсолютно специфичными для печени. Ее несомненное достоинство в том, что она значительно расширяет и детализирует оценку функциональных повреждений гепатоцитов с помощью сывороточной ферментограммы.
 2020-08-05
2020-08-05 160
160







