1. Реакция Вюрца (удлинение углеродной цепи алканов):
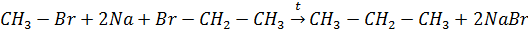
2. Реакция Дюма (декарбоксилирование солей карбоновых кислот – сплавление со щелочами):
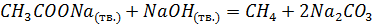
3. Реакция Кольбе (электролиз растворов солей карбоновых кислот):
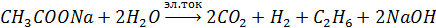
4. Реакция Вюрца-Фиттига (получение гомологов бензола из галогенбензола):
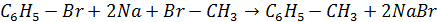
5. Реакция Кучерова (гидратация алкинов):
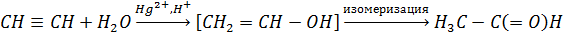
6. Реакция Зелинского (тримеризация ацетилена):
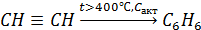
7. Реакция Зелинского–Казанского (получение бензола из циклогексана):
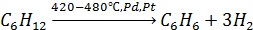
8. Реакция Коновалова (нитрование алканов):
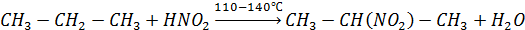
9. Реакция Зинина (восстановление нитробензола до анилина):
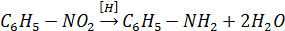
10. Реакция Густавсона (получение циклоалкана из дигалогенопроизводных):
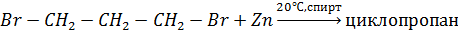
11. Реакция Фриделя–Крафтса (алкилирование бензола):
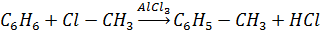
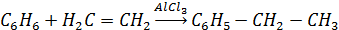
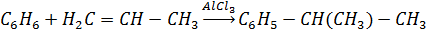
12. Реакция Прилежаева (каталитическое окисление этилена с получением эпоксида):
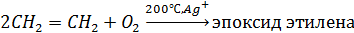
13. Реакция Вагнера (мягкое окисление алкенов):
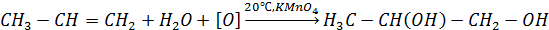
14. Реакция Лебедева (получение бутадиена-1,3):
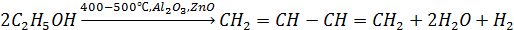
Тема №5 «Приготовление растворов»
Этап 1.
Для приготовления 110 г 11 % раствора Na2CO3 возьмем 110 ∙ 0,11 = 12,1 г чистого карбоната натрия. Далее зальем его 110 – 12,1 = 97,9 г дистиллированной воды.
Этап 2.
Используя раствор соли, приготовленной в этапе 1, приготовим методом разбавления разбавленные растворы карбоната натрия: 2.1 – 60 мл с концентрацией 8 %, 2.2 – 20 мл с концентрацией 5 %.
2.1.
Для начала переведем мл в г. Для этого воспользуемся таблицей плотностей при разных концентрациях [1]. Таким образом, 60 ∙ 1,0555 = 63,33 г. (m1 +m2). Теперь воспользуемся правилом креста:
11 8 – 0 = 8 %
8
0 11 – 8 = 3 %
Далее по формулам [2] вычисляем массы компонентов:
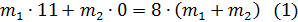
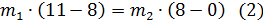
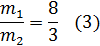
Из (1) уравнения получаем m1 = (63,33 ∙ 8)/11 = 46,058 г.
Из (2) уравнения m2 = (46,058 ∙ 3)/8 = 17,272 г.
Вывод: для приготовления 60 мл раствора Na2CO3 концентрацией 8 % необходимо взять 46,058 г 11 % раствора сульфата натрия и разбавить его 17,272 г дистиллированной воды.
2.2.
Переведем мл в г. Для этого снова воспользуемся таблицей плотностей при разных концентрациях. Таким образом, 20 ∙ 1,0338 = 20,676 г. (m1 +m2). Теперь воспользуемся правилом креста:
11 5 – 0 = 5 %
5
0 11 – 5 = 6 %
Далее по формулам вычисляем массы компонентов:

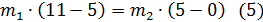
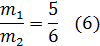
Из (4) уравнения получаем m1 = (20,676 ∙ 5)/11 = 9,398 г.
Из (5) уравнения m2 = (9,398 ∙ 6)/5 = 11,278 г.
Вывод: для приготовления 20 мл раствора Na2CO3 концентрацией 5 % необходимо взять 9,398 г 11 % раствора сульфата натрия и разбавить его 11,278 г дистиллированной воды.
Этап 3.
Для приготовления методом смешения 40 мл 7 % раствора Na2CO3 используем растворы, приготовленные в этапе 2. Переведем мл в г: 40 ∙ 1,04825 = 41,93 г. Снова воспользуемся правилом креста:
8 7 – 5 = 2 %
7
5 8 – 7 = 1 %
Воспользуемся формулами:
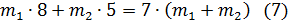
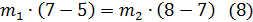
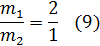
Решаем систему уравнений (7) и (9) методом подстановки:
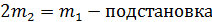
Отсюда m2 = 13,977 г, m1 = 27,954 г.
Вывод: для приготовления 40 мл раствора Na2CO3 концентрацией 7 % необходимо взять 13,977 г 5 % раствора сульфата натрия и смешать его с 27,954 г 8 % раствора той же соли.
Тема №6 «Перегонка»
Оглавление
1. Простая перегонка. 70
2. Вакуумная перегонка. 73
3. Перегонка с водяным паром.. 76
4. Перегонка с дефлегматором.. 79
5. Перегонка нефти. 82
6. Получаемые продукты из нефти. 84
Простая перегонка
Простая перегонка (дистилляция) – способ разделения смеси жидких веществ, основанный на различной температуре кипения компонентов смеси. При этом отогнанный дистиллят обогащается низкокипящим компонентом, а остаток – высоко кипящим.
Область применения
1) Разделение жидких смесей веществ, значительно различающихся по температуре кипения (более 60 °С, менее: см. фракционная перегонка, перегонка с водяным паром, перегонка в вакууме). Но с температурой до 200 °С (более 200 °С вещества разлагаются и следует применять перегонку под вакуумом). Пример: разделение смеси эфир (т. кип. 35 °С)/толуол (т. кип. 110 °С).
2) Отделение жидкого вещества от нелетучих примесей (твердых компонентов). Пример: перегонка эфира (т. кип. 35 °С) над натрием (нелетуч).
3) Наиболее часто простая перегонка используется для очистки продажных растворителей, температуры кипения основных химических растворителей можно посмотреть здесь.
Оборудование
Типичный прибор для простой перегонки приведен на рисунке:
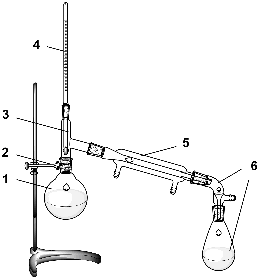
1) Круглодонная колба с исходным раствором. Жидкость должна занимать не более 2/3 объема колбы для предотвращения выброса кипящей жидкости в приемную колбу.
2) Лапка. Важно! Металлическая лапка НЕ должна соприкасаться со стеклом, для избежания растрескивания колбы при перегонке. Для этого между колбой и лапкой помещают резиновые прокладки.
3) Насадка Вюрца или 3-х ходовой переходник. Насадка Вюрца выбирается из варианта (А) для жидкостей с температурой кипения менее 120 °С и (Б) для жидкостей с температурой более 120 °С.
4) Термометр. Выбирается из необходимой температуры кипения жидкости и вставляется в насадку Вюрца таким образом, чтобы верхняя часть шарика ртути совпадала с нижней частью бокового отвода насадки. Термометр без шлифа может быть использован, если имеется соответствующая насадка.
5) Холодильник Либиха. Холодильник Либиха (1) используется для жидкостей с температурой кипения до 120 °С. Его длина тем больше, чем меньше температура кипения вещества. Подключают холодильник к воде таким образом, чтобы поток воды был направлен против движения паров. Для облегчения соединения внешнюю поверхность керном можно смочить водой. Для веществ с температурой кипения более 120 °С используется воздушный холодильник, либо перегонка проводится без холодильника. В редком случае можно использовать обратный холодильник (2).
6) Аллонж и приемные колбы. Аллонж выбирают исходя из следующих критериев: Простой аллонж (А) – для не воспламеняющихся, не гидроскопичных веществ, Важно! при этом используются приемные колбы без шлифа. Аллонж с боковым отводом (Б) – для легковоспламеняющихся веществ (к отводу подсоединяют шланг и направляют его в сливное отверстие, для удаления не сконденсировавшихся паров), для гидроскопичных веществ (к отводу подсоединяют шланг и направляют в склянки Дрекселя или Тищенко с концентрированной серной кислотой, чтобы избежать попадание в перегнанный дистиллят следов влаги, либо соединяют с хлор кальциевой трубкой). Аллонж-«паук» (B) применяют для смены фракций с определенной температурой кипения, отвод используют как и в случае аллонжа (Б).
7) Нагревающий элемент. Выбирают исходя из свойств перегоняемой смеси. Колбонагреватели и пламенные горелки – для негорючих жидкостей. Важно! Водяные бани (т. кип. вещества до 100 °С) – для ЛВЖ. Масляные бани (т. кип. вещества до 200 °С) – для более точной регулировке температуры в перегонной колбе. При этом температура бани на 20-30 °С больше температуры кипения жидкости.
Рекомендации
1) Важно! Следует следить, чтобы прибор всегда был соединен с атмосферой.
2) В перегонную колбу следует добавить «кипелки» (осколки фаянса, молекулярные сита и т.п.) для равномерного кипения жидкости. Важно! Нельзя добавлять свежие кипелки в кипящую жидкость. При этом неизбежно происходит бурное ее вскипание и выброс из колбы.
3) При правильной скорости перегонки на термометре всегда удерживается капля жидкости, если ее нет – раствор перегрет.
4) Нормальная скорость перегонки, если из холодильника стекает 1 капля в 2-3 сек.
5) Если вещество начинает кристаллизоваться при перегонке охлаждение следует отключить, чтобы горячие пары вещества растворили выпавший осадок.
Вакуумная перегонка
Перегонка под вакуумом – способ разделения смеси жидких веществ, основанный на различной температуре кипения компонентов смеси в вакууме. Особое значение имеет при перегонке термолабильных веществ. В вакууме вещества кипят гораздо с меньшей температурой, приблизительное соответствие температуры в вакууме и при атмосферном давлении можно узнать из этой монограммы.
Область применения
1) Разделение жидких смесей веществ, различающихся по температуре кипения (менее 60 °С – с дефлегматором, с более 60 °С – простая перегонка) и имеющих высокую температуру кипения. Пример: выделение ДМСО из смеси ацетон (т. кип. 56 °С)/диметилсульфоксид (ДМСО) (т. кип. 189 °С с разложением при 1 атм., ~60 °С в вакууме водоструйного насоса без разложения).
2) Отделение высоко кипящего жидкого вещества от нелетучих примесей (твердых компонентов). Пример: перегонка ДМСО над гидридом кальция (не летуч).
3) Разделение смесей неразделимых при атмосферном давлении. Пример: разделение азеотропной смеси этанол/вода. Этанол кипит при 70 мм. рт. ст. при 28 °С без образования азеотропа с водой.
4) Часто перегонка под вакуумом используется для очистки продажных высоко кипящих растворителей, реактивов, для очистки и выделения термолабильных или высоко кипящих продуктов реакций.
Оборудование
Типичный прибор для вакуумной перегонки с дефлегматором приведен на рисунке:
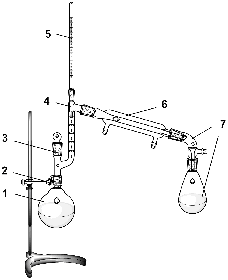
1) Круглодонная колба с исходным раствором (А). Жидкость должна занимать не более 1/3 объема колбы для предотвращения выброса кипящей жидкости в приемную колбу. Часто для вакуумной перегонки используется колбы Кляйзена (Б), уже включающие в себя дефлегматор и переходник к термометру и холодильнику. Важно! Применяют колбы только с круглым дном.
2) Лапка. Важно! Металлическая лапка НЕ должна соприкасаться со стеклом, для избежания растрескивания колбы при перегонке. Для этого между колбой и лапкой помещают резиновые прокладки.
3) Насадка Вюрца или 3-х ходовой переходник. Насадка Вюрца выбирается из варианта (А) для жидкостей с температурой кипения менее 120 °С и (Б) для жидкостей с температурой более 120 °С.
4) Дефлегматор. Длина дефлегматора выбирается из условия, чем уже интервал температур, тем длинее дефлегматор. По разделяющей способности один из лучших дефлегматоров - с насадкой из отрезков стеклянной спирали.
5) Термометр. Выбирается из необходимой температуры кипения жидкости и вставляется в насадку Вюрца таким образом, чтобы верхняя часть шарика ртути совпадала с нижней частью бокового отвода насадки. Термометр без шлифа может быть использован, если имеется соответствующая насадка.
6) Холодильник Либиха. Холодильник Либиха (1) используется для жидкостей с температурой кипения до 120 °С. Его длина тем больше, чем меньше температура кипения вещества. Подключают холодильник к воде таким образом, чтобы поток воды был направлен против движения паров. Для облегчения соединения внешнюю поверхность керном можно смочить водой. Для веществ с температурой кипения более 120 °С используется воздушный холодильник, либо перегонка проводится без холодильника. В редком случае можно использовать обратный холодильник (2).
7) Аллонж и приемные колбы. Аллонж выбирают исходя из следующих критериев: Аллонж с боковым отводом (А) – для перегонки единственной фракции. К отводу подсоединяют шланг и направляют его к вакуумному насосу (через ловушку). Аллонж-«паук» (Б) применяют для смены фракций с определенной температурой кипения, отвод используют как и в случае аллонжа (А).
8) Ловушка. При использовании масляного насоса перед насосом помещают ловушку с жидким азотом, для избежания попадания пара в насос.
9) Нагревающий элемент. Выбирают исходя из свойств перегоняемой смеси. Колбонагреватели и пламенные горелки – для негорючих жидкостей. Масляные бани (т. кип. вещества до 200 °С) – для более точной регулировки температуры в перегонной колбе. При этом температура бани на 20-30 °С больше температуры кипения жидкости.
Рекомендации
1) Важно! Все шлифы прибора должны быть смазаны вакуумной смазкой для получения высокого вакуума. Применяют колбы только с круглым дном. Все работы под вакуумом проводятся в очках, в вытяжном шкафу.
2) Следует помнить, что в вакууме обычные кипелки не работают и необходимо использовать капилляр, деревянную палочку (перегонка на венике) или магнитную мешалку.
3) При правильной скорости перегонки на термометре всегда удерживается капля жидкости, если ее нет – раствор перегрет.
4) Нормальная скорость перегонки, если из холодильника стекает 1 капля в 2-3 сек.
5) При длительных перегонках приемные колбы помещают в охлаждающие бани.
6) Если вещество начинает кристаллизоваться при перегонке охлаждение следует отключить, чтобы горячие пары вещества растворили выпавший осадок.
7) После окончания перегонки охлаждают прибор и лишь потом отключают вакуум. При этом сначала впускают в прибор воздух (или инертный газ) и лишь затем выключают насос.
 2020-08-05
2020-08-05 1929
1929
