| А. Тримеризация ацетилена | 1. С6Н6 + 3Н2 ® C6H12 |
| Б. Алкилирование бензола В. Реакция Вюрца Г. Гидрирование бензола | 2. 3С2Н2 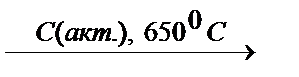 C6H6
3. С7Н14 C6H6
3. С7Н14  C6H5CH3 + 4Н2 C6H5CH3 + 4Н2
|
4. С6Н6 + СН3Сl 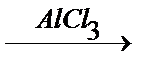 С6Н5СH3 + НСl С6Н5СH3 + НСl
| |
| 6. C6H5Br + CH3Br + 2Na ® С6Н5СН3 + 2NaBr | |
28. Установите соответствие между формулой соли и окрашиванием пламени при внесении ее в пламя горелки:
Название вещества Формула вещества
| А. СаСl2 | 1. Фиолетовое |
| Б. NaCl | 2. Коричнево-красное |
| В. КСl | 3. Желто-зеленое |
| Г. ВаСl2 | 4. Желтое |
| 5. Зеленое |
29. Установите соответствие между схемой окислительно-восстановительной реакции и коэффициентом перед восстановителем:
Схема реакции Коэффициент
А. 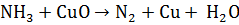
| 1. 6 |
Б. 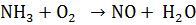
| 2. 5 |
В.  → → 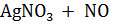 + + 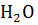
| 3. 4 |
Г. 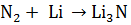
| 4. 3 |
| 5. 2 6. 1 |
30. Установите соответствие между формулой вещества и классом органических соединений:
Вещество Класс органических соединений
А. 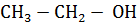
| 1. Карбоновая кислота |
Б. 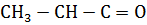

 
| 2. Сложный эфир 3. Спирт 4. Альдегид |
В. 


| 5. Амин |
Г. 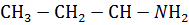

| |
В заданиях 31-32 правильным ответом является последовательность из четырех букв, которые соответствуют правильным ответам в последовательности. Выберите правильные ответы и внесите их в бланк ответа без пробелов, запятых и других символов.
31. Установите последовательность использования реагентов для получения бензоата калия
А) гексан
Б) бензойная кислота
В) бензол
Г) толуол
32. Установите последовательность усиления кислотных свойств веществ
А) H2S
Б) H2SO4
B) H2O
Г) H2SO3
В заданиях 33-34 правильным ответом является число. Запишите это число в бланк ответа без пробелов, запятых и других символов.
33. Составьте уравнения реакций по схемам:
P → P2O5 → H3PO4 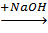 Na3PO4 → Ag3PO4,
Na3PO4 → Ag3PO4,
вычислите сумму коэффициентов во всех уравнениях реакций (запишите число в бланк ответов).
Рассчитайте массу нитробензола, который образуется из бензола массой 234 г при нитровании его азотной кислотой массой 189 г. (Запишите число в бланк ответа с точностью до целочисленного значения).
Вариант № ХХХХ
Тест состоит из 34 заданий различных форм и разного уровня сложности. Ответы на задания Вы должны внести в бланк ответов.
Инструкция по выполнению теста
1. Правила выполнения заданий приведены перед каждым блоком заданий в тесте.
2. Отвечайте только после того, когда Вы внимательно прочитали и поняли суть задания.
3. Старайтесь выполнить все задания.
4. В качестве справочного материала Вы можете пользоваться таблицами: «Периодическая таблица химических элементов Д.И.Менделеева», «Таблица растворимости кислот, оснований, солей в воде», «Электрохимический ряд напряжений металлов», которые приведены в конце теста.
Инструкция по заполнению бланка ответов
1. В бланк ответа вписывайте только правильные, по Вашему мнению, ответы.
2. Ответ записывайте четко, придерживаясь требований инструкции. В заданиях 1-32, верный ответ отметьте символом «Х».
3. В заданиях 33-34 правильным ответом является число. Запишите это число в бланк ответа без пробелов, запятых и других символов.
4. Неправильно отмеченные, исправленные записи будут считаться ОШИБКОЙ! Не ухудшайте свой результат из-за невнимательности!
ЧАСТЬ 1:
Задания 1-20 содержат четыре варианта ответа, среди которых только ОДИН правильный. Выберите правильный ответ и внесите его в бланк ответа.
1. Элементы расположены в порядке уменьшения их атомного радиуса в ряду:
А) Li, Na, K
Б) Au, Ag, Cu
В) C, F, O
Г) Cl, Br, I
2. Масса SO2 количеством вещества 0,25 моль равна
А) 20 г
Б) 40 г
В) 32 г
Г) 16 г
3. Наиболее активный неметаллический элемент второго периода
А) Ne
Б) F
B) Li
Г) Si
4. Число σ-связей в молекуле бромбензола равно
А) 8
Б) 6
В) 12
Г) 7
5. К 60 г раствора хлорида натрия с массовой долей соли 20% добавили 40 мл воды. Массовая доля соли в полученном растворе равна
А) 7%
Б) 12%
B) 20%
Г) 10%
6. Укажите реакцию, в результате которой можно получить нитрат меди(ІІ)
А) нитрат цинка + медь
Б) нитрат серебра + медь
В) нитрат алюминия + медь
Г) оксид азота(II) + медь
7. Максимальный объем (при н.у.) бромоводорода, который может присоединить 0,25 моль ацетилена, равен
А) 11,2 л
Б) 22,4 л
В) 2,24 л
Г) 4,48 л
8. Для получения 25 г железа согласно уравнению
Fe2O3(ТВ) + 3СО(Г) = 2Fe(ТВ) + 3СO2(Г); DН = +27 кДж
требуется затратить теплоту количеством
А) 4,8 кДж
Б) 6 кДж
В) 12 кДж
Г) 13,5 кДж
9. Для осуществления превращений
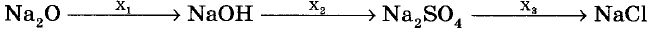
Необходимо последовательно использовать следующие вещества
А) H2O, AgNO3, H2SO4
Б) BaCl2, H2SO4, H2O
B) H2O, H2SO4, BaCl2
Г) H2SO4, BaCl2, H2O
10. Укажите название вещества, имеющего структурную формулу

А) 2,2-диметилпропановая кислота
Б) 2,3-диметилбутановая кислота
В) 2,2-диметилбутаналь
Г) 2,3-диметилпропаналь
11. Объем кислорода (при н.у.), который потребуется для полного окисления 120 л пропана, равен
А) 22,4 л
Б) 600 л
В) 120 л
Г) 840 л
12. Первичным амином является
А) (СН3)2- NН
Б) С2Н5 – NН2
B) (СН3)3- N
Г) С6Н5- NН-СН3
13. Число электронов, участвующих в процессе восстановления в реакции 2С2Н6 + 7O2 ® 4СO2 + 6Н2O, равно
А) 14
Б) 4
B) 7
Г) 28
14. Укажите вещество, которое образуется в результате присоединения хлороводорода к бутену-1
А) 2-хлоробутан
Б) 2-хлоробутен
В) 1-хлоробутан
Г) 2,2-дихлоробутан
15. Укажите условия для проведения межмолекулярной дегидратации спиртов:
А) в присутствии раствора серной кислоты
Б) нагревание до 140°С в присутствии концентрированной серной кислоты
В) при комнатной температуре и в присутствии концентрированной серной кислоты
Г) в присутствии никеля
16. Укажите правильное утверждение: Для смещения равновесия реакции N2(Г) + О2(Г) ⇄ 2NO(Г), DН > 0 вправо необходимо
А) увеличить концентрацию исходных веществ и снизить давление
Б) увеличить концентрацию продуктов реакции и снизить давление
В) увеличить температуру и давление
Г) увеличить концентрацию исходных веществ и повысить температуру
17. Продуктами обжига пирита FeS2 являются:
А) FeO и SO2
Б) Fe2O3 и SO2
В) FeO и SO3
Г) Fe2O3 и SO3
18. Верны ли следующие суждения о свойствах жиров?
1 – Жиры – это сложные эфиры глицерина и высших карбоновых кислот
2 – Омыление жиров происходит как в кислой, так и в щелочной среде
А) верно только 1
Б) верно только 2
В) верны оба суждения
Г) оба суждения неверны
19. Укажите продукты гидролиза метилацетата
А) СН3СООН, СН3ОН
Б) СН3СООН, СН3СОН
В) С3Н7СООН, СН3ОН
Г) СН3ОН, НСООН
20. Химическая реакция в растворе возможна между
А) 
Б) 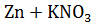
B) 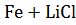
Г) 
Задания 21-25 содержат шесть вариантов ответов, среди которых НЕСКОЛЬКО правильных. Выберите правильные ответы и внесите их в бланк ответа.
21. Из перечисленных характеристик к метиламину относятся:
А) не имеет запаха
Б) реагирует с этаном
В) горит
Г) является донором электронной пары
Д) изменяет окраску лакмуса на синий
Е) проявляет амфотерные свойства
22. С разбавленным раствором серной кислоты реагируют
А) гидроксид алюминия
Б) угарный газ
B) метан
Г) оксид цинка
Д) медь
Е) карбонат кальция
23. Порядковые номера элементов главных подгрупп
А) 14
Б) 22
В) 32
Г) 40
Д) 20
Е) 24
24. Формулы веществ гомологического ряда ацетиленовых углеводородов
А) гексин
Б) ацетилен
В) пропилен
Г) этиленгликоль
Д) пропин
Е) метаналь
25. Укажите одноосновные кислоты:
А) Н3РO4
Б) Н3ВO3
B) НСlO4
Г) H3AsO4
Д) НРO3
Е) HCN
ЧАСТЬ 2
В заданиях 26-30 к каждому из четырех элементов первого столбца, выберите один соответствующий элемент второго столбца. Выберите правильные ответы и внесите их в бланк ответа без пробелов, запятых и других символов.
26. Установите соответствие между электронными формулами химических элементов и их положением в периодической системе:
|
27. Установите соответствие между типом реакции и схемой реакции:
Тип реакции Схема реакции
| А. Разложение | 1. Гидроксид алюминия® хлорид люминия |
| Б. Обмен | 2. Гидроксид алюминия® оксид алюминия |
| В. Замещение | 3. Гидроксид алюминия ® гексагидроксоалюминат калия |
| Г. Соединение | 4. Алюминий ® нитрат алюминия |
28. Установите соответствие между названием вещества и количеством s- и p-связей в молекуле этого вещества:
Название вещества Количество s- и p-связей
| А. Бутен | 1. Одна p-связь и пять s-связей |
| Б. Этен | 2. Две p-связи и три s-связи |
| В. Этин | 3. Две p-связи и шесть s-связей |
| Г. Пропадиен | 4. Одна p-связь и шесть s-связей |
| 5. Одна p-связь и одиннадцать s-связей |
29. Установите соответствие между реагентами и схемами превращения элемента серы:
 2020-08-05
2020-08-05 169
169








