Кальций - один из важнейших минеральных элементов организма. Он участвует в формировании скелета и тканей зуба, необходим для свёртывания крови, мышечного сокращения, генерации электрических потенциалов, участвует в регуляции проницаемости и возбудимости клеточных мембран, в механизмах выделения медиаторов и гормонов клетками, активирует многие ферменты, имеет значение для роста и размножения клеток. Кальций выполняет роль вторичного посредника в действии многих гормонов и медиаторов на клетки и осуществляет регуляцию внутриклеточных процессов. Постоянный уровень кальция в крови особенно важен для функции возбудимых структур. Даже небольшое его снижение в крови повышает возбудимость нервно-мышечной системы и приводит к тоническим сокращениям скелетной мускулатуры.
В организме содержится 2 кг кальция, 99% которого находится в костях в составе гидроксиапатита [Са10(Р04)6(ОН)2], кристаллы которого заключены в органический матрикс.
Минеральный компонент кости находится в состоянии постоянного обновления благодаря деятельности остеобластов и остеокластов. При этом большая часть кальция находится в состоянии медленного обмена и только 0,4% в состоянии более быстрого обмена с кальцием внеклеточной жидкости, со скоростью 2 г/сут. Показано, что введение радиоактивного кальция в кровь вызывает его появление в зубах уже через 2 часа. Среди многих констант внутренней среды организма концентрация кальция является одной из самых строгих. Уровень кальция в плазме крови колеблется в очень узких пределах 2,2-2,5 ммоль/л. Около 40% кальция сыворотки крови связано с белками, главным образом с альбумином, 50% находится в ионизированном состоянии, и 10% - это кальций, связанный в составе низкомолекулярных комплексов (с цитратами, фосфатами и бикарбонатами).
В клетках концентрация кальция очень низка - 10 -7 мМ/л, это в 1000 раз меньше, чем во внеклеточной жидкости. Такое состояние достигается благодаря действию кальциевой АТФ-азы, которая откачивает кальций из клетки в обмен на ион Н+ и благодаря кальций-натриевому обмену. Большая часть внутриклеточного кальция содержится в митохондриях и цитоплазматическом ретикулуме.
В организм кальций поступает главным образом с молочными продуктами. Рекомендуемая норма -1000 мг в сутки. До 700 мг катиона всасывается в кишечнике, до 200 мг выделяется с мочой, до 100 мг с потом. Некоторое его количество выделяется с калом.
У человека главным местом всасывания кальция является тонкий кишечник, особенно эффективно процесс протекает в 12-перстной и в начальном отделе тонкой кишки. Из просвета кишки кальций поступает в энтероцит через кальциевые каналы по электрохимическому градиенту. На базолатеральной мембране клетки находится кальций-активируемая АТФ-аза, которая транспортирует кальций против электрохимического градиента за пределы клетки. Через межклеточное пространство кальций достигает кровеносных капилляров и поступает в кровь. Одновременно со всасыванием катиона происходит его секреция слюнными, желудочными железами, поджелудочной железой, печенью и железами кишки в просвет кишечника. Часть кальция опять подвергается всасыванию, часть выводится с калом.
Фосфор. В организме фосфор находится в двух состояниях: в виде органических фосфоросодержащих соединений и неорганических фосфатов плазмы, представленных свободными анионами фосфорной кислоты (НРО42- Н2РО4-) и её солями: фосфорнокислым натрием, калием, кальцием. В плазме крови в норме содержится 0,9-1,5 ммоль/л неорганического фосфата. Анионы фосфорной кислоты НРО42- и Н2 РО4- в соотношении 4:1 являются существенной частью буферной системы крови. В пищеварительном тракте фосфор всасывается в виде неорганического фосфат-аниона. Основная часть фосфорнокислых солей откладывается в костях в виде Са3(РО4)2 и образующегося в процессе минерализации костей гидроксиапатита. Между неорганическим фосфатом костей и крови существует постоянный обмен. За сутки обменивается около 10-20% фосфата костной ткани.
Обмен фосфат-аниона тесно связан с обменом кальция. Постоянство концентрации кальция и фосфата в крови и внеклеточной жидкости является результатом динамического равновесия между притоком ионов в кровь (всасывание в кишечнике, реабсорбция в почках, мобилизация из кости) и удалением их из крови (экскреция с мочой, секреция в кишечнике, отложение в кость).
Регуляция этих процессов осуществляется системой, включающей 3 гормона: паратиреоидный гормон (ПТГ), кальцитонин и кальцитриол, образующийся в почках из витамина Д3.
Первый из названных гормонов – паратиреоидный гормон, он же паратирин или паратгормон.Секреция этого гормона паращитовидными железами зависит от концентрации кальция в крови, поступающей к железам. Если содержание кальция снижается, то железы реагируют усиленным выделением паратгормона. При введении паратгормона в кровь экспериментальных животных уже через несколько минут повышалось содержание кальция в крови.
Механизм действия гормона тесно связан с функцией почек и метаболизмом кальция и фосфора в костной ткани. Действие гормона на кость реализуется через остеокласты, разрушающие кость. Увеличивается активность этих клеток, секреция ими фермента коллагеназы, под действием которой происходит разрушение органической основы кости. Возрастает активность гиалуронидазы, вызывающей разрушение гликозаминогликанов основного вещества.
Паратгормон влияет также на цикл трикарбоновых кислот, способствуя накоплению лимонной, молочной и угольной кислот в костной ткани, которые вызывают разрушение минерального компонента кости. Указанные процессы ведут к резорбции кости и поступлению освобождающихся ионов кальция и фосфатов в кровь.
ПТГ действует и на остеобласты. Он ускоряет их жизненный цикл, клетки быстрее погибают и при этом освобождается значительное количество лизосомальных ферментов, разрушающих органический матрикс кости, что сопровождается выходом кальция и фосфатов.
ПТГ является ведущим гормоном, регулирующим выведение кальция и фосфатов почками. Он стимулирует реабсорбцию кальция в почечных канальцах и одновременно значительно снижает реабсорбцию фосфата. Развивающаяся фосфатурия приводит к снижению концентрации фосфат-анионов в крови, что в свою очередь способствует мобилизации неорганического фосфата из кости и переходу его в кровь. А так как в костях фосфат связан с кальцием, то его мобилизация вторично приводит к освобождению ионов кальция и увеличению его концентрации в крови. Паратгормон действует также и на кишечник, где увеличивает всасывание кальция и фосфора. Влияние его на всасывание кальция осуществляется через стимуляцию образования в энтероцитах 1,25-(ОН)2-Дз.
Таким образом, рост концентрации кальция в крови, наблюдаемый при действии ПТГ, достигается за счёт увеличения его поступления из костной ткани, за счёт всасывания в кишечнике и уменьшения выведения с мочой. А снижение концентрации фосфата в крови несмотря на усиление его всасывания в кишечнике и поступление из костной ткани происходит за счёт значительного увеличения его выведения с мочой.
При недостаточной секреции этого гормона (гипопаратиреоз) в крови снижается уровень кальция в крови, что сопровождается тетанией, мышечными судорогами, которые развиваются вследствие повышения возбудимости двигательных центров на фоне гипокальциемии. При гиперпаратиреозе происходит мобилизация кальция и фосфора из кости, костная ткань рассасывается, уровень кальция в крови повышается и кальций может откладываться в паренхиматозных органах.
Следующий гормон, участвующий в регуляции обмена кальция и фосфора - к альцитонин (КТ), вырабатывается парафолликулярными клетками щитовидной железы. В отношении кальция он является функциональным антагонистом ПТГ. Кальцитонин вызывает снижение уровня кальция и одновременно фосфата в крови Стимулом для выделения кальцитонина является увеличение концентрации ионизированного кальция в крови. Кальцитонин угнетает всасывание кальция в кишечнике, одновременно подавляет желудочную и панкреатическую секрецию, тем самым, снижая усвоение экзогенного кальция.
В костной ткани гормон снижает число и активность остеокластов замедляет процесс спонтанной резорбции и мобилизации кальция, стимулируя, наоборот, образование фосфорно-кальциевых комплексов. В почке млекопитающих кальцитонин оказывает кальциуретическое и фосфатоуретическое действие за счет подавления реабсорбции обоих ионов в дистальном отделе нефрона.
Таким образом, уменьшение поступления кальция и фосфата из кишечника, костной ткани и усиленное выведение их почками приводит к снижению концентрации ионов в плазме крови.
Витамин Дз является важнейшим гормоном, регулирующим гомеостаз кальция и фосфора во внутренней среде организма. Необходимый для жизнедеятельности витамин Д3 поступает с пищей через кишечник или образуется в коже из 7-дигидрохолестерина под действием ультрафиолетового облучения. Образовавшийся после неферментативных фотохимических превращений холекальциферол с кровью поступает в печень, где гидроксилируется с образованием 25-гидроксихолекальциферола (25-(ОН)-Д3), который в почках превращается в 1,25-дигидроксихолекальциферол - 1,25-(ОН)2-Д3 и 24,25-дигидроксихолекальциферол - 24,25-(ОН)2-Дз. Первый является наиболее активной гормональной формой витамина Д3 и называется кальцитриолом.
Основная физиологическая роль витамина Д3 состоит в регуляции обмена кальция и фосфатов также за счет влияния на их содержание в костной ткани, всасывание в кишечнике и выделение почками. Действие кальцитриола на клетки-мишени заключается в индукции синтеза кальций связывающего белка (КСБ) - кальбайдина, который участвует во внутриклеточном транспорте кальция. В энтероцитах кишечника кальцитриол стимулирует всасывание кальция и контролирует все процессы, связанные с перемещением катиона через клетки.
Прежде всего, 1,25-(ОН)2-Д3 значительно увеличивает проницаемость щеточной каймы, влияя на липидные компоненты и увеличивая «текучесть» мембраны. В результат облегчается вход кальция в клетку по электрохимическому градиенту. Далее, стимулируя в энтероцитах синтез КСБ, гормон увеличивает количество кальция, доставляемое в базальную часть клетки, где на базолатеральной мембране он же стимулирует активность Са АТФ-азы, откачивающей катион из клетки против электрохимического градиента. Кальцитриол также увеличивает всасывание фосфатов в кишечнике. В почках витамин Д3 увеличивает реабсорбцию кальция и фосфата, способствуя их возвращению в кровь. Таким образом под влиянием витамина Д3 уровень кальция и фосфатов в крови повышается.
Хорошо известно антирахитическое действие витамина Д3. Гормон влияет на процессы минерализации костной ткани прежде всего за счёт увеличения содержания кальция и фосфатов в крови. Кроме того, гормон оказывает прямое действие на процессы отложения Са и Р в кости путём стимуляции образования КСБ хондроцитами.
Действие витамина Д3 на кость зависит от уровня кальция в крови. При достаточном количестве иона кальцитриол оказывает анаболическое действие на кость, особенно у растущих организмов, усиливая синтез остеобластами органического матрикса и способствуя отложению фосфорно-кальциевых соединений. Иная картина наблюдается при гипокальциемии. В этом случае 1,25-(ОН)2-Дз стимулирует всасывание кальция в кишечнике, но тормозит функциональную активность остеобластов и образование кости на тот период, пока кальций в крови не восстановится до нормального уровня за счёт всасывания его в кишечнике. Кроме того, показано, что кальцитриол в низких и высоких концентрациях оказывает противоположное действие на кость. Антирахитическое действие он оказывает в низких концентрациях, а в высоких - подавляет синтез коллагена, тормозит минерализацию кости и способствует её резорбции. Поддержание гомеостаза кальция и фосфата в крови осуществляется при тесном взаимодействии между витамином Д3 и гормоном паратиреоидином. Витамин Д3, усиливая всасывание кальция и фосфатов в кишечнике, приводит к повышению концентрации ионов в крови. На это изменение состава крови паращитовидные железы реагируют снижением секреции паратгормона, что приводит к снижению выведения фосфатов с мочой, в результате в организме будет достаточно и кальция и фосфатов для роста и обновления костной ткани. При гиповитаминозе Д количество кальция и фосфатов в крови оказывается недостаточным для кальцификации костей, что служит причиной развития рахита у детей. Однако концентрация кальция в крови в этих условиях поддерживается почти на нормальном уровне за счёт костной ткани, т.к. в ответ на гипокальциемию возрастает секреция паратгормона и стимулируется процесс деминерализации костной ткани.
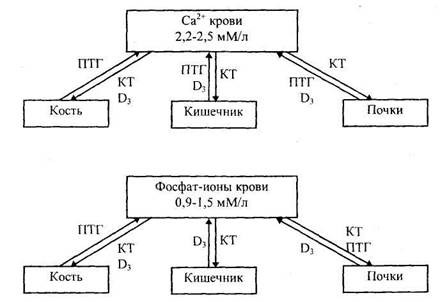
Схема действия паратиреоидного гормона (ПТГ), Bit D3 и кальцитонина (КТ), регулирующих уровень кальция и фосфатов в крови.
Дентин - это та же кость. Он продуцируется одонтобластами, типичными секреторными клетками, аналогичными остеобластам. Одонтобласт секретирует органический компонент межклеточного вещества дентинный матрикс, включающий коллаген, а также протеогликаны и гликозаминогликаны. Затем происходит пропитывание матрикса солями кальция с образованием кристаллов гидроксиапатита. Гормональные регуляторы (витамин Д3, ПТГ и кальцитонин) оказывают такое же влияние на обмен кальция в дентине, как и в костной ткани.
При гипофункции паращитовидных желез и гиповитаминозе витамина Д в детском возрасте нарушается образование эмали и дентина, при гиперфункции отмечаются изменения в пародонте. Снижение секреции кальцитонина сопровождается развитием множественного кариеса.
ВЛИЯНИЕ ЭНДОКРИННЫХ Ж ЕЛЕЗ__НА МОРФОФУНКЦИОНАЛЬНОЕ СОСТОЯНИЕ ОРГАНОВ И ТКАНЕЙ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ.
Железы внутренней секреции влияют на закладку, дифференцировку и развитие органов и тканей полости рта у эмбриона, плода и ребёнка в первые годы жизни.
В эмбриогенезе корковое вещество надпочечников и щитовидная железа начинают функционировать раньше других желёз (8 и 12 неделя соответственно). Гормоны этих желёз стимулируют рост и дифференцировку тканей и органов всего организма плода, в том числе и органов челюстно-лицевой области. Начиная с 6-7 недели эмбрионального периода, образуется твёрдое и мягкое нёбо и происходит разделение первичной ротовой полости на полость рта и носа, развитие преддверия полости рта и языка. В этот же период начинает формироваться зубная пластинка и происходит закладка и образование зачатков молочных зубов. Становление функции щитовидной железы у человека совпадает с периодом дифференцировки зачатков молочных зубов, т.к. на 10 неделе эмбрионального развития образуются амелобласты, на 12 - одонтобласты, на 16 - начинается период дентино- и амелогенеза, и на 17 неделе внутриутробной жизни начинают развиваться постоянные зубы.
Развивающийся зубной зачаток и пародонт очень чувствительны ко всем нарушениям гормонального гомеостаза.
При недостаточной функции щитовидной железы у матери будет наблюдаться недоразвитие всех элементов тканей зубов у плода (системная гипоплазия) и нарушение сроков их прорезывания у ребёнка. Нарушение формирования твердого нёба - его расщепление (палатолалия), аномалия строения языка (глосолалия). При гипотиреозе у ребенка отмечается нарушение прорезывания зубов и аномалия развития эмали, а также значительное увеличение губ и языка, приводящее к затруднению речи и акта глотания. Слизистая оболочка отёчная, дёсны бледные, набухшие. При гипертиреозе отмечается в основном ускоренное прорезывание зубов.
При угнетении функции щитовидной железы или её полном удалении у взрослого человека нарушается фосфорно-кальциевый обмен и развивается множественный кариес в области шеек зубов. Наблюдается также атрофия поднижнечелюстных желёз. При гипертиреозе у взрослого также возможен множественный кариес, кроме того, отмечается набухание десен.
При недостаточности функции коркового вещества надпочечников (болезнь Аддисона) отмечается пигментация слизистой оболочки щёк, губ и края языка. Это происходит вследствие отложения меланина в соединительной ткани и в базальных эпителиальных клетках под влиянием меланотропного гормона гипофиза, секреция которого увеличивается по механизму отрицательной обратной связи между надпочечником и гипофизом вследствие снижения в крови уровня кортикостероидных гормонов.
При гипокортицизме нарушается способность различать оттенки вкусовых и обонятельных ощущений, которая восстанавливается при введении гормонов. При гиперфункции коры надпочечников проявляется катаболическое действие кортикостероидных гормонов - наблюдается рассасывание костной ткани (остеопороз).
Увеличение секреции соматотропного гормона приводит к чрезмерному разрастанию костей и мягких ткней лица, черепа, конечностей- акромегалия. Увеличиваются размеры губ (макрохейлия), языка (макроглоссия), наблюдается гиперплазия дёсен, расширение межзубных промежутков, увеличение зубной дуги.
При недостаточной секреции инсулина поджелудочной железой (диабет) отмечается сухость слизистой полости рта вследствие дегидратации тканей, изменения мелких сосудов, гиперемия слизистой, кровоточивость, нарастающая подвижность зубов, отложения зубного камня.
В главе 8 уже рассматривалась роль паратирина и кальцитонина в поддержании уровня кальция и фосфора в крови. Необходимо добавить, что при пониженной секреции паращитовидных желёз в детском возрасте наблюдается гипоплазия эмали и нарушение образования дентина, у взрослого уменьшается проницаемость эмали. При гиперсекреции изменения развиваются, главным образом, в пародонте. При увеличении секреции гормона щитовидных желёз тиреокальцитонина, а также при увеличении секреции околоушными железами паротина наблюдается увеличение проницаемости эмали.
Таким образом, нарушения функции эндокринных желёз у ребёнка и у взрослого приводят к различным отклонениям в формировании и развитии зубов: к задержке рассасывания молочных зубов, нарушению сроков и порядка прорезывания зубов, изменениям структуры дентина и цемента, некариозному поражению твердых тканей зубов (гипоплазии, патологическому стиранию, некрозу, эрозии).
БОЛЕВАЯ СЕНСОРНАЯ СИСТЕМА.
Боль формируется как ответная реакция организма на действие повреждающих раздражителей. Данная реакция выработалась в процессе эволюции живых существ как приспособительная реакция, направленная на повышение выживаемости во внешней среде. Если бы организм не обладал чувством боли, как это наблюдается в отдельных случаях у людей («врожденная анальгия»), то своевременно определить опасность и вредоносность воздействия было бы невозможно, и смерть организма в таких случаях была бы более вероятной.
Различают боль физическую и психогенную. Физическая, в свою очередь, бывает соматической и висцеральной, поверхностной и глубокой, острой и хронической. Кроме того, начиная с аутоэкспериментов Геда (т.е. опытов на себе, проведённых в 1903г) и вплоть до настоящего времени, боль разделяется ещё на два типа: первый тип — острая, так называемая эпикритическая боль, которая быстро осознаётся, чётко локализуется, хорошо детерминируется, к ней быстро развивается адаптация, и она продолжается не дольше, чем действие стимула; второй тип — тупая, так называемая протопатическая боль, которая осознается более медленно, плохо локализуется и детерминируется, сохраняется длительное время и к ней практически не возникает адаптации. Считается, что второй тип боли эволюционно более древний и менее совершенный как сигнал опасности.
Реакция организма на боль носит системный характер и складывается из нескольких компонентов: 1. сенсорный компонент (перцептуальный) - собственно ощущение боли, возникает на основе афферентных возбуждений, приходящих в ЦНС от болевых рецепторов; 2. аффективный или эмоциональный компонент, чаще всего связанный с переживанием отрицательных эмоций; 3. вегетативный компонент, т.е. вовлечение в реакцию различных висцеральных органов и систем (дыхание, кровообращение, эндокринные железы и т.д.); 4. двигательная защитная реакция, направленная на избегание и на защиту от действия повреждающего фактора.
Гед на себе изучал восстановление болевой чувствительности после перерезки поверхностного кожного нерва, концы которого сшивались шёлком. В первое время после перерезки при действии различных болевых раздражителей на исследуемый участок кожи не было никаких болевых ощущений. Через 8-10 недель, когда восстанавливалось проведение по волокнам группы С (тонкие, безмиелиновые, проводящие с самой низкой скоростью), появились сильные болевые ощущения. Боль была тупая, продолжительная, плохо локализовалась, и к ней не возникала адаптация. Гед назвал её протопатической. Только через 1,5-2 года, когда срастались волокна типа А (толстые, миелиновые, с высокой скоростью проведения), появлялось другое ощущение боли. Она была острой, хорошо локализованной, к ней быстро наступала адаптация. Эту боль Гед назвал эпикритической. По-видимому, в эволюции сначала возникла протопатическая боль (только как сигнал опасности) и лишь позднее - эпикритическая боль (не только как сигнал опасности, но и с дифференциацией её характера и локализации).
Выделяют физиологическую и патологическую боль. Физиологическая (нормальная) боль возникает как адекватная реакция нервной системы на опасные для организма ситуации, и в этих случаях она выступает как фактор предупреждения о процессах, потенциально опасных для организма. Обычно физиологической болью называют ту, которая возникает при целостной нервной системе в ответ на повреждающие или тканеразрушающие стимулы. Главным биологическим критерием, отличающим патологическую боль, является ее дизадаптивное и патогенное значение для организма. Механизмы патологической боли рассмотрим позднее, а пока обсудим механизмы формирования боли в рамках болевой сенсорной системы.
Болевая сенсорная система, как и другие сенсорные системы (анализаторы) состоит из трех отделов: воспринимающего, передающего и коркового. В корковом отделе при взаимодействии с ассоциативными зонами формируется ощущение боли, происходит ее осознание с выработкой варианта поведения для устранения источника боли. Систему восприятия и передачи болевого сигнала называют ноцицептивной системой (nocere-повреждение, cepere- воспринимать, лат.).
Многие годы было непонятно, возникает ли боль в результате активации специфических волокон или в результате сверх активности сенсорных волокон, в норме имеющих другие модальности. Последняя возможность, как кажется, в большей степени соответствует нашему обыденному опыту. За возможным исключением обоняния, любые избыточные по интенсивности сенсорные стимулы - слепящий свет, рвущий ухо звук, тяжелый удар, тепло или холод за пределами нормального диапазона - приводят к возникновению боли. Такой взгляд здравого смысла был заявлен Эразмом Дарвином (Erasmus Darwin) в конце 18-го и Уильямом Джеймсом (William James) в конце 19-го века. Здравый смысл, однако, здесь (как и везде) оставляет желать чего-то еще. В настоящее время мало кто сомневается, что в большинстве случаев ощущение боли возникает в результате возбуждения специализированных ноцицептивных волокон. Ноцицептивные волокна не имеет специализированных окончаний. Они присутствуют в виде свободных нервных окончаний в дермисе кожи и в иных местах организма. Гистологически они неотличимы от C-механорецепторов и C - и A-дельта терморецепторов. Они отличаются от упомянутых рецепторов тем, что порог для их адекватных стимулов выше нормального диапазона. Они могут подразделяться на несколько разных типов по критерию того, какая сенсорной модальность представляет для них адекватный стимул.
Рецепторы боли. Известно, что все соматические рецепторы по порогу чувствительности разделяются на низкопороговые и высокопороговые. Низкопороговые рецепторы возбуждаются слабыми неповреждающими раздражителями (прикосновение, давление и т. д.). Высокопороговые рецепторы, как правило, возбуждаются при воздействии сильных повреждающих раздражителей (сильное сжатие, уколы, разрезы, сильные температурные воздействия, воздействия химических веществ и т д.), но могут реагировать и на неповреждающие стимулы. Эти высокопороговые рецепторы получили название болевых рецепторов или ноцицепторов. Ноцицепторы составляют 25-40% всех рецепторных образований.
По механизму возбуждения болевые рецепторы делятся на механо-, хемо- и термоноцицептры.
Механоноцицепторы локализуются главным образом на коже, а также в фасциях, сухожилиях, суставных сумках, слизистых, в периодонте. Их деполяризация происходит в результате механической деформации мембраны. Возбуждение от большинства механоноцицепторов передаётся по быстропроводящим миэлинизированным А-дельта волокнам.
Термоноцицепторы активируются действием высоких и низких температур. Возбуждение от них передаётся также по волокнам типа А-дельта.
Хемоноцицепторы расположены в более глубоких слоях тканей. Особенно много их в стенках мелких артерий. Специфическими раздражителями для них являются химические вещества алгогены
При травматическом повреждении тканей или при их воспалении высвобождаются особые вещества алгогены. Эти медиаторы воспаления вызывают химическое раздражение болевых рецепторов.
Различают три типа алгогенов:
тканевые (ацетихолин, серотонин, гистамин, простагландины, ионы натрия и калия),
плазменные (брадикинин, каллидин) и
выделяющиеся из нервных окончаний (вещество Р, соматостатин).
Тканевые алгогены непосредственно активируют свободные нервные окончания. Плазменные - также могут действовать на нервные окончания, но чаще они повышают чувствительность окончаний, т.е. сенситизируют ноцицепторы. Вещество Р при повреждающих воздействиях выделяется из нервных окончаний и действует на рецепторы, локализованные на мембране этих же окончаний, вызывая генерацию потока болевых импульсов.
В коже, и, особенно, в дентине зубов были обнаружены своеобразные комплексы свободных нервных окончаний с клетками иннервируемой ткани, которые рассматриваются как сложные рецепторы болевой чувствительности. Особенностью как поврежденных нервов, так и свободных немиелинизированных нервных окончаний является их высокая хемочувствительность.

Рисунок Механизм действия алгогенов, выделяющихся из нервных окончаний.
В теле чувствтельного нейрона (1) синтезируется нейромедиатор, который при помощи аксонного транспорта (4) доставляется к нервным окончаниям на периферию (5) и к центру (2), где выделяется в качестве медиатора (3).
Сильное механическое или термическое раздражение свободных нервных окончаний вызвает выделение нейромедиатора (8) из нервных окончаний (9). Выделившийся медиатор взаимодействует с мембранными рецепторами (7), вызывает дополнительную деполяризация мембраны свободных нервных окончаний и усиление сигнала, корорый передается в ЦНС.
 2020-09-24
2020-09-24 197
197








