В баллоне содержится газ известных значений температуры 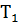 и давления
и давления 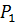 . Термическое уравнение, характеризующее состояние газа, является моделью вириального уравнения неидеального газа Боголюбова-Майера в усеченном виде.
. Термическое уравнение, характеризующее состояние газа, является моделью вириального уравнения неидеального газа Боголюбова-Майера в усеченном виде.
В задании варьируются параметры изучаемого объекта (газа).
Размеры баллона:
Диаметр 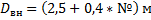
Высота 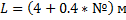
Параметры рабочего тела (газа), содержащегося в газгольдере:
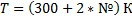
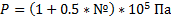 , где № – номер варианта
, где № – номер варианта
Характеристики рабочего тела (газа):
| Газ | Тс, К | Рс, атм | М, кг/кмоль | Vc, 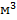 /кмоль /кмоль
| ω |
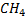
| 190,6 | 45,4 | 16,063 | 0,099 | 0,008 |
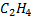
| 282,4 | 49,7 | 28,054 | 0,129 | 0,065 |
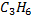
| 365 | 45,6 | 42,081 | 0,181 | 0,148 |
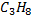
| 369,8 | 41,9 | 44,097 | 0,203 | 0,152 |
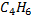
| 425 | 42,7 | 54,092 | 0,221 | 0,195 |
| C2H2 | 308,3 | 60,6 | 26,038 | 0,113 | 0,184 |
| C2H6 | 305,4 | 48,2 | 30,07 | 0,148 | 0,098 |
Определить:
1) массу газа, содержащегося в баллоне (m, кг).
Для определения плотности газа использовать уравнение Ван-дер-Ваальса, представленное в вириальном виде. Объем баллона считать по уравнению следующему соотношению (1.1):
V = 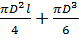 , (1)
, (1)
, где V - объем баллона, [ 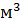 ];
];
D – диаметр цилиндрической части баллона, [ 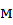 ];
];
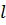 – длина цилиндрической части баллона, [м];
– длина цилиндрической части баллона, [м];
Толщиной стенок пренебречь.
2) Определить значения давления газа в баллоне 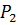 , если все содержимое баллона нагревают до температуры
, если все содержимое баллона нагревают до температуры 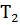 =
= 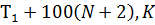 . Процесс считать равновесным.
. Процесс считать равновесным.
Теплопроводность стенок баллона пренебречь. Объем баллона жёсткий.
3) Рассчитать величину подведённой теплоты к газу.
4) Представить (PV), (TS) диаграммы процесса.
Критические параметры и теплофизические характеристики газов представлены в таблице (1) и таблице (2).
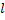
|
| D |
| Рис. 1 Жёсткий газовый баллон. |
Таблица 1. Критические параметры
| Наименование | Формула | M, 
| 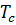 , K , K
| 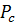 , атм , атм
| 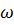 
|
| Метан | C 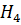
| 16,043 | 190,6 | 45,4 | 0,008 |
| Ацетилен | 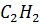
| 26,038 | 308,3 | 60,6 | 0,184 |
| Этилен | 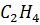
| 28,054 | 282,4 | 49,7 | 0,065 |
| Этан | 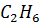
| 30,07 | 305,4 | 48,2 | 0,098 |
| Пропилен | 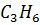
| 42,081 | 365 | 45,6 | 0,148 |
| Пропан | 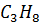
| 44,097 | 369,8 | 41,9 | 0,152 |
| 1,3-Бутадиен | 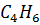
| 54,092 | 425 | 42,7 | 0,195 |
Таблица 2.
Теплофизические характеристики газов.
Константы теплоемкости газов:
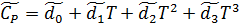 ,
, 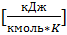 ;
;
Константы уравнения Антуана: A, B, C;
Теплота парообразования при нормальном барометрической температуре 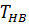 , [K]:
, [K]: 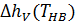 , [
, [ 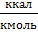 ];
];
| Наименование | Формула |
|
|
| |||||
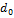
| 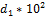
| 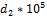
| 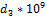
| A | B | C | |||
| Метан | C 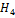
| 1955 | 19,268 | 5,217 | 1,198 | -11,326 | 15,2243 | 897,84 | -7,16 |
| Ацетилен | 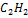
| 4050 | 26,841 | 7,584 | -5,011 | 14,133 | 16,3481 | 1637,14 | -19,77 |
| Этилен | 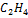
| 3237 | 3.809 | 15,671 | -8,355 | 17,565 | 15,5368 | 1347,01 | -18,15 |
| Этан | 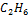
| 3515 | 5,414 | 17,824 | -6,943 | 8,719 | 15,6637 | 1511,42 | -17,16 |
| Пропилен | 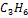
| 4400 | 3,712 | 23,472 | -11,611 | 22,065 | 15,7027 | 1807,53 | -26,15 |
| Пропан | 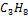
| 4487 | -4,228 | 30,649 | -15,876 | 32,171 | 15,7260 | 1872,46 | -25,16 |
| 1,3-Бутадиен | 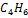
| 5370 | -1,689 | 34,211 | -23,418 | 63,395 | 1577,27 | 2142,66 | -34,3 |
 2020-10-11
2020-10-11 264
264

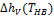 ,
, 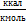
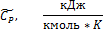
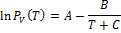 , мм рт. ст.
, мм рт. ст.






