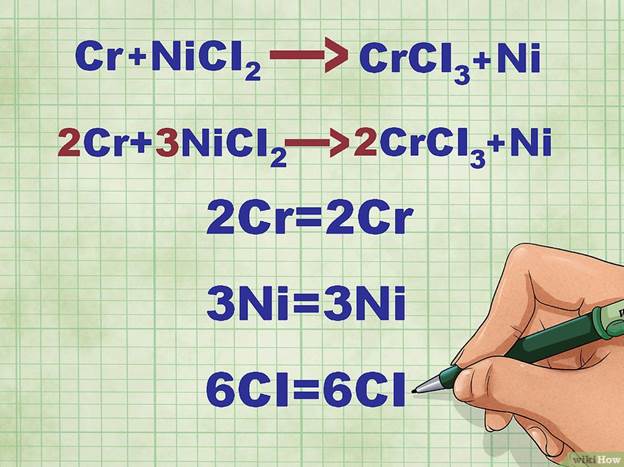
1
Сбалансируйте полное молекулярное уравнение. Прежде чем приступить к записи ионного уравнения, следует сбалансировать исходное молекулярное уравнение. Для этого необходимо расставить соответствующие коэффициенты перед соединениями, так чтобы число атомов каждого элемента в левой части равнялось их количеству в правой части уравнения.
· Запишите число атомов каждого элемента по обе стороны уравнения.
· Добавьте перед элементами (кроме кислорода и водорода) коэффициенты, так чтобы количество атомов каждого элемента в левой и правой части уравнения было одинаковым.
· Сбалансируйте атомы водорода.
· Сбалансируйте атомы кислорода.
· Пересчитайте количество атомов каждого элемента по обе стороны уравнения и убедитесь, что оно одинаково.
· Например, после балансировки уравнения Cr + NiCl2 --> CrCl3 + Ni получаем 2Cr + 3NiCl2 --> 2CrCl3 + 3Ni.
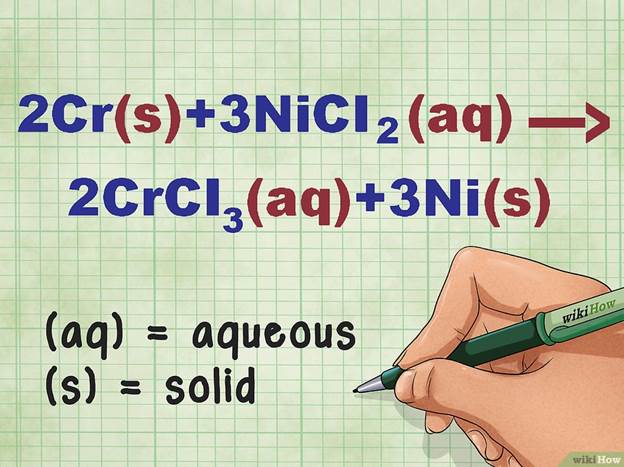
2
Определите, в каком состоянии находится каждое вещество, которое участвует в реакции. Часто об этом можно судить по условию задачи. Есть определенные правила, которые помогают определить, в каком состоянии находится элемент или соединение.[10]
· Если в условии задачи не указано состояние того или иного элемента, используйте для его определения таблицу Менделеева.
· Если в условии сказано, что соединение находится в растворе, отметьте это (р-р).
· Если в уравнение входит вода, определите по таблице растворимости, диссоциирует ли данное ионное соединение.[11] В случае высокой растворимости соединение диссоциирует в воде (р-р). Если соединение имеет низкую растворимость, оно останется в твердом виде (тв).
· Если в реакции не участвует вода, ионное соединение останется в твердом виде (тв).
· Если в задаче фигурирует кислота или основание, они будут растворены в воде (р-р).
· В качестве примера рассмотрим реакцию 2Cr + 3NiCl2 --> 2CrCl3 + 3Ni. В чистом виде элементы Cr и Ni находятся в твердой фазе. NiCl2 и CrCl3 представляют собой растворимые ионные соединения, то есть они находятся в растворе. Таким образом, данное уравнение можно переписать в следующем виде: 2Cr(тв) + 3NiCl2(р-р) --> 2CrCl3(р-р) + 3Ni(тв).
3
Определите, какие соединения диссоциируют (разделяются на катионы и анионы) в растворе. При диссоциации соединение распадается на положительный (катион) и отрицательный (анион) компоненты. Эти компоненты затем войдут в ионное уравнение химической реакции.
· Не диссоциируют твердые тела, жидкости, газы, молекулярные соединения, ионные соединения с низкой растворимостью, многоатомные ионы и слабые кислоты.
· Полностью диссоциируют ионные соединения с высокой растворимостью (используйте таблицу растворимости) и сильные кислоты (HCl(р-р), HBr(р-р), HI(р-р), H2SO4(р-р), HClO4(р-р) и HNO3(р-р)).[12]
· Учтите, что хотя многоатомные ионы не диссоциируют, они могут входить в состав ионного соединения и отделиться от него в растворе.
4
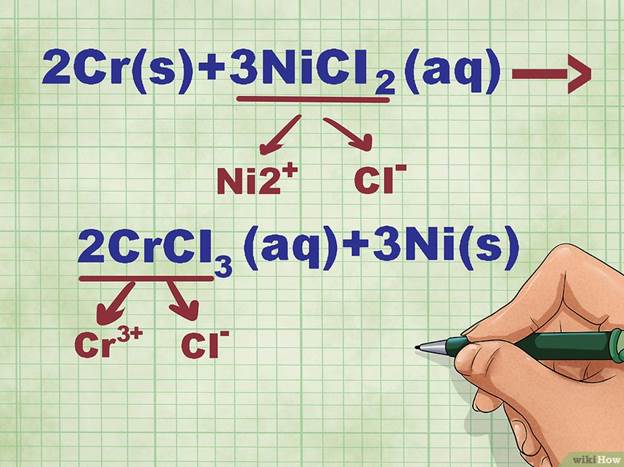
Посчитайте заряд каждого диссоциировавшего иона. При этом помните, что металлы образуют положительно заряженные катионы, а атомы неметаллов превращаются в отрицательные анионы. Определите заряды элементов по таблице Менделеева. Необходимо также сбалансировать все заряды в нейтральных соединениях.
· В приведенном выше примере NiCl2 диссоциирует на Ni2+ и Cl-, а CrCl3 распадается на Cr3+ и Cl-.
· Ион никеля имеет заряд 2+, поскольку он соединен с двумя ионами хлора, каждый из которых имеет единичный отрицательный заряд. При этом один ион Ni должен сбалансировать два отрицательно заряженных иона Cl. Ион Cr имеет заряд 3+, так как он должен нейтрализовать три отрицательно заряженных иона Cl.
· Помните о том, что многоатомные ионы имеют свои собственные заряды 

5
Перепишите уравнение так, чтобы все растворимые соединения были разделены на отдельные ионы. Все что диссоциирует или ионизируется (например, сильные кислоты) распадется на два отдельных иона. При этом вещество останется в растворенном состоянии (р-р). Проверьте, чтобы уравнение было сбалансировано.
· Твердые вещества, жидкости, газы, слабые кислоты и ионные соединения с низкой растворимостью не изменят своего состояния и не разделятся на ионы. Оставьте их в прежнем виде.
· Молекулярные соединения просто рассеются в растворе, и их состояние изменится на растворенное (р-р). Есть три молекулярных соединения, которые не перейдут в состояние (р-р), это CH4(г), C3H8(г) и C8H18(ж).
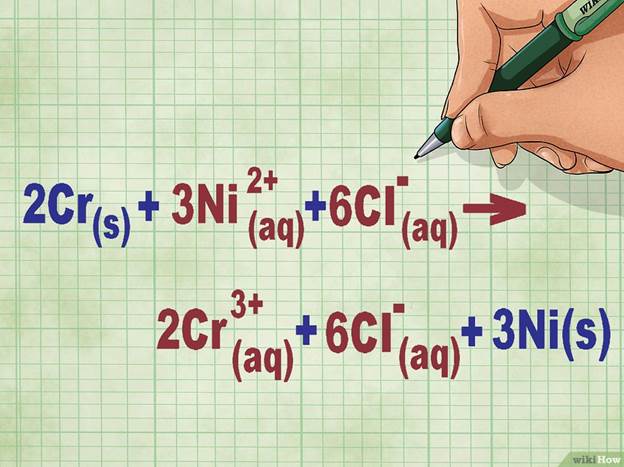
· Для рассматриваемой реакции полное ионное уравнение запишется в следующем виде: 2Cr(тв) + 3Ni2+(р-р) + 6Cl-(р-р) --> 2Cr3+(р-р) + 6Cl-(р-р) + 3Ni(тв). Если хлор не входит в состав соединения, он распадается на отдельные атомы, поэтому мы умножили количество ионов Cl на 6 с обеих сторон уравнения.
6
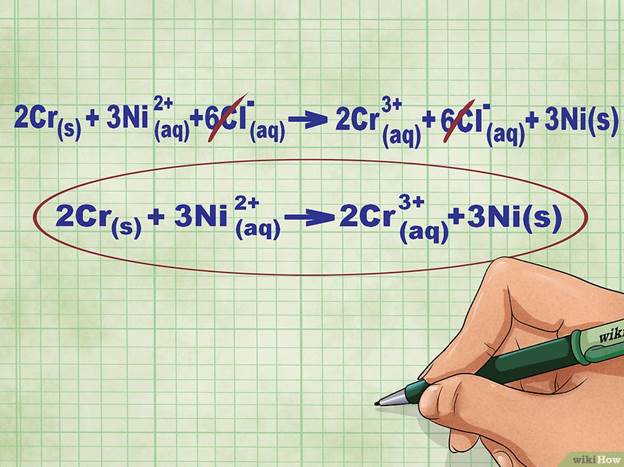
Сократите одинаковые ионы в левой и правой части уравнения. Можно вычеркнуть лишь те ионы, которые полностью идентичны с обеих сторон уравнения (имеют одинаковые заряды, нижние индексы и так далее). Перепишите уравнение без этих ионов.
· В нашем примере обе части уравнения содержат 6 ионов Cl-, которые можно вычеркнуть. Таким образом, получаем краткое ионное уравнение: 2Cr(тв) + 3Ni2+(р-р) --> 2Cr3+(р-р) + 3Ni(тв).
· Проверьте результат. Суммарные заряды левой и правой частей ионного уравнения должны быть равны.
 2020-10-12
2020-10-12 127
127







