В классической механике одинаковые частицы (электроны, протоны, элементарные частицы, атомы и т.д.) не теряют своей индивидуальности. Можно проследить за изменением состояния каждой частицы, ее траекторией и импульсом.
В квантовой механике выполняется соотношение неопределенностей, и понятие траектории не имеет смысла.
В квантовой механике одинаковые частицы теряют свою индивидуальность и тождественно неразличимы.
Принцип тождественности (неразличимости) микрочастиц является фундаментальным принципом и состоит в том, что экспериментально различить тождественные частицы невозможно.
Принцип тождественности микрочастиц можно также определить следующим образом: в системе одинаковых частиц реализуются только такие состояния, которые не меняются при перестановке местами двух любых частиц.
Например, система из 2-х частиц описывается функцией 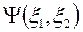 , где
, где 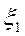 и
и  - совокупность независимых переменных, определяемых местоположением и спином частицы. Если частицы поменять местами, то функция
- совокупность независимых переменных, определяемых местоположением и спином частицы. Если частицы поменять местами, то функция 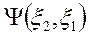 может измениться только на фазовый множитель
может измениться только на фазовый множитель 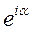 (так, чтобы
(так, чтобы  осталось неизменным). В результате получаем:
осталось неизменным). В результате получаем:

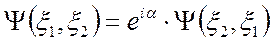 и
и  ,
,
где 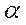 - некоторая вещественная постоянная.
- некоторая вещественная постоянная.
Тогда
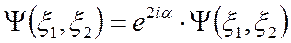 .
.
Из этого выражения следует, что 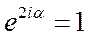 , тогда
, тогда 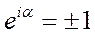 . Это означает, что
. Это означает, что  =
= 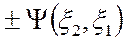 . Знаки
. Знаки  ”+” и “-“ означают симметричные и антисимметричные состояния, определяемые спином.
”+” и “-“ означают симметричные и антисимметричные состояния, определяемые спином.
Частицы, состояния которых описываются антисимметричными функциями, называются фермионами. Это частицы с полуцелым спином (например, электроны, протоны, нейтроны, нейтрино). Системы, образованные этими частицами, подчиняются статистике Ферми-Дирака.
Симметричные функции описывают состояния частиц называемых бозонами. Это частицы с целым спином, к ним относятся, например, фотоны,  - и
- и  - мезоны. Системы частиц, состоящих из бозонов, подчиняются статистике Бозе-Эйнштейна.
- мезоны. Системы частиц, состоящих из бозонов, подчиняются статистике Бозе-Эйнштейна.
Рассмотрим систему, состоящую из 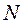 электронов. Каждая частица может находиться в одном из состояний
электронов. Каждая частица может находиться в одном из состояний 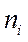 . Амплитуда вероятности
. Амплитуда вероятности 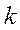 - го состояния системы будет
- го состояния системы будет
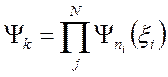 ,
,
где 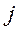 - номер частицы.
- номер частицы.
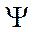 - функция – это суперпозиция всех возможных состояний системы
- функция – это суперпозиция всех возможных состояний системы
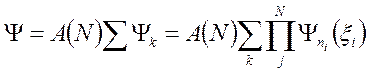 .
.
Для системы из 2-х электронов реализуется антисимметричная комбинация:
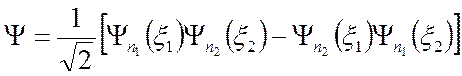
или
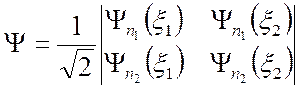 .
.
Для системы из 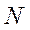 электронов:
электронов:
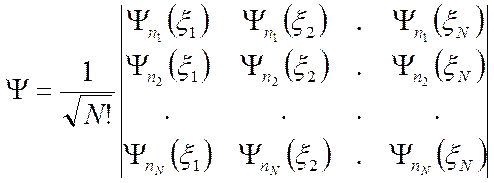 .
.
Если из 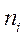 - состояний окажется два одинаковых состояния, например,
- состояний окажется два одинаковых состояния, например, 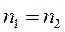 , то две строки определителя будут одинаковыми, и определитель станет равным нулю (из свойств определителя). Получается, что вероятность такой ситуации тождественно равна нулю. Следовательно, для того, чтобы
, то две строки определителя будут одинаковыми, и определитель станет равным нулю (из свойств определителя). Получается, что вероятность такой ситуации тождественно равна нулю. Следовательно, для того, чтобы 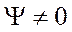 , необходимо, чтобы состояния
, необходимо, чтобы состояния  были различными.
были различными.
Отсюда следует важный вывод: в системе частиц с полуцелым спином (например, электронов) в одном и том же квантовом состоянии не может находиться более одной частицы. Это – так называемый принцип Паули, установленный в 1925 г.
Следовательно, в атоме каждый электрон может находиться в состоянии, характеризуемом квантовыми числами  ,
, 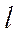 ,
, 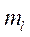 ,
, 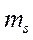 .
.
 2020-10-12
2020-10-12 265
265








