10. Три свободные  имеет атом:
имеет атом:
1) 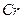 2)
2) 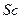 3)
3) 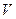 4)
4) 
11. Электронная формула иона 

 соответствует атому:
соответствует атому:
1)  2)
2)  3)
3) 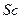 4)
4) 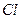
12. Атому  в возбужденном состоянии соответствует формула:
в возбужденном состоянии соответствует формула:
1)  3)
3) 
2)  4)
4) 
13. Низшая степень окисления для элемента с электронной формулой  равна:
равна:
1) 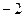 2)
2)  3)
3)  4)
4) 
14. Вещества с ковалентной полярной связью это:
1) хлор 3) кислород
2) вода 4) железо
15.  - гибридизация в следующей частице:
- гибридизация в следующей частице:
1)  2)
2)  3)
3)  4)
4) 
16. Более устойчивый оксид:
1) ½ О2 + Са → СаО, ∆Н= − 635,97 КДж/Моль
2) ½ О2 + 2Ag → Ag2O, ∆H= − 30,56 КДж/Моль
3) ½ O2 + Ba → BaO, ∆H= −558,51 КДж/Моль
4) ½ O2 + Fе → FеO, ∆H= − 263,68 КДж/Моль
17. Основные свойства преобладают в большей степени у оксида (подтвердите расчетами)______
1) СаО + СО2 → СаСО3
∆Gо КДж/Моль -604,2 -394,38 -1128,8
2) SrO + СО2 → SrCO3
∆Gо КДж/Моль -559,8 -394,38 -1137,6
18. Если температурный коэффициент скорости химической реакции равен 2, то при повышении температуры от 20оС до 50оС скорость реакции _________
1) увеличивается в 8 раз 3) увеличивается в 4 раза
2) увеличивается в 6 раз 4) увеличивается в 2 раза
19. Для смещения равновесия в системе SO2 (г) + Cl2 (г) ↔ SO2Cl2 (г), ∆Н < 0
в сторону продуктов реакции необходимо ______________________________
1) понизить температуру 3) понизить концентрацию SO2
2) понизить давление 4) ввести катализатор
20. При повышении давления в 3 раза скорость реакции 2NO (г) + О2 (г) → 2NO2 (г) увеличивается
1) в 6 раз 2) в 8 раз 3) в 9 раз 4) в 27 раз
ИТОГОВАЯ КОНТРОЛЬНАЯ РАБОТА № 2
Способы выражения концентрации растворов; общие свойства
растворов неэлектролитов; растворы электролитов; гидролиз солей;
Окислительно-восстановительные реакции
ВАРИАНТ № 1
 2020-10-10
2020-10-10 157
157








