Укажите номер правильного ответа:
1. Массовая доля глюкозы в растворе, полученном при смешивании 100 г 10%-ного и 200 г 2%- ного растворов, равна _________________ %
1) 4,6 2) 10 3) 15 4) 17
2. Для получения раствора этиленгликоля, замерзающего при (– 37,2оС) необходимо в 500 г воды ( ) растворить __________ граммов этиленгликоля (Мr = 62)
) растворить __________ граммов этиленгликоля (Мr = 62)
1) 620 2) 310 3) 930 4) 465
3. Уравнению реакции K2CO3 + CaBr2 → CaCO3 + 2KBr соответствует сокращенное ионное уравнение
1) 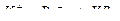 3)
3) 
2) 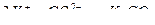 4)
4) 
4. Метилоранж желтый при растворении в воде каждой из двух солей
1) Na3PO4 и K2S 3) Na2SiO3 и FeCl3
2) Ba(NO3)2 и AlCl3 4) K2SO3 и K2SO4
5. В уравнении реакции, схема которой
Na2S + KMnO4 + H2SO4 → Na2SO4 + MnSO4 + K2SO4 + H2O,
сумма коэффициентов перед формулами исходных веществ
1) 25 2) 29 3) 15 4) 16
Дайте полное решение задания, используя ионно-электронный метод.
Часть В. Выполните тестовые задания
Дополните:
1. Массовая доля растворенного вещества (w%) показывает _______________
2. В основе титрометрического анализа лежит закон _____________________
3. Осмотическое давление – это _______________________________________
4. Понижение температуры замерзания растворов от концентрации имеет математическое выражение ∆tозам = ____________, где ________________________
5. Константа диссоциации (Кд) характеризует _________________, для HNO2 имеет следующее математическое выражение ____________________________
6. Слабые многокислотные основания и многоосновные кислоты диссоциируют _____________________________________________________
7. Водородный показатель – это ___________, его математическое выражение имеет вид рН = __________________

8. Раствор серной кислоты имеет рН = 1. Концентрация H2SO4 в растворе при 100% диссоциации равна_______________ моль/л
9. Окислитель в ходе реакции _______________, поэтому его алгебраическая величина степени окисления _________________________________________
10. В кислой среде а) недостаток кислорода в частице берём из _________ с образованием ______________________________________________________
б) избыток кислорода в частице связываем _________ с образованием ______________________________________________________
 2020-10-10
2020-10-10 203
203








