Простые эфиры сравнительно инертны (используются как инертные растворители). Связь С-О в них полярна, но прочна: энергии связей С-О и С-С близки и разрываются в жестких условиях. В ариловых эфирах С-О с ароматическим циклом дополнительно упрочнена р-π-сопряжением.
1. Основные свойства.
Эфиры не растворимы в воде, но растворяются в концентрированной серной кислоте с образованием оксониевых солей:
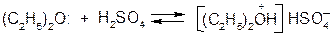
образование комплексов с кислотами Льюиса (эфираты)

2. Расщепление галогеноводородами.
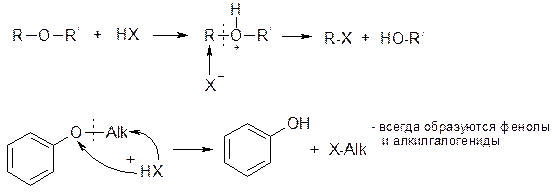
Реакция идет только с концентрированными кислотами (низкая основность эфиров): HI > HBr > HCl > H2SO4.
В растворах щелочей и разбавленных кислот простые эфиры устойчивы.
3. Окисление кислородом воздуха.
Все простые эфиры при хранении на воздухе окисляются кислородом с образованием взрывоопасных гидроперекисей. Поэтому распространенные растворители – диэтиловый эфир, ТГФ, диоксан – перед применением нужно проверять на наличие перекисей и при необходимости проводить очистку от них.

ОКСИРАНЫ (1,2-ЭПОКСИДЫ)
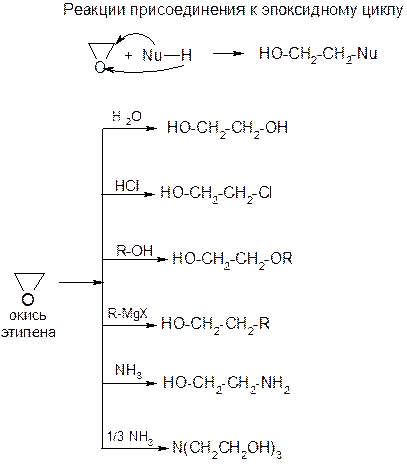
Отдельные представители простых эфиров – см. учебник.
ЛИТЕРАТУРА:
1. Белобородов В.Л., Зурабян С.Э., Лузин А.П., Тюкавкина Н.А. – Органическая химия (основной курс) – Дрофа, М., 2003 г., с. 340 – 404.
26.08.09
 2014-02-05
2014-02-05 873
873







