Виды коллагена
Коллаген — полиморфный белок, в настоящее время известно 19 типов коллагена, которые отличаются друг от друга по первичной структуре пептидных цепей, функциям и локализации в организме. 95% всего коллагена в организме человека составляют коллагены I, II и III типов.
| Типы | Гены | Ткани и органы |
| I | COLIA1, COL1A2 | Кожа, сухожилия, кости, роговица, плацента, артерии, печень, дентин |
| II | COL2A1 | Хрящи, межпозвоночные диски, стекловидное тело, роговица |
| III | C0L3A1 | Артерии, матка, кожа плода, строма паренхиматозных органов |
| IV | COL4A1-COL4A6 | Базальные мембраны |
| V | COL5A1-COL5A3 | Минорный компонент тканей, содержащих коллаген I и II типов (кожа, роговица, кости, хрящи, межпозвоночные диски, плацента) |
| VI | COL6A1-COL6A3 | Хрящи, кровеносные сосуды, связки, кожа, матка, лёгкие, почки |
| VII | COL7A1 | Амнион, кожа, пищевод, роговица, хорион |
| VIII | COL8A1-COL8A2 | Роговица, кровеносные сосуды, культуральная среда эндотелия |
| IX | COL9A1-COL9A3 | Ткани, содержащие коллаген II типа (хрящи, межпозвоночные диски, стекловидное тело) |
| X | COL10A1 | Хрящи (гипертрофированные) |
| XI | COLUA1-COL11A2 | Ткани, содержащие коллаген II типа (хрящи, межпозвоночные диски, стекловидное тело) |
| XII | COL12A1 | Ткани, содержащие коллаген I типа (кожа, кости, сухожилия и др.) |
| XIII | C0L13A1 | Многие ткани |
| XIV | COL14A1 | Ткани, содержащие коллаген I типа (кожа, кости, сухожилия и др.) |
| XV | C0L15A1 | Многие ткани |
| XVI | COL16A1 | Многие ткани |
| XVII | COL17A1 | Гемидесмосомы кожи |
| XVIII | COL18A1 | Многие ткани, например печень, почки |
| XIX | COL19A1 | Клетки рабдомиосаркомы |
Гены коллагена называются по типам коллагена и записываются арабскими цифрами, например СОL1 — ген коллагена 1 типа, COL2 — ген коллагена II типа и т.д. К этому символу приписываются буква А (обозначает α-цепь) и арабская цифра (обозначает вид α-цепи). Например, COL1A1 и COL1A2 кодируют, соответственно, α1, и α2-цепи коллагена I типа.
Синтез и созревание коллагена — сложный многоэтапный процесс, начинающийся в клетке, а завершающийся в межклеточном матриксе:
1. На полисомах ЭПР синтезируются полипептидные препро-α-цепи коллагена. Они содержит начиная с N-конца: 1). гидрофобный «сигнальный» пептид, содержащий около 100 АК; 2). N-концевой пропептид, содержащий около 100 АК, в том числе цистеин; 3). α-цепь коллагена 4). С-концевой пропептид, содержащий около 250 АК, в том числе цистеин. Концевые С- и N-пропептиды формируют глобулярные домены и необходимы для правильного формирования тройной спирали. «Сигнальный» пептид, обеспечивает поступление синтезируемой на рибосоме препро-α-цепи в полость ЭПР.
2. В полости ЭПР при отщеплении сигнального пептида препро-α-цепи коллагена превращаются в про-α-цепи.
3. Поступающие в полости ЭПР про-α-цепи коллагена подвергаются модификации.
а). Цистеины N-пропептидов образуют внутрицепочечные дисульфидные мостики, формируя на N-конце глобулярную структуру;
б). Пролины и лизины в Y-положении (гли-х-у) про-α-цепей гидроксилируются пролил-4-гидроксилазой и лизил-5-гидроксилазой в 4-гидроксипролины (Hyp) и 5-гидроксилизины (Hyl). Некоторые пролины в Х-положениях гидроксилируются в 3-гидроксипролины пролил-3-гидроксилазой. Оксигеназы (гидроксилазы), содержат Fe2+, находятся на мембране ЭПР. Для реакции необходимы а-КГ, О2 и витамин С:
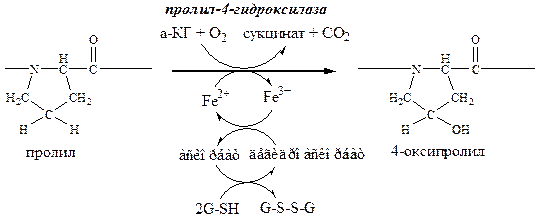
Гидроксилирование пролина необходимо для стабилизации тройной спирали коллагена, ОН-группы гидроксипролина участвуют в образовании водородных связей.
Гидроксилирование лизина необходимо для последующего образования ковалентных связей между молекулами коллагена при сборке коллагеновых фибрилл.
в). Гидроксилизин про-α-цепей при участии гликозилтрансфераз гликозилируется галактозой или галактозилглюкозой. В молекуле коллагена сухожилий (тип I) количество углеводов равно 6, а в моллекуле коллагена капсулы хрусталика (тип TV) — 110. Роль этих углеводных групп неясна.
4). В просвете ЭПР после отделения от рибосом про-α-цепей, 3 из них с помощью С-концевых пропептидов соединяются между собой дисульфидными мостиками (цистеины С-пропептидов образуют внутри- и межцепочечные дисульфидные мостики) и скручиваются с образованием тройной спирали проколлагена. Тройная спираль проколлагена стабилизируется водородными связями. После этого гидроксилирование и гликозилирование про-α-цепей прекращается.
5). Из ЭПР молекулы проколлагена перемещаются в аппарат Гольджи, включаются в секреторные пузырьки и секретируются в межклеточное пространство.
6). В межклеточном матриксе от некоторых проколлагенов (I, II, III, V, XI типов) проколлагенпептидазы отщепляют концевые С- и N-пропептиды, в результате чего образуется тропоколлагены. У проколлагенов IV, VIII, X типов концевые пропептиды не отщепляются.
Синтезированные молекулы проколлагенов и тропоколлагенов способны образовывать различные структуры. Например, тропоколлагены образуют фибриллы, а проколлагены образуют сети.
| Структура | Тип коллагена |
| Фибриллы | I, II, III – основные. V, XI - минорные |
| Ассоциированные с фибриллами | IX, XII, XIV, XVI, XIX |
| Сети | IV, VIII, X |
| Микрофибриллы | VI |
| «Заякоренные» фибриллы | VII |
| Трансмембранные домены | XIII, XVII |
| Другие | XV, XVIII |
 2014-02-02
2014-02-02 10148
10148
