Эта реакция может катализироваться кислотами и основаниями.
При кислотном катализе присоединение идет по электрофильному механизму:
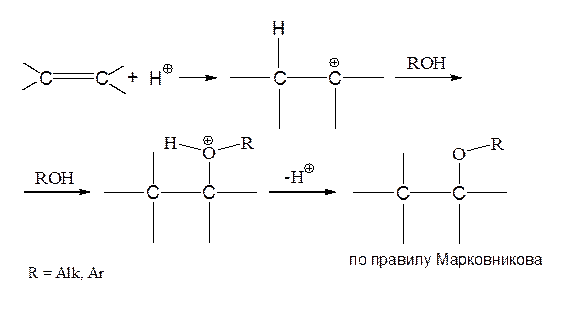
Реакционная способность спиртов уменьшается в ряду:
первичные > вторичные > третичные.
С субстратами, более подверженными атаке нуклеофилов, чем электрофилов (полигалогенолефины, субстраты Михаэля), реакцию лучше проводить в щелочном растворе:
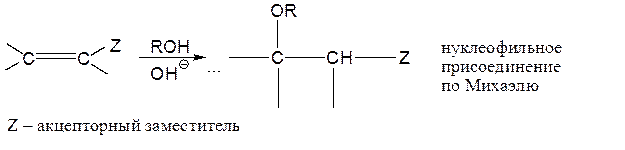
Поскольку тройные связи более чувствительны к нуклеофильной атаке, чем двойные, то присоединение ROH к тройным связям катализируется основаниями особенно эффективно:
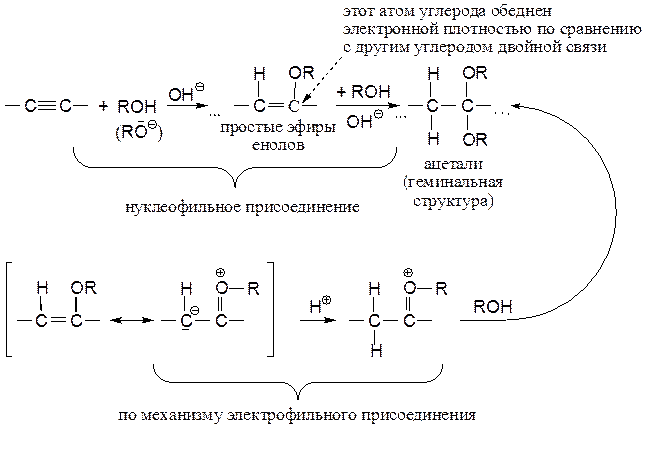
Реакционная способность спиртов уменьшается в ряду: первичные > вторичные > третичные.
Простые эфиры енолов более чувствительны к электрофильной атаке, чем тройные связи, поэтому присоединение спиртов к таким эфирам может также катализироваться кислотами. Как видно из приведенной схемы, и нуклеофильное, и электрофильное присоединение спирта к простому эфиру енола приводит к геминальной структуре – ацеталю. Действительно, из двух возможных промежуточных карбанионов более стабилен «геминальный» анион, поскольку в «вицинальном» анионе электронодонорный заместитель связан с отрицательно заряженным углеродом:
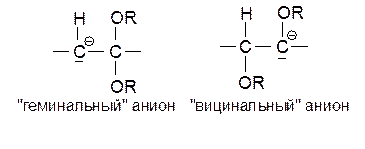
Спирты и фенолы присоединяются к кетенам, давая сложные эфиры:
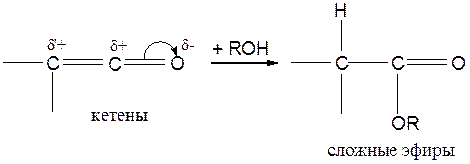
δ'+ < δ+
Это – нуклеофильное присоединение. Аналогично присоединяются к кетенам и другие нуклеофилы:
H2O (OHˉ) ® с образованием кислот;
NH3 ® с образованием амидов;
RCOOH ® с образованием ангидридов кислот.
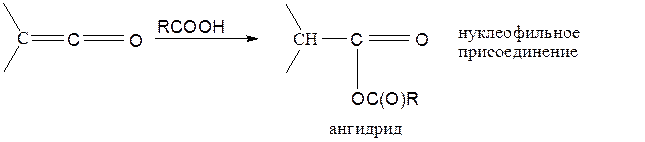
 2014-02-02
2014-02-02 594
594







