Теоретические основы общей химии
Саратов 2006
Общая химия
Лекции по общей химии
для студентов всех специальностей
Удк 678.5
ББК 35.819
Рецензент:
Кафедра общей и неорганической химии
Саратовского государственного университета им. Н.Г. Чернышевского
Доктор химических наук, профессор
Саратовского государственного университета им. Н.Г. Чернышевского
К.К. Ильин
Одобрено
редакционно-издательским советом
Саратовского государственного технического университета
Ю.В. Алексашин, В.В. Ефанова, И.Д. Кособудский,
Е.В. Третьяченко, И.Е. Шпак
Лекции по химии: учеб. пособие / Ю.В. Алексашин, В.В. Ефанова, И.Д. Кособудский, Е.В. Третьяченко, И.Е. Шпак
. – Саратов: Сарат. гос. техн. ун-т, 2006. – 190 с.
ISBN 5-7433-1471-3
В пособии в ясной и доступной форме излагаются основные понятия, законы и методы современной химии в приложении к техническим проблемам.
Пособие состоит из двух частей. В первой части рассмотрены основы теоретической химии, необходимые для понимания свойств многочисленных неорганических соединений и материалов. Также изложены современные взгляды на строение вещества, на закономерности протекания обменных и окислительно-восстановительных процессов, которые объяснены с позиции термодинамики.
Во второй части представлены коллоидные системы, общие свойства, металлов и сплавов, электро- химические системы, методы борьбы с коррозией, полимеры, индентификация химических веществ, химия конструкционных материалов.
© Саратовский государственный
технический университет, 2006
| ISBN 5-7433-1471-3 | © Ю.В. Алексашин, В.В. Ефанова, И.Д. Кособудский, Е.В. Третьяченко, И.Е. Шпак |
1. Предмет химии
Химия как раздел естествознания. Понятие о формах материи: вещество и поле. Специфичность химической формы движения материи. Связь химии с другими науками. Понятие химической системы и химической реакции. Значение химии для инженеров избранной специальности, в технологических и экономических вопросах народного хозяйства. Химия и охрана окружающей среды. Роль химии в решении экологических проблемах.
Основой современного научного мировоззрения является положение: в мире нет ничего, кроме движущейся материи.
Материя – философское понятие для обозначения объективной реальности существующей независимо от сознания человека и данной ему в ощущениях.
Известны две физические формы существования материи – вещество и поле.
Вещество – материальное образование, состоящее из частиц, имеющих собственную массу, т.е. это материя на разных стадиях ее организации: элементарные частицы – ядра атомов – атомы – молекулы – атомные, ионные или молекулярные агрегации (твердые тела, жидкости, газы) и т.д.
Поле – материальная среда, посредством которой осуществляется взаимодействие между частицами вещества или отдельными телами. Например, гравитационное, электромагнитное поля, поле ядерных сил. Основной характеристикой этой формы, материи является энергия.
Основным свойством материи, способом ее существования является движение. Количественной мерой движения материи служит энергия. Между массой и энергией существует взаимосвязь, количественно выражаемая уравнением Эйнштейна: E = m·c2, где E – энергия, m – масса, c – скорость света в вакууме.
Формы движения взаимосвязаны и взаимопревращаемы между собой. Например, атомы могут образовывать молекулы, молекулы разрушаясь, образуют атомы. Формы движения материи изучают разные естественные науки: химия, физика, биология и др. Формы движения могут переходить друг в друга. Например, химическая форма – в электрическую и т.д.
Химия изучает химическую форму движения материи, под которой понимают качественное изменение веществ, т.е. превращение одних веществ в другие. При химических процессах происходит обмен между атомами, разрушение одних связей и возникновение других. В результате химических процессов возникают новые вещества с новыми химическими и физическими свойствами.
Таким образом, химия – это наука, изучающая состав, строение, свойства веществ, их превращения и явления, сопровождающие эти превращения.
Современная химия – это разветвленная система многих наук: общей химии, электрохимии, биохимии и т.д.
Общая химия изучает общие законы и концепции химии, включая периодический закон, теорию химической связи, основные закономерности химических процессов, учение о растворах, окислительно-восстановительные реакции (ОВР) и пр.
Объектом изучения химии являются химические элементы и их соединения.
Химический элемент – это совокупность атомов с одинаковым зарядом ядер. В свою очередь атом – это наименьшая частица химического элемента, сохраняющая его химические свойства.
Молекула – наименьшая частица вещества, способная к самостоятельному существованию, обладающая его основными химическими свойствами. Она состоит из одинаковых или различных атомов. Если молекулы состоят из одинаковых атомов, то вещество называется простым. Например, He, Fe, H2, O2, O3, P4, S8.
Простое вещество является формой существования химического элемента в свободном состоянии.
Если молекула вещества состоит из разных атомов, то вещество называют сложным, или химическим соединением. Например, CO2, H2O, NH3, H2SO4, NaOH, KCl и т.д. Любое вещество характеризуется составом (природой и числом атомов в молекуле), строением (пространственным расположением атомов в молекуле) определенными физическими и химическими свойствами.
Химические свойства вещества характеризуют его способность участвовать в химических реакциях, т.е. процессах превращения одних веществ в другие. Например, стальная конструкция постепенно превращается в ржавчину; топливо в двигателе – в выхлопные газы; вино – в уксус.
Химические процессы могут протекать с изменением химического состава вещества, т.е. химическими реакциями и без изменения (например, фазовые переходы: вода при 100°С превращается в пар, при 0°С – в лед).
Часто процессы записывают в виде уравнений химических реакций или схем процесса:
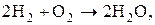
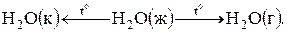
Совокупность веществ, находящихся во взаимодействии и мысленно выделенная из окружающей среды, называется системой. Например, атом H (система из ядра и электрона), водный раствор различных солей (система из H2O и соли), смесь газов над поверхностью катализатора (система H2, N2 и катализатора – пористое Fe).
Химия связана с другими естественными науками. Химические реакции играют важную роль в физических, биологических, геологических и других процессах.
Связь между различными науками очень тесная. На стыках наук возникают новые науки, например, биохимия, геохимия, ядерная химия, космохимия и др.
2. Значение химии в изучении природы
и развитии техники
«Широко распростирает химия руки свои в дела человеческие…», эти слова принадлежат М.В. Ломоносову, сказанные более двух столетий назад.
Современный уровень жизни человечества невозможен без продуктов и методов химии. Химическая отрасль – одна из важнейших отраслей промышленности в нашей стране. Производимые ею химические соединения, различные композиции и материалы применяются повсюду: в машиностроении, металлургии, сельском хозяйстве, строительстве, электротехнической промышленности, связи, транспорте, космической технике, медицине, быту и пр. Только для приготовления пищевых продуктов применяется около тысячи различных химических веществ. Всего для практических нужд промышленность выпускает более 1 миллиона веществ. От химии зависит во многом экологическое благосостояние и обороноспособность страны. Поэтому, чтобы не сдерживать развитие других отраслей промышленности, современная химия должна представлять им новые соединения и материалы с требуемым набором свойств. Химическая наука и химическая промышленность должны развиваться опережающими темпами, расширять ассортимент продуктов, повышать их качество и объем выпуска. В нашей стране существуют неограниченные производства основной химической промышленности, выпускающей кислоты, щелочи, соли, удобрения и другие соединения.
Большое место занимает нефтехимическое производство: получение топлива, масел, растворителей, мономеров, синтетического каучука, химических волокон, препаратов для защиты растений, кормов и добавок ним.
Существует и малая химия, когда объемы выпускаемой продукции невелики, но ассортимент довольно широк. К такой химии относятся вспомогательные вещества: для производства полимерных материалов (катализаторов, стабилизаторов, пластификаторов, антипиренов – веществ, защищающих древесину и другие материалы), красители, лекарственные препараты, дезинфицирующие средства и другие препараты санитарии и гигиены, средства химизации сельского хозяйства – гербициды, инсекциды, фунгициды (защита от грибковых заболеваний), дефолианты и др.
Главным направлением развития современной химической промышленности являются: производство новых соединений и материалов и повышение эффективности существующих производств. Для этого важно найти новые реакции и катализаторы, выяснить механизм протекающих процессов. Это определяет химической подход при решении инженерных задач повышения эффективности производства. Типичной чертой химической промышленности является: 1) сравнительно небольшое количество специалистов-химиков, а больше представителей других специальностей (механиков, теплоэнергетиков, специалистов по автоматизации производства и др.) 2) Характер крупных размеров энерго- и водопотребления, высоких экологических требований к производству.
3. Проблемы защиты окружающей среды
В связи с техническим процессом масштабы возможного воздействия на природу стали соизмеримы с масштабами глобальных природных процессов. Неконтролируемая деятельность человека приводит к негативным изменениям в окружающей среде: земной атмосфере, гидросфере, недрах и плодородном слое Земли, к гибели животных и растений. Возникла необходимость защиты человеком самого себя и среды обитания от собственного воздействия на нее. В охране окружающей среды особенно велика роль химии и химической технологии.
3.1. Охрана атмосферы
Источником загрязнения атмосферы прежде всего являются предприятия черной и цветной металлургии, тепловые электростанции, автомобильный транспорт. Выбросы в атмосферу содержат оксиды углерода, азота, серы, соединения металлов, а также пыль.
Круговорот углерода в природе включает реакцию фотосинтеза: из CO2 и H2O в зеленых растениях под воздействием солнечного света образуются органические вещества, при этом в атмосферу выделяется кислород. С другой стороны, процессы дыхания животных и растений, происходит с участием кислорода. Образующийся CO2 – вновь возвращается в атмосферу.
1. Ученые считают, что все возрастающее выделение CO2 в атмосферу может привести к изменению климата на Земле в результате потепления. Это приведет к таянию полярных льдов и вызовет катастрофическое повышение уровня Мирового океана на 4-8 м.
2. Накопление в атмосфере пыли может привести к понижению температуры на Земле (подумайте, с чем это связано).
3. Увеличение содержания в атмосфере оксидов неметаллов приводит к росту кислотности водоемов и гибели их обителей.
4. Под губительным действием оксидов серы и азота разрушаются строительные материалы и памятники старины.
5. Очень остро перед человечеством состоит проблема выхлопных газов автотранспорта, наносящих ущерб жизнедеятельности животных и растений. Составные части выхлопных газов: CO, оксиды серы, азота, углеводороды, соединения свинца. CO взаимодействует с гемоглобином крови в 200 раз активнее кислорода и снижает способность крови быть его источником. Это приводит к головной боли, снижает умственную способность. Оксиды азота вызывают общую слабость, головокружение, тошноту. SO2 вызывает спазмы дыхательных путей. Свинец – токсичный элемент, действует на ферментные системы, обмен веществ, накапливается в морских отложениях и в пресной воде.
6. Токсические соединения металлов поступают в атмосферу в выбросах предприятий черной и цветной металлургии, а также в результате сжигания отходов и мусора. Отходы от химических предприятий следует утилизировать (на основе химических превращений).
3.2. Охрана гидросферы
Вода на нашей планете занимает 2/3 поверхности Земли. Основная масса воды сосредоточена в морях и океанах. Доля пресной воды составляет только 2%. В природе осуществляется постоянный круговорот воды, который сопровождается ее очисткой.
Вода применяется во всех областях народного хозяйства и в быту. В связи с развитием промышленности, ростом городов расход воды все время увеличивается. Одновременно усиливается загрязнение воды промышленными и бытовыми отходами. Это приводит к нарушению естественных процессов самоочищения водоемов, наносит ущерб их обитателям.
1. Важным показателем качества воды является количество растворенного в ней кислорода. Кислород необходим для жизни обителей водоемов. За счет деятельности аэробных (аэро-воздушный) бактерий кислород используется для окисления органических веществ животных и растительных организмов с образованием CO2, H2O,  . Тем самым осуществляется самоочищение воды.
. Тем самым осуществляется самоочищение воды.
При недостатке кислорода процесс разложения органических веществ ведут анаэробные (не требующие O2) бактерии с образованием CH4, NH3, H2S, PH3. Вода приобретает гнилостный запах, гибнет рыба и другие обитатели водоемов.
2. Большой вред природным водоемам наносят растворенные в сточных водах минеральные удобрения, смываемые с поверхности почвы. Эти удобрения вызывает бурное разрастание сорной травы и водорослей. Это приводит к засорению водоемов и их гибели.
3. Огромный урон живым организмам в водоемах наносят промышленные сточные воды, содержащие ядовитые вещества, в частности соединения токсичных металлов.
Способы очистки сточных вод зависят от характера содержащихся в них загрязнений.
1) Бытовые сточные воды в основном содержат органические вещества. Поэтому они после обеззараживания хлором или озоном подвергается биологической очистке. При биологическом окислении органических веществ образуется биомасса, которую используют для получения белково-витаминного концентрата для подкормки животных.
Очистка промышленных сточных вод от органических веществ применяют также радиационные методы (γ – излучение). Этот метод позволяет уничтожить ядовитые вещества: красители, пестициды, фенолы, поверхностно-активные вещества.
2) Очистка промышленных сточных вод весьма сложна. Они содержат вещества, которые являются ядами для микроорганизмов и не могут быть очищены биологическим методами. Удаление металлов может быть осуществлено осаждением их в виде нерастворимых веществ-осадков (HgS, PbS и т.д.), а также экстракцией органическими растворителями.
3) Для очистки сточных вод от неорганических солей применяются дистилляция, вымораживание, электродиализ, обратный осмос и др. Наиболее надежный способ защиты водоемов основан на создании экономически рациональных замкнутых систем, обеспечивающих многократное использование воды в производстве.
3.3. Безотходная технология
Комплексное использование сырья
Химическая промышленность нашей страны выпускает около 70 тыс. химических веществ. Большие задачи стоят перед химиками и технологами по созданию новых технологий и производству новых химических материалов. Велика роль химической технологии в решении проблемы использования отходов не только химических предприятий, но и тепловых электростанций, горнодобывающей, металлургической промышленности и т.д. Д.И. Менделеев считал, что в химии нет отходов. Любые отходы могут быть использованы как сырье для получения других химических продуктов. Таким образом, важнейшей задачей химической технологии является комплексное использование сырья, создание производств без отходов:
 Потребление
Потребление

 Сырье Производство
Сырье Производство
 Отходы Вторичное сырье
Отходы Вторичное сырье
Примером комплексного использования сырья может служить переработка апатитной руды. Эту руду флотацией разделяют на апатит и нефелин. Из апатита получают H3PO4, фосфорные удобрения, соединения фтора, гипс. При переработке нефелина получают глинозем, поташ, кальцинированную соду, цемент, элемент, галлий.
Важнейшей задачей является переработка шлаков пирометаллургических производств. Шлаки содержат оксиды кремния, алюминия, кальция, магния, железа, марганца, никеля, меди, кобальта, свинца, кадмия, редких металлов и др. элементов. Для выделения металлов из шлаков предложен метод восстановления расплавленного шлака в электропечах коксом в присутствии извести.
Для кардинального решения проблем охраны окружающей среды необходимо международное сотрудничество.
3.4. Ноосфера – сфера разума
Ноосфера – состояние биосферы, при котором разумная деятельность человека становится решающим фактором ее развития.
С развитием науки и техники создаются новые возможности охраны окружающей среды. Акад. В.И. Вернадский еще в начале XX века отмечал, что наступит время, когда человек сделается основным фактором эволюции биосферы.
Биосфера сформировалась и функционирует за счет деятельности растений, животных и микроорганизмов. Сегодня в биосфере доминирующую роль играет человек. Его трудом выведены новые сорта растений, новые породы животных, появились бескрайние поля культурных растений, создаются каналы и новые моря, исчезают болота и пустыни, перемещаются огромные массы ископаемых пород, синтезируются новые материалы и химические элементы. Преобразующая деятельность человека сегодня распространяется на дно океана и в космическое пространство. Все возрастает влияние человека на окружающую среду порождает сложные проблемы во взаимоотношений человека с природой.
Человек – часть природы, поэтому и производительную деятельность человека надо рассматривать в рамках природы. В будущем средой обитания человечества станет ноосфера («ноо» – разум), где разумно и рационально организованные производства и потребление станут основой полной гармонии между человеческим обществом и природой.
Домашнее задание:
Глинка Н.Л. Общая химия Л.: Химия, 1979, с. 11-46 (в дальнейшем идут сокращения: Г., с. 11-46).
Коровин Н.В. Общая химия. М.: Высшая школа, 2002, с. 10-16. (в дальнейшем в сокращенном виде: К., с. 10–16).
 2014-02-02
2014-02-02 3720
3720