2. УФ – спектры поглощения

λ, нм
ХИМИЧЕСКИЕ МЕТОДЫ (ОБЩИЕ РЕАКЦИИ)
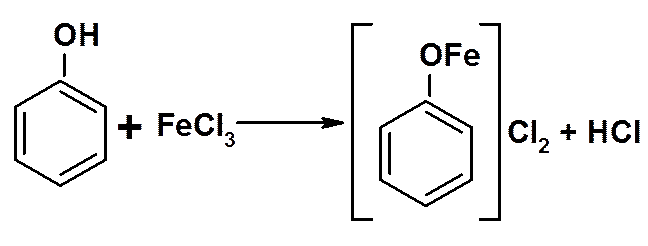 3. Реакция с солями Fe3+ - образование окрашенныХ комплексныХ соединениЙ:
3. Реакция с солями Fe3+ - образование окрашенныХ комплексныХ соединениЙ:
окрашивание зависит от количества фенольных гидроксилов и их расположения:
Фенол – синее или фиолетовое; Резорцин – синее;
Тимол – светло-зеленое (в спиртовой среде).
4. Реакции замещения (с бромной водой):
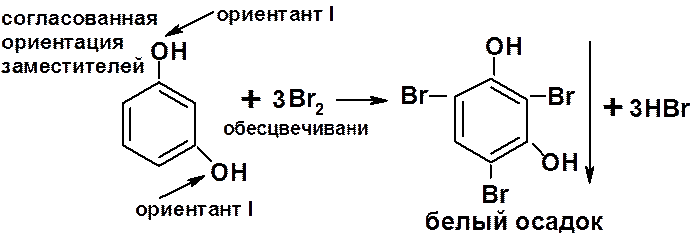
5. Реакция азосочетания ( проходит в два этапа):
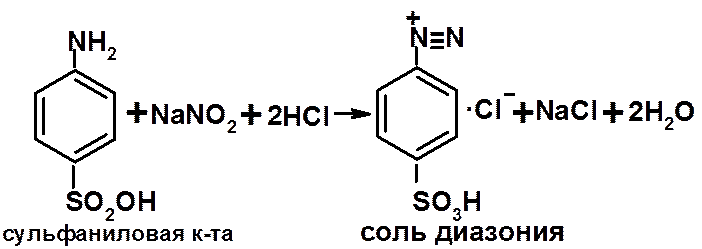 - получЕНИЕ соли диазония:
- получЕНИЕ соли диазония:
- сочетание полученной соли диазония со щелочным раствором фенола:
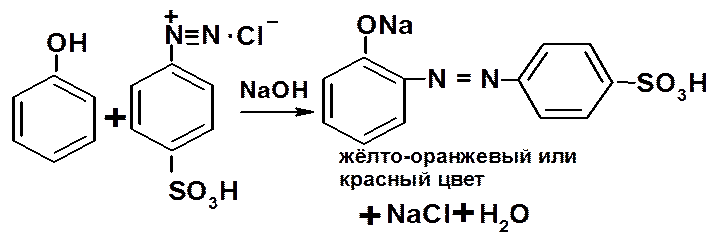
6. Индофенольная проба:
окислители (например, гипохлориты или бромная вода) в присутствии аммиака окисляют фенолы с образованием хинонов, хинониминов и индофенолов:
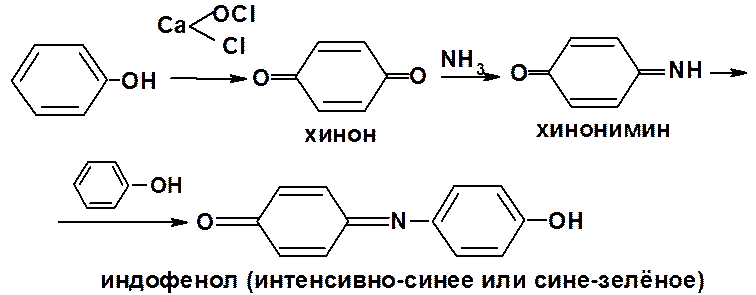
Специфические реакции
7. реакции конденсации:
7.1. с фталевым ангидридом или гидрофталатом калия:
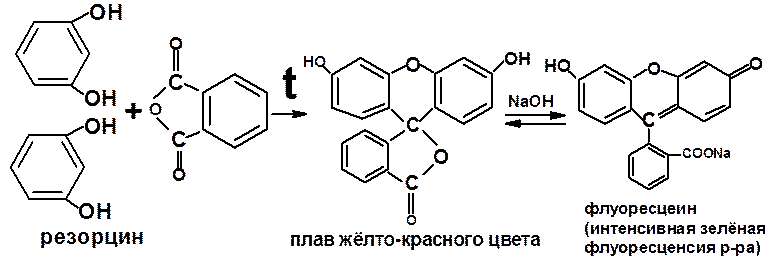
Фенол – в аналогичной реакции образует фенолфталеин
(в щелочной среде – пурпурное окрашивание);
Тимол – тимолфталеин
(синее окрашивание в щелочной среде)
7.2. с хлороформом в присутствии гидроксида натрия:
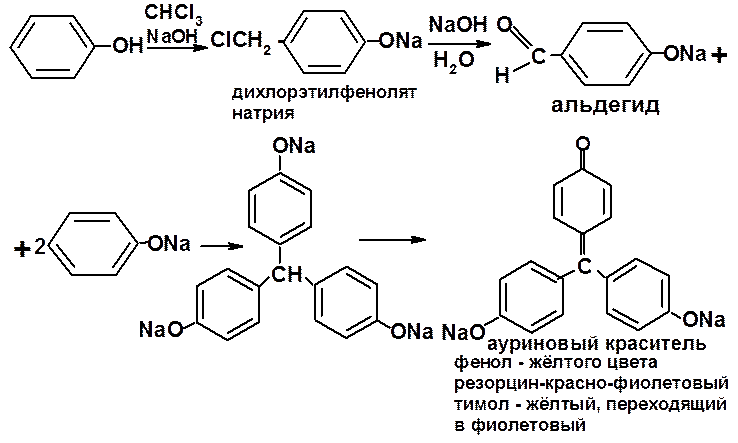
7.3. 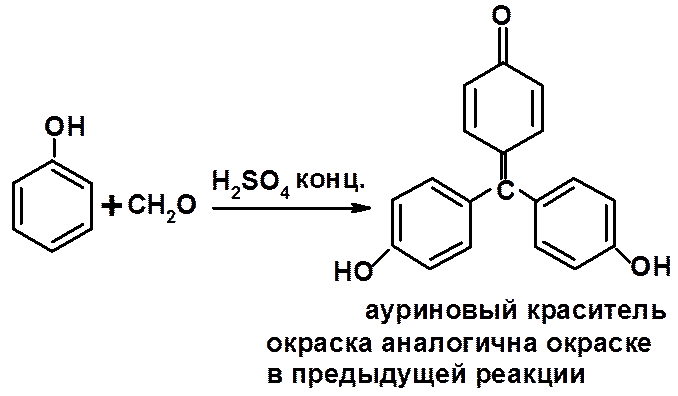 с реактивом Марки (раствор формальдегида в конц. H2SO4)
с реактивом Марки (раствор формальдегида в конц. H2SO4)
Количественное определение ЛВ фенолов:
(методы, основанные на реакциях замещения)
1. Метод прямой броматометрии (тимол) в сернокислой среде, индикатор – метилоранж:
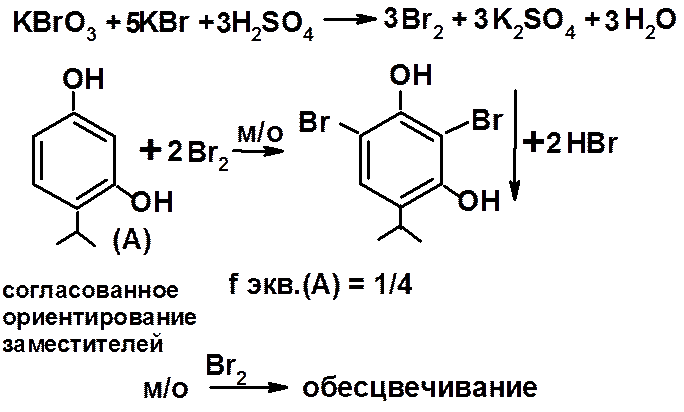
2. Метод обратной иодиметрии (резорцин, фенол) с иодиметрическим окончанием:

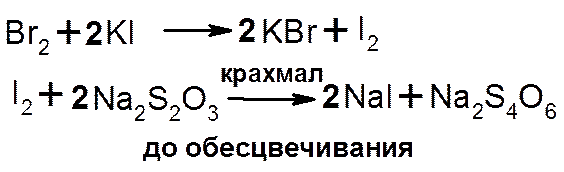
3. Метод обратной иодхлорметрии (иодиметрии):
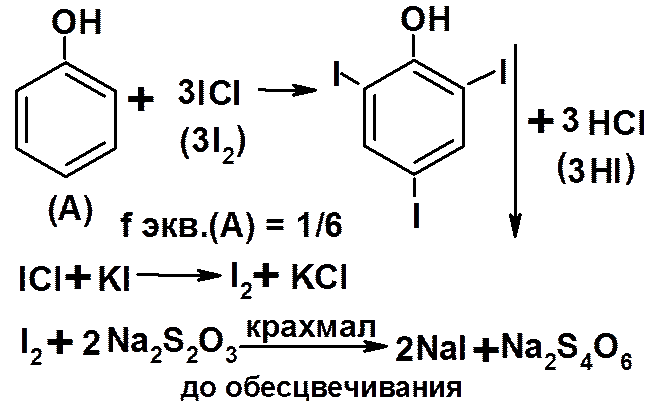
Физико-химические методы (в лекформах)
 2014-02-03
2014-02-03 4774
4774








