5.1. Розрахунок кількості водню в колошниковому газі
а) Утворюється водню при неповному горінні в доменній печі природного газу:
Vн2г= ПГ·(2·СН4пг+3·С2Н6пг+4·С3Н8пг+5·С4Н10пг+6·С5Н12пг)·0,01 =8,2·(2·94+3·1,5+4·0,8+5·0,2+6·0,4)·0,01=16,326,м3/100 кг чугуна.
б) Утворюється водню з вологи дуття по реакції:
Н2О + С = Н2 + СО
Vн2вол = Vд · φд · 0,01=152,384· 2 · 0,01=3,047, м3/100 кг чавуну.
в) Водень летких речовин коксу:
Vн2лк=К·Vк·Н2лк·10-4· 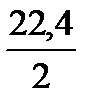 =49,972·1·25·10-4·11,2=1,399, м3/100 кг чавуну.
=49,972·1·25·10-4·11,2=1,399, м3/100 кг чавуну.
г) Водень органічної маси коксу:
Vн2орг= К·Н2орг·0,01· 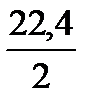 =49,972·0,4·0,01·11,2=2,238, м3/100 кг чавуну.
=49,972·0,4·0,01·11,2=2,238, м3/100 кг чавуну.
д) Приймаємо, що на реакції непрямого відновлення витрачається 1/3 частина водню, що утворюється в доменній печі.
е) Всього в колошниковому газі водню:
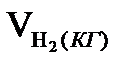 =(Vн2 г+Vн2 вол+Vн2 лк+Vн2 орг)·
=(Vн2 г+Vн2 вол+Vн2 лк+Vн2 орг)· 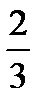 =(16,326+3,047+1,399+2,238)·
=(16,326+3,047+1,399+2,238)· 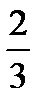 =
=
=15,341, м3/100 кг чавуну.
5.2. Розрахунок кількості СО2 в колошниковому газі
Основне джерело СО2 в доменному газі – це відновлення оксидів заліза за допомогою СО. Вищі оксиди заліза (Fe2O3 та Fe3O4) відновлюються до FеO повністю по реакціям непрямого відновлення. Для зручності обчислень будемо умовно вважати, що на цій стадії непряме відновлення оксидів заліза йде виключно за участю СО, а водень бере участь як відновник тільки лише на стадії відновлення FеO до Fе. Таке допущення не змінює результатів розрахунку.
У даних про хімічний склад агломерату та окатишів зазвичай указують загальний вміст Fе і вміст FеO. Природно, ні металевого заліза, ні FеO у вільному стані в залізорудних матеріалах немає. Вказана кількість FеO входить до складу інших сполук, наприклад, Fе3O4 = Fе2O3·FеO, але для розрахункового аналізу процесів відновлення будемо умовно вважати FеO вільним оксидом, а також що все інше залізо знаходяться у вигляді Fe2O3.
а) Усього Fe2O3 в шихті:
Fе2O3ш = 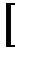 Fеч–0,01·(А·FеOа + О·FеOо)·
Fеч–0,01·(А·FеOа + О·FеOо)· 
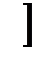 ·
· 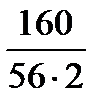 =
=
= 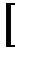 93,934-0,01·(146,531·13,2 + 25,922·1,29)·
93,934-0,01·(146,531·13,2 + 25,922·1,29)· 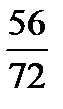
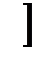 ·
· 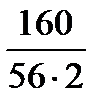 =
=
=112,329, кг/100кг чавуну,
де 56 – атомна маса заліза,
72 и 160 – молекулярні маси FeO и Fe2O3.
б) Кількість СО2, що утворюється при відновленні Fe2O3 до FeO по реакції:
Fe2O3 + СО = 2 FeO + СО2
Fe2O3ш · 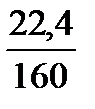 =112,329·0,14=15,726, м3/100кг чавуну.
=112,329·0,14=15,726, м3/100кг чавуну.
в) Відновлюється заліза з FeO непрямим шляхом:
Feч (1 – rd)=93,934·(1-0,374)=58,754, кг/100кг чавуну.
г) З цієї кількості відновлюється заліза воднем по реакції:
FeO + Н2 = Fe + Н2О
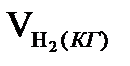 ·
· 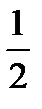 ·
· 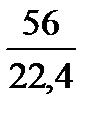 =15,341·0,5·2,5=19,176,кг/100кг чавуну.
=15,341·0,5·2,5=19,176,кг/100кг чавуну.
д) Відновлюється заліза по реакції:
FeO + СО = Fe + СО2
Feч·(1–rd) – 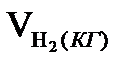 ·
· 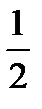 ·
· 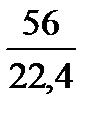 =58,754-19,176=39,577, кг/100кг чавуну.
=58,754-19,176=39,577, кг/100кг чавуну.
При цьому утворюється СО2:
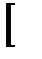 Feч·(1–rd) –
Feч·(1–rd) – 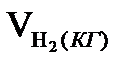 ·
· 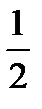 ·
· 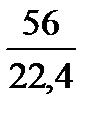
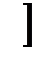 ·
· 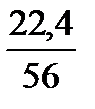 =15,831, м3/100кг чавуну.
=15,831, м3/100кг чавуну.
е) Усього утворюється СО2 при відновленні оксидів заліза:
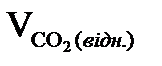 = Fe2O3ш·
= Fe2O3ш· 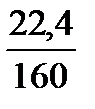 +
+ 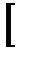 Feч·(1–rd) –
Feч·(1–rd) – 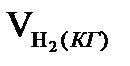 ·
· 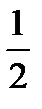 ·
· 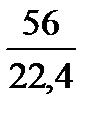
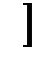 ·
· 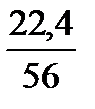 =15,726+15,831=31,557, м3/100кг чавуну.
=15,726+15,831=31,557, м3/100кг чавуну.
ж) СО2 летких речовин коксу:
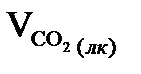 =К·Vк·СО2лк·10-4·
=К·Vк·СО2лк·10-4· 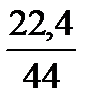 =49,972·1·9·10-4·0,51=
=49,972·1·9·10-4·0,51=
=0,022, м3/100 кг чавуну.
з) Кількість СО2 у колошниковому газі:
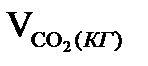 =
= 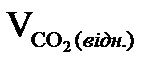 +
+ 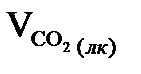 =31,557+0,022=31,580, м3/100 кг чавуну.
=31,557+0,022=31,580, м3/100 кг чавуну.
 2021-12-25
2021-12-25 251
251








