ПРАКТИЧЕСКАЯ РАБОТА № 1
ОПРЕДЕЛЕНИЕ ТЕРМОДИНАМИЧЕСКИХ ПАРАМЕТРОВ ГАЗОВОЙ СМЕСИ
Цель работы: определить термодинамические параметры газовой смеси по индивидуальным исходным данным.
Исходные данные
| Вариант | CO2 % | H2 % | N2 % | H2O % | SO2 % | CO % | O2 % | pсм кгс/см2 | vсм м3 | tсм °С |
| — | —— | — | 0,95 | |||||||
| — | — - | —— | 2 | 1,00 | ||||||
| — | —— | — | 0,90 | |||||||
| — | —— | — | 1,05 | |||||||
| — | —— | — | 1,05 | |||||||
| — | —— | — | 0,85 | |||||||
| — | —— | — | 0,70 | |||||||
| — | — | —— | — | 0,95 | ||||||
| — | — | — | 1,00 | |||||||
| — | — | — | 1,05 | |||||||
| — | — | — | 1,15 | |||||||
| — | — | 1,20 | ||||||||
| — | — | — | 1,25 | |||||||
| — | — | — | 1,05 | |||||||
| — | — | — | 0,85 | |||||||
| — | — | — | 1,20 | |||||||
| — | — | — | 1,00 | |||||||
| — | — | — | 0,90 | |||||||
| — | — | — | 1,00 | |||||||
| — | — | — | 1,05 | |||||||
| — | — | — | 1,05 | |||||||
| — | — | — | 1,00 | |||||||
| — | — | — | 0,95 | |||||||
| — | — | — | 1,15 | |||||||
| — | — | — | 0,85 | |||||||
| — | — | — | 0,95 | |||||||
| — | — | 1,2 | ||||||||
| — | — | — | 1,0 | |||||||
| — | — | — | 0,8 | |||||||
| — | — | 0,9 | ||||||||
| — | — | 1,05 | ||||||||
| — | — | 0,85 |
Содержание работы:
1. Выбрать исходные данные из таблицы, согласно своего варианта – номер по списку в учебном журнале.
2.. Выразить исходные данные в единицах системы СИ: pсм кгс/см2 = pсм Па, tсм°С = Т К
3. Определить состав смеси в массовых долях.
Так как содержание компонентов смеси задано в процентах, то для определения массовой доли достаточно значение, указанное в таблице, разделить на 100%. Например: CO2 =12%, следовательно, g CO2 = 0,12
3. Провести расчет параметров газовой смеси.
3.1. Определить молярную массу компонентов.
Молярная масса компонента определяется с помощью таблицы «Периодическая система элементов Д.Ф. Менделеева». По атомной массе компонента определяем молекулярную массу и соответственно молярную.
Например: атомная масса кислорода, примерно, равна 16, а молекулярная 32, т.к. в молекуле кислорода два атома. Соответственно молярная масса кислорода будет составлять µО2 = 32 кг/кмоль, молекулярная масса СО2 = 12+ (16*2) = 44, следовательно µсо2 =44 кг/кмоль.
3.2. Определить газовые постоянные компонентов смеси
R i = 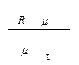
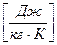
 ,
,
где R i 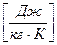 - удельная газовая постоянная компонента смеси,
- удельная газовая постоянная компонента смеси,
Rµ = 8314  - универсальная газовая постоянная,
- универсальная газовая постоянная,
µi 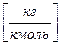 - молярная масса компонента смеси.
- молярная масса компонента смеси.
 2022-01-07
2022-01-07 452
452







