Таблицы термодинамических свойств воды и водяного пара
Для определения параметров состояния воды и водяного пара служат таблицы термодинамических (теплофизических) свойств воды и водяного пара. Современные таблицы составлены с использованием Международной системы единиц СИ. В таблицах приняты следующие обозначения физических величин и их размерности:
p – давление, Па: 1 МПа = 103 кПа = 106 Па = 10 бар;
Т – температура, К;
t – температура, оС:
v – удельный объем, м3/кг;
h – удельная энтальпия, кДж/кг;
s – удельная энтропия, кДж/(кг×град).
В термодинамических расчетах принято параметры (кроме p и t) обозначать для жидкости при температуре насыщения (кипения) индексом "штрих" (v ', h ', s '), для сухого насыщенного пара индексом "два штриха" (v '', h '', s ''), а для влажного насыщенного пара индексом " х " (vх, hх, sх). В таблицах приводятся также значения удельной теплоты парообразования r = h '' – h ' и разности энтальпии в состоянии насыщения s '' и s '.
Для влажного насыщенного пара (степень сухости 0< x < 1) параметры пара рассчитываются по формулам:
vx = v ' + x (v '' – v '); (2.74)
h x = h ' + x (h '' – h ') = h ' + x×r; (2.75)
s x = s ' + x (s '' – s '). (2.76)
Причем, v ' < v x < v ''; h ' < hx < h ''; s ' < sx < s ''.
Для жидкости при t < t н и для перегретого пара при t > t н параметры воды и пара находятся по таблице перегретого пара
При p £ p кр = 22,115 МПа таблица поделена горизонтальной линией на две части: верхняя – для области жидкости; нижняя – для перегретого пара. Граница раздела этих областей проходит при t = t н.
При p > p кр нет видимого фазового перехода воды в пар и вещество остается однородным (жидкость или пар). Условная граница между жидкостью и паром в этом случае может приниматься по критической изотерме.
Внутренняя энергия для воды и водяного пара в таблицах не приводится, она определяется по формуле:
u = h – p × v. (2.77)
Если u и h имеют размерность кДж/кг, то давление должно быть выражено в кПа, а удельный объем в м3/кг.
Диаграмма h – S (энтальпия – энтропия) находит широкое применение при расчетах паровых процессов и циклов теплоэнергетических установок.
Для практических целей диаграмма h – s выполняется не для всех фазовых областей воды, а только для ограниченной области водяного пара (рис. 2.17).
На рабочей диаграмме h – s наносится густая сетка изобар, изохор, изотерм и линий постоянной степени сухости х. Как уже отмечалось, в области влажного насыщенного пара изотерма совпадает с изобарой, причем геометрически это прямые линии. Чем выше давление, тем изобара круче и ближе к оси ординат.
На практике расчету подлежат четыре основных термодинамических процесса изменения состояния воды и водяного пара: изобарный (p = const), изохорный (v = const), изотермический (Т = const), адиабатный (dq = 0). Изображение указанных процессов в диаграммах p – v и T – s показано на рис. 2.15 и 2.16.
Состояние влажного насыщенного пара определяется в технике давлением р и степенью сухости х. Точка, изображающая этот состояние, находится на пересечении изобары и линии х = const. Состояние перегретого пара определяется давлением р и температурой t. Точка, изображающая состояние перегретого пара лежит на пересечении соответствующей изобары и изотермы.
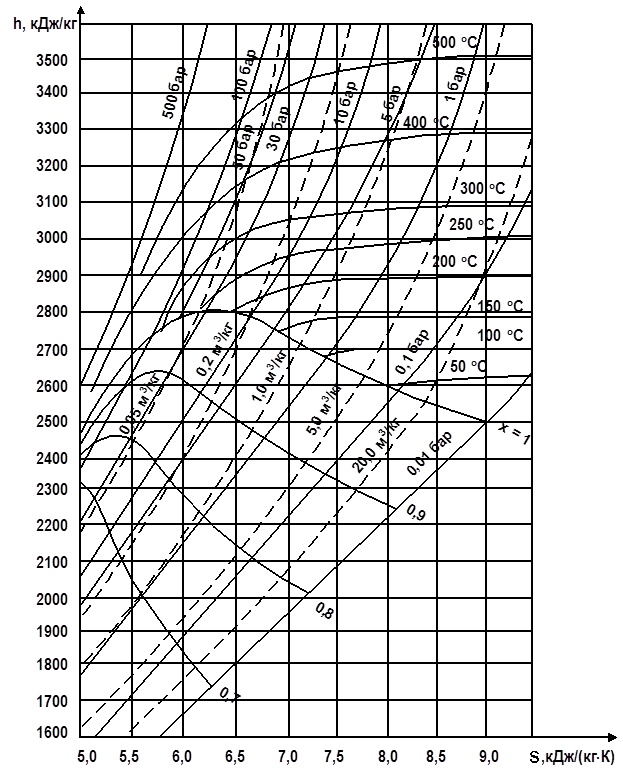
Рис. 2.17 Рабочая h–s диаграмма водяного пара
Расчеты основных процессов водяного пара можно проводить как аналитическим, так и графическим методом, с применением h – s диаграммы. Аналитический метод сложен из-за громоздкости уравнений состояния водяного пара.
В таблице 2.4 приведены расчетные формулы для определения количества теплоты, работы изменения объема, и изменения внутренней энергии для основных термодинамических процессов.
Таблица 2.4: Расчетные формулы основных термодинамических процессов
| Процесс | q, кДж/кг | l, кДж/кг | D u, кДж/кг |
| p = const | h 2 – h 1 | p (v 2 – v 1) | h 2 – h 1 – p (v 2 – v 1) |
| v = const | u 2 – u 1 | h 2 – h 1 – v (p 2 – P 1) | |
| Т = const | T (s 2 – s 1) | q – D u | h 2 – h 1 – (p 2 v 2 – p 1 v 1) |
| dq = 0 | u 1 – u 2 | h 2 – h 1 – (p 2 v 2 – p 1 v 1) |
 2014-02-24
2014-02-24 10270
10270








