Рисунок 10.4
Рисунок 10.3
Рисунок 10.2
Гидрофильная оболочка Мицелла
Схема мицеллообразования.
Мицеллы имеют коллоидные размеры и содержат большое количество молекул (до 200). Размеры мицелл ограничиваются силами электростатического отталкивания между сближенными полярными группами и Ван-дер-Ваальсовыми силами притяже-ния между неполярными группами. В результате образуется неполярное ядро с гидрофильной оболочкой. Мицеллы обладают объемной емкостью, т.е. имеют пустоты, которые могут быть заполнены другими молекулами без нарушения термодинамической стойкости системы.
В зависимости от свойства вещества его солюбилизация в водной среде осуществляется по одному из трех возможных способов.
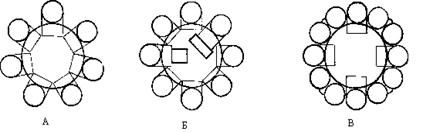
Возможные способы солюбилизации (растворения)
А. Неполярного вещества.
Б. Вещества с полярной и гидрофобной частью.
В. Вещества без гидрофобной части, содержащих несколь-ко полярных групп.
1. Механизм растворения (солюбилизации) неполярных органических (А) веществ в присутствии ПАВ в водной среде с ПАВ представляет собой проникновение молекул этого вещества внутрь неполярных гидрофобных групп мицеллы ПАВ.
2. Соединения, содержащие полярную группу и достаточ-но большой углеводородный радикал (Б), при солюбилизации в водной среде располагаются так, что их углеводородный "хвост" находится внутри мицеллы, а полярная группа была обращена наружу. Причем, неполярные группы таких соединений проникают между молекулами ПАВ внутрь мицелл и занимают там свое место параллельно или почти параллельно неполярным гидрофобным группам молекул ПАВ.
3. Для соединений, содержащих несколько полярных групп (В), наиболее вероятна их адсорбция на поверхности мицелл.
Экспериментально установлено, что солюбилизация углеводородов падает с ростом длины цепи, солюбилизирующая способность ПАВ в пределах одного гомологического ряда возрастает по мере увеличения числа углеводородных атомов. Неионогенные соединения отличаются меньшей солюбилизирующей активностью по сравнению с ионогенными. Исключительно высока солюбилизирующая активность холата и дезоксихолата натрия.
В неводных растворителях (углеводородных) структура мицеллы «обратна» по отношению к структуре мицелл в воде: углеводородные цепи направлены наружу, к поверхности раздела мицелла - вода, а полярные группы находятся внутри или в ядре мицеллы. Солюбилизация в неводных средах называется "обратной солюбилизацией".
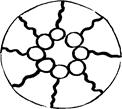
Схема «обратной солюбилизации»
Процесс обратной солюбилизации также используется в фармацевтической практике для создания лекарств, облада-ющих пролонгированным действием (например, масляный раствор витамина В12).
Установлено, что на процесс солюбилизации влияют такие факторы, как температура, природа и концентрация ПАВ, добавление электролитов, алифатических спиртов и других веществ.
Принципиального различия в механизме процессов солюбилизации и гидротропии нет, так как в основе обоих процессов лежит межмолекулярное притяжение растворителя и растворяемого вещества. Разница в количествах гидротропного вещества и ПАВ, необходимых для повышения растворимости труднорастворимых веществ, объясняется различием структуры их (истинных и коллоидных) растворов. ПАВ в растворе образуют коллоидные агрегаты – мицеллы, которые и обеспечивают растворение. Гидротропные вещества создают истинный раствор, в котором молекулы равномерно распределе-ны по всему объекту. Отрыв молекулы труднорастворимого вещества от твердой фазы в первом случае осуществляется молекулярным агрегатом - мицеллой, во втором - накоплением довольно значительного количества отдельных молекул гидротропного вещества вокруг молекул труднорастворимого вещества.
Типичными солюбилизированными препаратами являются ихтиол (тифеновое масло солюбилизировано аммонийной солью сульфоихтиоловой кислоты), вазолименты (вазелиновое масло солюбилизировано в спиртовой среде аммониевым мылом), мыльно-крезоловые препараты и многие другие.
В настоящее время широко используется возможность получения солюбилизированных препаратов. Наиболее эффек-тивными солюбилизаторами оказались твины. Установлено, что растворимость бензойной, салициловой, ацетилсалициловой кислот, рибофлавина, кодеина, стрептоцида и сульфаниламидов возрастает в 2-5%-ных растворах различных твинов в 1,2 - 2,3 раза. С помощью солюбилизации получены водные растворы синтомицина (0,6 - 0,9%), дибазола (1,9%), фурацилина (0,09 - 1,0%).
В последнее время предложены солюбилизированные препараты нитрофурановых соединений (фурагина, фурадонина, солафура) в концентрации до 1,5%.
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ ПРИГОТОВЛЕННЫЕ С ИСПОЛЬЗОВАНИЕМ ПРИНЦИПА МИЦЕЛЛООБРАЗОВАНИЯ.
 Наночастицы или нанокапсулы получают путем полимеризации ряда мономеров с последующим образованием мицеллы, включающей (неводный) липофильный раствор лекарственного вещества. Первоначально солюбилизацию лекарственного вещества проводят с помощью веществ, способных в дальнейшем к полимеризации:
Наночастицы или нанокапсулы получают путем полимеризации ряда мономеров с последующим образованием мицеллы, включающей (неводный) липофильный раствор лекарственного вещества. Первоначально солюбилизацию лекарственного вещества проводят с помощью веществ, способных в дальнейшем к полимеризации:
- производные алкилцианакрилатной и метилакрилатной кислот;
- из природных веществ - это альбумины сыворотки крови, желатин и другие.
Впоследствии в систему вводят полимеризующий агент и (или) процесс полимеризации индуцируют с помощью лучей, УФ - облучения. Образующиеся мицеллы - наночастицы - размером от 10 до 1000 нм, удельной поверхности 10 м2/г. В центральной полости таких нанокапсул находятся липофильные лекарственные вещества. Гидрофильные вещества чаще адсорбируются на поверхности наночастиц.
Скорость высвобождения лекарственных веществ из наночастиц связана со скоростью разрушения этих частиц и может контролироваться выбором соответствующего мономера или природного материала.
Диспергированные в воде для инъекций наночастицы вследствие их малого размера образуют прозрачные или опалесцирующие растворы, применяемые для парентерального введения.
На фармацевтическом факультете Парижского универси-тета разработан способ получения наночастиц размером 200-300 нм путем полимеризации изобутилцианакрилата - последний при контакте с водой самопроизвольно полимеризуется с образованием биоразрушающегося полимера.
По сравнению с известными наночастицами на основе метилметакрилата и полиалкил-2-цианакрилата предложенные нанокапсулы обладают рядом преимуществ. Их получение проводят при комнатной температуре и рН близкому к нейтральному показателю среды, что повышает стабильность многих лекарственных веществ. Очень высока степень захватывания активного вещества липофильного характера центральной полостью нанокапсулы. Полученные наночастицы стабильны, их можно стерилизовать автоклавированием, такие частитцы из полиизобутилцианакрилата биоразрушаются и нетоксичны.
Одной из разновидностей наночастиц являются наночасти-цы, приготовленные на основе лецитина, пальмитиновой кислоты, казеината натрия, гликолята натрия и соевого масла с растворенными в последнем лекарственными веществами: противовоспалительными веществами, кортикостероидами, простагландинами и др.
 Эти наночастицы получили название липидных микросфер. Они (подобно липосомам) захватываются клетками (эндоцитоз) моноцитами и фагоцитами, тем самым могут явиться средством доставки лекарственного вещества непосредственно к органу-мишени - в органы ретикулоэндотели-альной системы (печень, селезенка и др.). Причем такие наночастицы накапливаются вокруг эндотелиальных клеток кровеносных сосудов и проникают в них.
Эти наночастицы получили название липидных микросфер. Они (подобно липосомам) захватываются клетками (эндоцитоз) моноцитами и фагоцитами, тем самым могут явиться средством доставки лекарственного вещества непосредственно к органу-мишени - в органы ретикулоэндотели-альной системы (печень, селезенка и др.). Причем такие наночастицы накапливаются вокруг эндотелиальных клеток кровеносных сосудов и проникают в них.
Липидные микросферы, изготовленные из пальмитиновой кислоты, казеината натрия, гликолята натрия и включенными растворами цитостатиков в соевом масле с добавкой яичных фосфолипидов, используются для в/в введения как транспортные системы для доставки лекарственных веществ в лимфатические узлы и в саму опухоль.
К преимуществам таких систем относятся их биоразруша-емость, возможность промышленного производства ввиду их высокой стабильности.
К недостаткам - необходимость проведения дополнитель-ных клинических и технологических испытаний.
 2014-02-24
2014-02-24 1638
1638








