Сера
Кислород
Кислород является самым распространённым элементом земной коры. Молекула кислорода двухатомна (О2). Простое вещество - молекулярный кислород - представляет собой газ без цвета и запаха, плохо растворимый в воде. В воздухе содержится 21 % (по объёму) кислорода. В природных соединениях кислород встречается в виде оксидов (Н2О, SiО2) и солей кислородных кислот. Промышленный способ получения кислорода – ректификация жидкого воздуха. Хранят в жидком состоянии воздух, азот и кислород хранят в сосудах Дъюара.
Кислород играет важную роль в природе. Он участвует в жизненно важном процессе – дыхании. Применение его разнообразно. Производство серной и азотной кислот, выплавка металлов, получение высоких температур и т.д.
Аллотропной модификацией кислорода является озон (O3). Озон - один из сильнейших окислителей; по окислительной активности он уступает только фтору. Он окисляет все металлы, кроме золота и платиновых металлов, а также большинство неметаллов. В стратосфере земли образует озоновый слой, поглощающий основную часть ультрафиолетового излучения. Для обнаружения озона применяется следующая реакция
2КI + О3+Н2О = I2 + 2КОН + О2.
Важным соединением кислорода является Н2О2 – пероксид водорода (Н–О–О–Н). Атомы кислорода находятся в промежуточной степени окисления -1 и поэтому могут проявлять как окислительные, так и восстановительные свойства:
Н2О2 + 2КI = I2 + 2КОН
2О-1 + 2 е = 2О-2,
2I- - 2е = I2;
5Н2О2 + 2КМnО4 + 3Н2SО4 = 5О2 + 2Мn SО4 + К2SО4 + 8Н2О
2О-1 - 2 е = О2,
2 Мn+7 + 5е = Мn+2.
Пероксид водорода в кислой среде способен окислять вещества, стандартный электродный потенциал которых не превышает +1,776 В, и восстанавливать только те, у которых потенциал больше +0,682 В.
Известны несколько аллотропных модификаций серы: ромбическая сера, моноклинная, пластическая. При нормальных условиях сера - твёрдое жёлтое вещество, нерастворимое в воде, но хорошо растворимое в органических растворителях.
Сера со многими металлами (Zn, Al, Fe, Сu, щелочные и щелочноземельные металлы) взаимодействует непосредственно
2Аl + 3S → Al2S3.
При высокой температуре сера взаимодействует с водородом с образованием сероводорода (H2S) – бесцветный газ с характерным запахом (тухлых яиц)
Н2 + S → Н2S.
Сероводород очень ядовит и способен вызвать тяжёлые отравления.
Сероводородная кислота является слабой двухосновной кислотой
Н2S ↔ H+ + НS-, К1 = 6∙10-8,
НS- ↔ H+ + S-2, К2 = 1∙10-14.
Сероводородная кислота образует соли –сульфиды, характеризующиеся низкой растворимостью
CuSO4 + H2S → CuS↓ + H2SO4,
Cu2+ + SO42- + H2S → CuS↓ + 2H+ + SO42-,
Cu2+ + H2S → CuS↓ + 2H+.
Протекание этой реакции возможно потому, что произведение растворимости образующегося сульфида меди меньше общей константы диссоциации сероводородной кислоты:
ПP(CuS) = 6∙10-36 << Кобщая(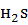 )=К1∙ К2 =6∙10-22.
)=К1∙ К2 =6∙10-22.
При поджигании на воздухе сероводород горит голубоватым пламенем
2 H2S + 3 O2 → 2 SO2 + 2 Н2O (в избытке кислорода).
Оксид серы (IV) образуется при горении серы на воздухе. Он хорошо растворяется в воде с образованием сернистой кислоты
SO2 + Н2O ↔ H2SO3.
Сернистая кислота – слабая двухосновная кислота (К1=1,6∙10-2, К2=6∙10-8). Её соли являются хорошими восстановителями и окисляются до серной кислоты или сульфатов
2 H2SO3 + O2 → 2 H2SO4.
При высокой температуре в присутствии катализатора (V2O5, сплавы на основе платины) диоксид серы окисляется кислородом до триоксида, который в свою очередь используется для получения серной кислоты:
2SO2 + O2 → 2SO3,
SO3 + Н2O → Н2SО4.
Концентрированная серная кислота, особенно горячая, - энергичный окислитель. Она восстанавливается до SO2, S или Н2S. Чем более активен металл, тем более глубоко восстанавливается кислота.
Сu + 2 Н2SO4 (конц.) → СиSO4 + SO2↑ + 2 Н2O;
3 Zn + 4 Н2SO4(конц.) → 3 ZnSО4 + S↓ + 4 Н2O.
Н2SO4 - сильная двухосновная кислота. В разбавленных водных растворах она диссоциирует практически полностью по схеме:
Н2SO4 → 2 Н+ + SO42-.
Олеум - это раствор SO3 в концентрированной серной кислоте.
В ряду Н2O – Н2S − Н2Sе − Н2Те с увеличением молекулярных масс должно наблюдаться повышение температур кипения. Как видно из рисунка 3 данная зависимость соблюдается, за исключением Н2О. Установлено, что аномальное повышение температуры кипения Н2О является следствием образования водородных связей между отдельными молекулами воды.
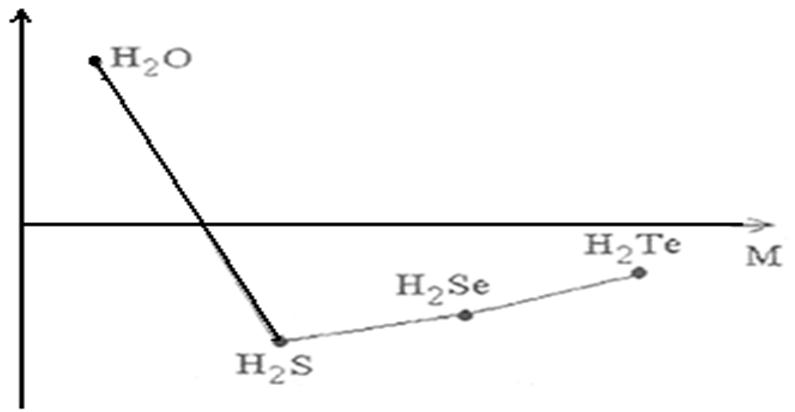
Рисунок 3 – зависимость температуры кипения водородных соединений р-элементов VI группы от молекулярной массы
 2014-02-09
2014-02-09 2831
2831








