ФЕРМЕНТЫ (продолжение).
1. КЛАСИФИКАЦИЯ ФЕРМЕНТОВ.
3. ФЕРМЕНТЫ ВМЕДИЦИНЕ.
Всего насчитывается 1800 ферментов, из них в чистом виде выделено 150. В 1961 г. в Москве состоялась международная комиссия по классификации и номенклатуре ферментов.
Согласно её работе, все ферменты были разделены на 6 классов, каждый из которых указывает тип каталитической реакции.
1. ОКСИДОРЕДУКТАЗЫ.
2. ТРАНСФЕРАЗЫ.
3. ГИДРОЛАЗЫ.
4. ЛИАЗЫ.
5. ИЗОМЕРАЗЫ.
6. ЛИГАЗЫ.
Каждый класс делится на подклассы. Они уточняют действие ферментов и указывают на химическую природу группы, которую атакует фермент. Подклассы делятся на ПОДПОДКЛАССЫ, которые ещё более конкретизируют действие ферментов, указывают на связь в молекуле субстрата, которая подвергается действию фермента. ПОДПОДКЛАСС может указывать на химическую природу акцептора.
1.ОКСИДОРЕДУКТАЗЫ.
Ферменты этого класса участвуют в ОВР (окислительно-восстановительные реакции), т.е. в реакциях транспорта электронов и протонов. Это наиболее многочисленный класс ферментов: насчитывается более 400 ОКСИДОРЕДУКТАЗ. Здесь выделяют 17 подклассов.
1.АЭРОБНЫЕ ДЕГИДРОГЕНАЗЫ.
Они участвуют в реакциях ДЕГИДРИРОВАНИЯ, при этом они отнимают атомы Н2 от окисленного субстрата и транспортируют их на О2.

Некоторые АЭРОБНЫЕ ДЕГИДРОГЕНАЗЫ называют ОКСИДАЗАМИ. Например, ОКСИДАЗЫ АК.
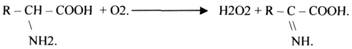
2.АНАЭРОБНЫЕ ДГ.
Эти ферменты также участвуют в реакциях ДЕГИДРИРОВАНИЯ, т.е. отнятия Н2 от окисляемого субстрата и транспортировка его на любой др. субстрат, кроме О2.
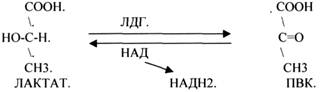
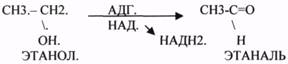
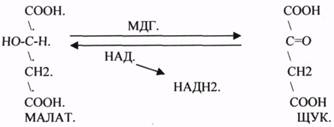
3.ПЕРОКСИДАЗЫ.
Это группа ферментов, которые отнимают Н2 от окисляемого субстрата и транспортируют его на ПЕРОКСИД.
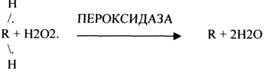
КАТАЛАЗА катализирует разложение Н2О2 до Н2О и молекулярного О2
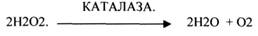
4.ЦИТОХРОМЫ.
Они содержат в своем составе ГЕМ а следовательно ионы железа, степень окисления которого может изменяться. ЦИТОХРОМЫ участвуют в транспорте только электронов.
2.ТРАНСФЕРАЗЫ.
Ферменты этого класса участвуют в транспорте атомных групп от одного субстрата к другому. Субстрат, от которого группа отнимается, является донором, а субстрат, который её принимает, является акцептором. В зависимости от переносимых групп, ТРАНСФЕРАЗЫ делятся на несколько подклассов:
1.АМИНОТРАНСФЕРАЗЫ. Они участвуют в реакциях ПЕРЕАМИНИРОВАНИЯ.
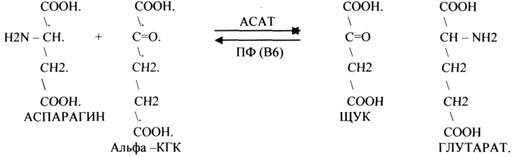
АСАТ - АСПАРАГИНОВАЯ АМИНОТРАНСФЕРАЗА.
2.МЕТИЛТРАНСФЕРАЗЫ (СНЗ группы).
3.ФОСФОТРАНСФЕРАЗЫ (ФОСФАТНЫЕ группировки).
4.АЦИЛТРАНСФЕРАЗЫ (кислотные остатки).
3.ГИДРОЛАЗЫ.
Ферменты этого класса участвуют в реакциях разрыва связей в молекулах субстратов при участии воды. При этом элементы воды присоединяются к свободным единичным валентностям, образовавшимся после разрыва связей. Т.о. сложные органические соединения распадаются на простые - каталитические реакции гидролиза. В зависимости от разрушаемых связей, различают следующие подгруппы ГИДРОЛАЗ.
1.ЭСТЕР АЗЫ действуют на СЛОЖНО-ЭФИРНЫЕ связи. К ним относятся ЛИПАЗЫ, ФОСФОЛИПАЗЫ, ХОЛЕСТЕРАЗЫ.
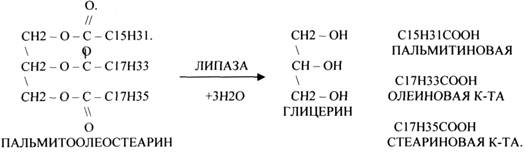
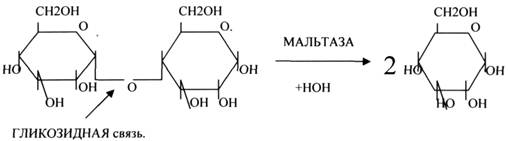
2.ГЛИКОЗИДАЗЫ - действует на ГЛИКОЗИДНУЮ связь, находящуюся в сложных углеводах. К ним относятся АМИЛАЗА, САХАРАЗА, МАЛЬТАЗА, ГЛИКОЗИДАЗЫ, ЛАКТАЗА.
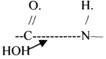
3.ПЕПТИДАЗЫ участвуют в разрыве ПЕПТИДНЫХ связей в белках. К ним относятся ПЕПСИН, ХИМОТРИПСИН, АМИНОПЕПТИДАЗА, КАРБОКСИПЕПТИДАЗА и т.д.
4.ЛИАЗЫ.
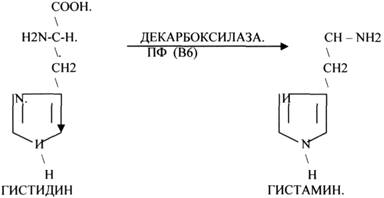
1.ДЕКАРБОКСИЛАЗЫ участвуют в реакциях ДЕКАРБКСИЛИРОВАНИЯ.
2.Ферменты, участвующие в разрыве связей между атомами углеводов не ГИДРОЛИТИЧЕСКИМ путём без участия воды. К ним относится АЛЬДОЛАЗА.
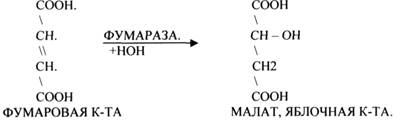
3.Ферменты, участвующие в реакциях ГИДРАТАЦИИ и ДЕГИДРАТАЦИИ.
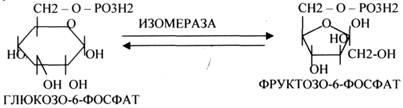
5.ИЗОМЕРАЗЫ.
Ферменты этого класса участвуют в ИЗОМЕРИЧЕСКИХ превращениях. При этом один структурный изомер может превращаться в другой, за счёт внутри молекулярной перегруппировки атомов.
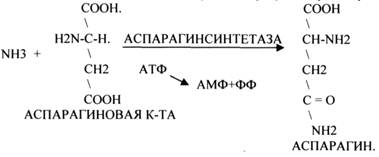
6.ЛИГАЗЫ.
Ферменты этого класса участвуют в реакциях соединения двух и более простых веществ с образованием нового вещества. Эти реакции требуют затрат энергии извне в виде АТФ.
НОМЕНКЛАТУРА ФЕРМЕНТОВ.
1.Тривиальная номенклатура. ПРИМЕР: пепсин, трипсин.
2.Рабочая номенклатура:
название S + тип превращения + окончание «аза».
ПРИМЕР: ЛАКТАТДЕГИДРОГЕНАЗА.
3.Систематическая номенклатура.
Название всех S, + тип каталитического + окончание «аза» участвующих в реакции превращения
ЕДИНИЦЫ АКТИВНОСТИ ФЕРМЕНТОВ. Мерой активности фермента могут быть скорость превращения субстрата и концентрация образующегося продукта реакции. Согласно современной классификации по системе СИ, единицей активности является КАТАЛ. КАТАЛ - это количество фермента, которое способно осуществить превращение 1 молекулы субстрата в 1 секунду при стандартных условиях.
Основное направление медицинской ЭНЗИМОЛОГИИ:
1.ЭНЗИМОПАТОЛОГИЯ (патологическое состояние, связанное с полным отсутствием фермента в организме).
2.ЭНЗИМОДИАГНОСТИКА (определение активности ферментов в диагностических целях). 3.ЭНЗИМОТЕРАПИЯ (использование ферментов в лечебных целях).
Лекция № 7. Основной путь катаболизма (ОПК).
1.ПОНЯТИЕ ОБ ОБМЕНЕ ВЕЩЕСТВ.
2.ЭТАПЫ ОБМЕНА ВЕЩЕСТВ.
3.ОПК, ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦТК).
ПОНЯТИЕ ОБ ОБМЕНЕ ВЕЩЕСТВ.
Обмен веществ - необходимое условие жизни, но он протекает и вне живой природы. Обмен веществ всегда связан с обменом энергии. Системы, обменивающиеся с окружающей средой веществом и энергией, называются открытыми (живой организм). Закрытые системы обмениваются только энергией. В соответствии со 2 законом термодинамики, открытые системы являются более устойчивыми. Отличительной особенностью обмена веществ в живой природе от обмена веществ в неживой системе является способность образовывать дочерние структуры из поступивших веществ.
Обмен веществ - это процессы взаимоотношения организма с внешней средой, представляющие совокупность химических реакций, которым подвергаются различные вещества с момента их поступления в организм до момента их выделения в виде конечных продуктов. Основные компоненты живых систем - белки, жиры, углеводы. В организм человека должно поступать: Белков - 100 г. в сутки, Жиров - 100 г. в сутки, Углеводов - 400 г. в сутки.
За сутки при обмене этих веществ образуется 2000-3000 ккал энергии.
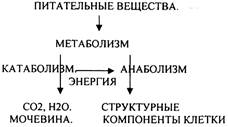
ЭТАПЫ ОБМЕНА ВЕЩЕСТВ.
1.Поступление веществ из внешней среды посредством питания и дыхания.
2.Превращение веществ в организме - МЕЖУТОЧНЫЙ обмен
3.Выделение конечных продуктов.
Распад БЖУ до ПИРУВАТА идёт индивидуально для каждой группы органических соединений и носит название специфического пути катаболизма. С образованием ПИРУВАТА начинается общий путь катаболизма, идентичный для обмена всех питательных веществ.
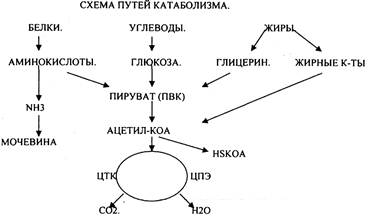
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ. ОПК можно разделить на несколько стадий:
1.Превращение ПВК в АЦЕТИЛ-КОА.
2.Распад АЦЕТИЛ-КОА в ЦТК (образование СО2).
3.Образование воды как конечного продукта в ЦПЭ— цикле пере носа электронов. ПРЕВРАЩЕНИЕ ПИРУВАТА В АЦЕТИЛ-КОА.
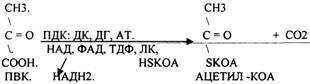
ПИРУВАТ подвергается реакции ОКИСЛИТЕЛЬНОГО ДЕКАРБОКСИЛИРОВАНИЯ. Этот процесс катализируется комплексом ферментов - ПИРУВАТДЕКАРБОКСИЛАЗНЫМ комплексом (ПДК), с участием в процессе 5 КОФЕРМЕНТОВ:
1.ДЕКАРБОКСИЛАЗЫ (включают КОФЕРМЕНТ - ТДФ).
2.АЦЕТИЛТРАНСФЕРАЗЫ (включают КОФЕРМЕНТ - ЛК, HSK.OA).
3.ДЕГИДРОГЕНАЗЫ (включают КОФЕРМЕНТ - НАД, ФАД, ЛК). ЦТК (цитратный цикл, цикл КРЕБСА).
В цикле КРЕБСА АЦЕТИЛ-КОА распадается до СО2 с образованием восстановленных КОФЕРМЕНТОВ - НАДН

АТФ в реакции не участвует, а используется энергия макроэргической связи АЦЕТИЛ-КОА ЦИТРИЛ-КОА не устойчив и очень быстро распадается под влиянием воды.
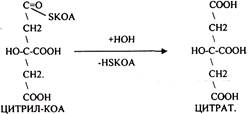
Лимонная кислота далее превращается в свой изомер (ИЗОЦИТРАТ) под влиянием фермента АКОНИТАЗЫ.
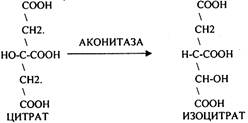
ИЗОЦИТРАТ подвергается далее ДЕГИДРИРОВАНИЮ под влиянием фермента -ИЗОЦИТРАТДЕГИДРОГЕНАЗЫ.
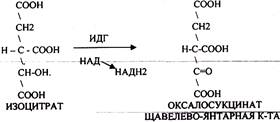
ЩЯВЕЛЕВО-ЯНТАРНАЯ К-ТА подвергается ДЕКАРБОКСИЛИРОВАНИЮ достаточно легко и не требует участия дополнительных ферментов - ПРЯМОЕ ДЕКАРБОКСИЛИРОВАНИЕ.
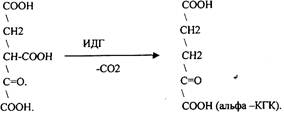
a-КГК подвергается реакции ОКИСЛИТЕЛЬНОГО ДЕКАРБОКСИЛИРОВАНИЯ, катализируемой комплексом ферментов (КЕТОГЛУТАРАТДЕГИДРОГЕНАЗНЫЙ комплекс), включающий 3 фермента и 5 КОФЕРМЕНТОВ.

СУКЦИНИЛ-КОА подвергается реакции субстратного ФОСФОРИЛИРОВАНИЯ.
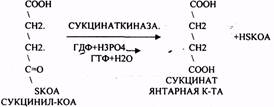
ГТФ + АДФ = ГДФ + АТФ
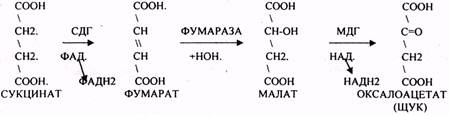
Т.о. происходит распад АЦЕТИЛ-КОА до СО2 и восстановленного HSKOA.
ФУНКЦИИ ЦТК.
1.Катаболическая - распад АЦЕТИЛА.
2.Анаболическая. Компоненты ЦТК могут использоваться для синтеза др. соединений
ЩУК - синтез АСП, МАЛAT - синтез глюкозы и т.д.
3.Интегративная. Взаимосвязь обмена БЖУ.
4.Энергетическая. Образование 1 молекулы АТФ. Если ЦТК работает вместе с дыхательной цепью, то образуется ещё 1 молекул АТФ.
5.ВОДОРОДГЕНЕРИРУЮЩАЯ - в результате ЦТК образуется 3 молекулы НАДН2 и 1 молекула ФАДН2, т.е. 4 пары молекул водорода. Они транспортируются в ЦТЭ.
 2014-02-12
2014-02-12 1473
1473








